Харчові розлади ЦНС
СИНДРОМ ВЕРНІКЕ-КОРСАКОФФА
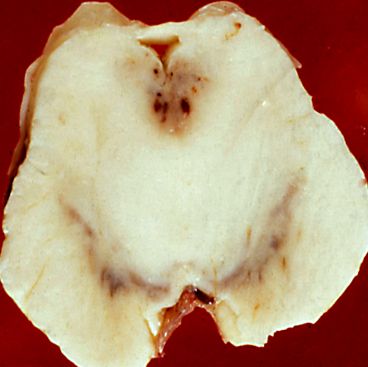
WKS, гостре ураження. Періакведуктальні ураження.
WKS обумовлений дефіцитом тіаміну (B1). Тіамінпірофосфат, активна форма тіаміну, необхідний для окисного метаболізму пірувату для виробництва АТФ. Топографія вогнищ ураження в СРК нагадує Синдром Лі, порушення обміну речовин, спричинене дефектами піруватдегідрогеназного комплексу та дихального ланцюга. Це свідчить про те, що пошкодження чутливих структур ЦНС в СРК відбувається через відмову енергії. Тіамін зберігається в декількох органах (серце, нирки, печінка, мозок, м’язи). Ці магазини можуть виснажуватися у пацієнтів з недостатнім харчуванням. Алкоголь витісняє з раціону більш поживну їжу, додає вуглеводи, що витрачають тіамін, і погіршує засвоєння вітамінів. Внутрішньовенне введення глюкози пацієнту з прикордонним дефіцитом тіаміну може спричинити WKS. Тому доповнення вітаміном В1 є обов’язковим для пацієнтів групи ризику.
СЕРЕДНЯ ЦЕНТРАЛЬНА ДЕГЕНЕРАЦІЯ
Дегенерація мозочка середньої лінії (також звана алкогольною дегенерацією мозочка) є складовою WKS, але може також відбуватися і окремо. Це викликає атаксію пози та ходи при відносному щадінні рук. Має підступний початок і підгострий або хронічний перебіг. Патологічно спостерігається втрата Пуркіньє та зернистих нейронів. У більшості випадків ураження приурочені до верхніх вермісів, що є дуже атрофічним.
У важких випадках дегенерація поширюється на півкулі мозочка, викликаючи атаксію рухів ніг. Локалізація патології у верхній частині вермісу відрізняє цю сутність від інших сімейних та спорадичних дегенерацій мозочка.
ДЕФІЦИТ ВІТАМІНУ Е
Дефіцит розчинного у ліпідах вітаміну Е виникає у випадках кишкової мальабсорбція такі як муковісцидоз, вроджена атрезія жовчних шляхів, резекція кишечника та абеталіпопротеїнемія (Синдром Бассена-Корнцвейга). Клінічно дефіцит вітаміну Е викликає сенсорну периферичну нейропатію, атаксію, пігментний ретиніт, а також скелетну та серцеву міопатію. Невропатологічне обстеження в таких випадках виявляє втрата дорсальних гангліозних нейронів з дегенерацією їх периферичного та центрального аксонів (периферична нейропатія та дегенерація заднього стовпа відповідно). Нейроаксональні набряки спостерігаються в грацильних і клиноподібних ядрах. Подібні зміни можуть відбутися у щурів та мавп з експериментальною депривацією вітаміну Е. Нейродегенеративні ефекти дефіциту вітаміну Е зумовлені втратою антиоксидантної дії альфа-токоферолактивна форма вітаміну Е, і його можна запобігти за допомогою добавок вітаміну Е.
ВІТАМІН В12 ДЕФІЦИТ
Основні дієтичні джерела вітаміну В12 (кобаламін) - це продукти тваринного походження, такі як м’ясна та молочна їжа. У шлунку кобаламін зв’язаний із внутрішнім фактором - глікопротеїном, що виробляється парієтальними клітинами шлунка. Комплекс кобаламіну-внутрішнього фактора транспортується до кінцевої клубової кишки, де він зв’язується з рецепторами на щітковій межі ентероцитів і поглинається. Загальним явищем дефіциту вітаміну В12 є пернициозна анемія, аутоімунний розлад, спричинений антитілами проти парієтальних клітин шлунка та внутрішнім фактором. Дефіцит вітаміну В12 також може бути наслідком гастриту хелікобактер пілорі, хірургічної резекції, пухлин та інших захворювань, що стосуються великих частин шлунка або нижньої частини клубової кишки. Суворі вегетаріанці (вегани), які пропускають з раціону всю їжу тваринного походження, також можуть не мати вітаміну В12. Нестача харчового вітаміну В12 у немовлят, які годують груддю у матерів-веганок, спричиняє дратівливість, млявість, неможливість процвітання, регресію нейророзвитку та мимовільні рухи, що називаються "синдромом дитячого тремору". Лікування вітаміном В12 швидко скасовує ці відхилення.
Нестача вітаміну В12 викликає гематологічні відхилення (мегалобластна анемія) та неврологічні ускладнення (підгостра комбінована дегенерація спинного мозку-SCD). Гематологічні відхилення, ймовірно, зумовлені порушенням синтезу ДНК. Мегалобластну анемію можна виправити, застосовуючи лише фолієву кислоту. Невропатологічні відхилення зумовлені іншим, поки невідомим, біохімічним механізмом. Спадкові метаболічні порушення кобаламінзалежних ферментів не викликають ССД. Вважається, що кобаламін відіграє роль у експресії фактора некрозу пухлини альфа (TNF-a) та епідермального фактора росту (EGF), який є окремим від його каталітичної активності. При дефіциті кобаламіну TNF-a підвищується, а EGF знижується. Цей дисбаланс може спричинити пошкодження білої речовини.
Спочатку СЦД викликає слабкість і парестезії кистей і стоп. У міру прогресування патології вібрація та відчуття положення втрачаються, і хода стає атаксичною. Слабкість погіршується, з’являється спастичність кінцівок. Поглиблений стан характеризується спастичною параплегією, контрактурами, атаксією та порушенням інших сенсорних модальностей.
Найбільш раннім невропатологічним ураженням є розтягнення мієлінових оболонок, надаючи губчастий вигляд ураженій білій речовині. За цим слідує розпад мієліну, який видаляється макрофагами. Loss аксонів також трапляється, але менш серйозно, ніж втрата мієліну. Поразки вражають спочатку задні та бічні (комбіновані) колони верхнього грудного та нижнього шийного відділів спинного мозку. Вони не впливають на анатомічні волокнисті системи, а навпаки, залучають білу речовину симетрично неселективно. У запущених випадках уражається вся окружність спинного мозку. Зорові нерви втягуються рідко. Усі ці зміни можна запобігти (і на ранніх стадіях, змінити) введенням вітаміну В12.
- Факти здоров’я тартару з лососем Страви Інформація про харчування
- Нове дослідження виявляє харчову якість та обмеження пропонованого ящика врожаю Америки - їжа
- Факти океанічного окуня, користь для здоров’я та харчова цінність
- Харчові факти солоної риби здорові
- Факти червоного винного оцту, користь для здоров’я; Харчова цінність