Зменшення кількості циркулюючого SAA корелюється зі зменшенням секреції SAA в животі під час втрати ваги
Ронг-Зе Ян
1 Відділ ендокринології, діабету та харчування, Медичний факультет Університету штату Меріленд
Якоб Б. Блюменталь
2 Відділ геронтології та геріатричної медицини, Медичний факультет Університету Меріленда
3 Служба досліджень VA, Геріатричні дослідження, освітній та клінічний центр, Медичний центр адміністрації ветеранів Балтимора
Ніколь М. Глінн
1 Відділ ендокринології, діабету та харчування, Медичний факультет Університету штату Меріленд
Мі-Чонг Лі
1 Відділ ендокринології, діабету та харчування, Медичний факультет Університету штату Меріленд
Ендрю П. Гольдберг
2 Відділ геронтології та геріатричної медицини, Медичний факультет Університету Меріленда
3 Служба досліджень VA, Геріатричні дослідження, освітній та клінічний центр, Медичний центр адміністрації ветеранів Балтимора
Да-Вей Гун
1 Відділ ендокринології, діабету та харчування, Медичний факультет Університету штату Меріленд
3 Служба досліджень VA, Геріатричні дослідження, освітній та клінічний центр, Медичний центр адміністрації ветеранів Балтимора
Аліса С. Райан
2 Відділ геронтології та геріатричної медицини, Медичний факультет Університету Меріленда
3 Служба досліджень VA, Геріатричні дослідження, освітній та клінічний центр, Медичний центр адміністрації ветеранів Балтимора
Анотація
Об’єктивна
Метою дослідження було визначити вплив втрати ваги (WL) окремо та за допомогою аеробних вправ (WL + AEX) на рівень SAA та жирову секрецію SAA з сідничних та черевних депо.
Дизайн та методи
Дев'яносто шість жінок із надмірною вагою або ожирінням у постменопаузі проходили 6-місячну ВЛ самостійно (n = 47) або з аеробними тренуваннями (n = 49) (6 місяців WL та WL + AEX вважаються ВЛ, коли групи об'єднувались). Їх рівень SAA в сироватці крові, масу тіла та жирову секрецію SAA ex vivo із сідничного та черевного депо вимірювали до та після втручань WL.
Результати
Учасники втратили в середньому 8% маси тіла при 10% зниженні рівня SAA в сироватці крові. Рівень SAA в сироватці крові залишався суттєво корельованим з масою тіла до та після ВЛ. Однак зміни рівня SAA в сироватці крові не корелювали із змінами маси тіла. Виділяється сіднична жирова тканина
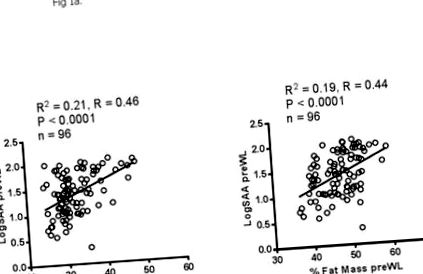
50% більше SAA, ніж черевної тканини, але зміни черевної, але не сідничної, секреції SAA корелювали (R 2 = 0,19, p 25 кг/м 2, діапазон 25–48 кг/м 2] жінки у віці до 49 і 76 років. Жінки перебували в постменопаузі і не мали менструацій протягом ≥1 року. Детальніше про цю програму WL були описані в іншому місці (20). Коротше кажучи, всі жінки в WL і WL + AEX відвідували щотижневі заняття WL під керівництвом Жінкам було наказано зменшити споживання калорій на 300–500 ккал/день. Для втручання WL + AEX жінки здійснювали вправи тричі на тиждень протягом шести місяців, використовуючи бігові доріжки та еліптичні тренажери, як описано (20). двоенергетична рентгенівська абсорбціометрія (Prodigy; Lunar Radiation Corp., Madison, WI). Зразки крові були взяті з антекубітальної вени після 12-годинного голодування протягом ночі, через 36–48 годин після останнього втручання в WL + AEX, і зберігали при -80 ° C до аналізу. Рівні SAA в сироватці крові вимірювали до та після інтерв’ю всіх учасників.
Посів жирової тканини та вимірювання SAA
Деякі з учасників проходили біопсію жирової тканини до та після режиму ЖЛ. Біопсії проводили через 36–48 годин після останнього вправи в групі WL + AEX. Зразки жирової тканини черевної порожнини та сідничної тканини отримували від суб'єктів, які голодували протягом ночі, шляхом аспірації 3-міліметровою канюлею під місцевою анестезією лідокаїном, як описано раніше (21). Фрагменти жирової тканини інкубували протягом 3 годин у M199-1% BSA (
100 мг/мл), а середовище збирали та зберігали при -80 ° C, як описано раніше (22), до аналізу SAA.
Рівні SAA в сироватці крові вимірювали за допомогою набору для імуноферментного аналізу (ELISA) відповідно до інструкцій виробника (BioSource, Камарілло, Каліфорнія, США). Для високочутливого вимірювання рівнів SAA в невеликому обсязі умовних середовищ гострої жирової культури людини застосовували метод мультиплексної електрохімілюмінесценції (МСЛ) Meso Scale Discovery (MSL) (Meso Scale Discovery, Гейтерсбург, США, США). Чутливість виявлення SAA за допомогою ELISA та MSD становила 5 нг/мл та 8 пг/мл, відповідно. Для ІФА коефіцієнти варіації внутрішньо- та міжаналітичного аналізу (CV) становили відповідно 5% та 8%, тоді як для MSD CV внутрішньо-аналітичного аналізу становив 4%. CV між пробами не визначали, оскільки всі зразки аналізували одночасно. Коефіцієнт кореляції між двома аналізами становив 0,87. Всі зразки аналізували в двох примірниках, а середнє значення використовували для аналізу даних.
Статистичний аналіз
10b, рис. 1b) у всій когорті між-індивідуальні зміни рівня SAA в сироватці крові різко коливались, коливаючись від -84 до 248% порівняно з відносно вузькими змінами WL між -2,1 і -24,0%. Не було жодної кореляції між змінами сироваткового SAA та змінами маси тіла, вираженими в абсолютних або відносних показниках відносно або відсотка (рис. 2), або перетвореного в журнал відсотка (не показано) у учасників, об'єднаних або розділених за групою.
Зв'язок між змінами ІМТ та змінами рівня SAA в сироватці крові.
Вплив WL на секрецію SAA
Зниження рівня SAA в сироватці після ШЛ може бути результатом нормальної секреції SAA із зменшення маси жиру та/або зменшення секреції з жирової або інших тканин. Щоб дослідити ці можливості, 42 суб'єктам було проведено біопсію черевної та сідничної жирової тканини до та після ВЛ та вимірювали секрецію жирової SAA ex vivo. Оскільки не було суттєвої різниці у впливі WL проти WL + AEX на жирову секрецію SAA (дані не показані), дані секреції SAA були об’єднані з обох груп для подальшого статистичного аналізу. В результаті (рис. 3) виділяється сіднична жирова тканина
50% більше SAA, ніж черевна (p Рис. 3a). Кількість SAA, що секретується з сідничної області, добре корелювала з кількістю з черевного депо раніше (R = 0,54, p Рис. 3b). Примітно, що спостерігалася більша варіація до 100-кратної різниці в секреції SAA до і після ВЛ. Таким чином, хоча загальна секреція жирової SAA зменшилась на 30% (p = 0,09) та 22% (p = 0,6) відповідно в абдомінальному та сідничному депо після WL, зменшення після WL не досягло статистичної значущості.
Кореляція зміни системного SAA із зміною жирової секреції SAA з черевного, але не сідничного жирового депо під час WL.
Обговорення
19 та 26% системних варіацій SAA у станах до та після WL (рис. 1) та механізми, що не залежать від маси жиру (наприклад, швидкість секреції жирової SAA та нежирової секреції SAA) мають більший ефект для визначення системні рівні SAA.
Оскільки існують регіональні відмінності в експресії та регуляції генів у депо підшкірного жиру (26–28), ми дослідили зміни вивільнення SAA ex vivo жирових зразків з черевної та сідничної областей. Результати показують, що жирова тканина в сідничному депо секретує
На 50% більше SAA, ніж у черевній порожнині, як до, так і після ВЛ. Помітна сильна кореляція між кількістю секреції SAA між двома депо, що свідчить про подібний механізм регулювання виробництва жирової SAA між депо. Примітно, що під час ЛЖ спостерігались великі індивідуальні зміни в секреції SAA, що вказує на те, що швидкість секреції SAA сильно варіюється серед осіб до та після WL. В результаті драматичне
Зменшення секреції SAA на 25% після ВЛ не досягло статистичної значущості.
Це дослідження виявляє помірну кореляцію між зниженням рівня SAA в сироватці крові та рівня секреції SAA у черевній порожнині (R = 0,43, рис. 4), припускаючи, що зменшення секреції SAA в черевній порожнині може сприяти зниженню SAA в циркуляції після ШЛ. Інтригуючим є той факт, що хоча сіднична жирова тканина виділяє більше SAA, ніж жирова тканина живота, лише секреція SAA жирової тканини черевної порожнини суттєво пов’язана з рівнем SAA, що циркулює. Одне з можливих пояснень полягає в тому, що місцевий стан живота сприяє вивільненню SAA на всьому рівні тіла. Це підтверджується висновком, що швидкість кровотоку в черевному депо втричі більша, ніж у сідничному депо (29). Більше того, температура шкіри живота на 1 ° C вища, ніж сіднична (33,3 проти 32,2 ° C), що може посилити вивільнення SAA з черевного депо в кровообіг. Інша можливість - через непрямий механізм, коли жирова тканина черевної порожнини виділяє більше прозапальних жирних кислот системно (29). Місцеве зменшення SAA знизило б ліполіз та вихід жирних кислот та запальних цитокінів у кровообіг, що призвело б до системного зниження запального статусу та вироблення SAA з нежирової тканини, такої як печінка.
У сукупності наші дані ще більше підтверджують той факт, що ІМТ та жирова маса є визначальним фактором системного рівня SAA. Однак системне зниження SAA після ВЛ, здається, не є прямим наслідком зниження ІМТ або маси жиру і може бути пов’язане з іншими хронічними захворюваннями, такими як стрес, гіпертонія та остеоартроз (30–32). Така велика варіація могла б затуманити або придушити внесок зміни маси жиру в системний рівень SAA протягом ВЛ. Причини більшої індивідуальної варіації до і після ВЛ варіації ex vivo секреції SAA з жирової тканини незрозумілі. Можливі пояснення включають, що SAA є високо та швидко регульованим білком; отже, великі варіації SAA у дослідженні гострого експлантату можуть відображати фактичний стан швидкої динаміки виробництва та секреції SAA, а також нещодавно синтезованого SAA під час біопсії жиру. Далі, висновок про те, що у однієї і тієї ж особини сіднична та абдомінальна секреція SAA добре корелюють до і після ШЛ (рис. 3), припускає, що подібні механізми регулювання можуть існувати в двох жирових областях у відповідь на втрату маси тіла.
Підводячи підсумок, ці результати показують, що ІМТ та маса жиру є визначальними для рівня циркулюючого SAA. Загальний ступінь зниження рівня SAA у сироватці крові порівнянний із зниженням ваги при вправі в когорті та без неї, але лише в сукупності зміни рівня SAA безпосередньо пов’язані зі зменшенням жирової маси. Ми також виявляємо, що сіднична жирова тканина виділяє
На 50% SAA більше, ніж жирова тканина живота, і ця секреція жирового SAA має тенденцію до зменшення після втрати ваги; однак лише зменшення секреції SAA в черевній порожнині корелювало із систематичним SAA. Таким чином, як зменшена жирова маса, так і зменшена секреція жирового саа в животі, поряд з іншими, поки невстановленими факторами, сприяють зниженню системних рівнів САА після втрати ваги.
Що вже відомо про цю тему?
SAA є адипокіном і вважається зв'язком між ожирінням та пов'язаними з ним захворюваннями.
- Індивідуальне дієтичне втручання дозволяє уникнути ненавмисної втрати ваги та модулює циркулюючі мікроРНК
- КОНТРОЛЬ ГІПЕРГЛІКЕМІЇ ОЖАРНОЇ ДІАБЕТИКИ ШЛЯХОМ ЗНИЖЕННЯ ВАГИ Аннали внутрішньої медицини
- Вплив помірного зниження ваги, зумовленого дієтою, та відновлення ваги на серцево-судинну структуру та
- Демістифікація дієт для схуднення Екологія продуктів харчування та харчування Том 45, No 5
- Вплив лікування оланзапіном, рисперидоном та галоперидолом на вагу та індекс маси тіла в