Витрати енергії у спокої, споживання калорій та білка у важкохворих: ретроспективне когортне дослідження
- Лист до цієї статті опублікований у Critical Care 2017 21: 39
Анотація
Передумови
Існує напружена дискусія щодо оптимального споживання енергії та білків для пацієнтів відділення інтенсивної терапії. Однак у більшості досліджень використовуються прогнозні рівняння, продемонстровані як неточні щодо цільового споживання енергії. Ми прагнули вивчити результати великої когорти пацієнтів інтенсивної терапії щодо відсотка введених калорій, розділених на витрати енергії в спокої (% AdCal/REE), отриманих непрямою калориметрією (IC), та споживання білка.
Методи
Включені пацієнти були госпіталізовані з 2003 по 2015 рік у відділення інтенсивної терапії на 16 ліжок в університетській лікарні вищої медичної допомоги та проводили вимірювання ІК для оцінки калорійних показників. Дані отримували з комп’ютеризованої системи та включали% AdCal/REE та споживання білка та інші змінні. Була використана модель пропорційної небезпеки Кокса для 60-денної смертності з моделюванням% AdCal/REE для врахування нелінійності. Також оцінювались тривалість перебування (LOS) та тривалість вентиляції (LOV).
Результати
Всього було включено 1171 пацієнт. % AdCal/REE мав значну нелінійну (стор 70% було пов'язано із збільшенням LOS та LOV.
Висновки
Результати цього дослідження свідчать про те, що недоїдання та перегодовування представляються шкідливими для критично хворих, так що досягнення Adcal/РЗЕ 70% мало перевагу у виживанні. Більш калорійне споживання може також бути пов’язане із шкодою у вигляді збільшення LOS та LOV. Тому оптимальний спосіб визначення калорійних цілей вимагає точної оцінки, яка в ідеалі проводиться за допомогою непрямої калориметрії. Ці висновки можуть забезпечити основу для майбутніх рандомізованих контрольованих досліджень, що порівнюють конкретні режими харчування на основі непрямих вимірювань калориметрії.
Передумови
Надання харчової підтримки критично хворим пацієнтам продовжує залишатися предметом напружених дискусій, при цьому головним питанням є оптимальна сума для максимальної користі. У зв’язку з цим результати недавніх досліджень не привели до більшої ясності, оскільки було продемонстровано як користь [1–3], так і шкоду [4, 5], коли споживання калорій збільшується до вимірюваних цілей, тоді як негативні наслідки недоїдання також були описані [6, 7]. Важливо зазначити, що з багатьох причин, як за задумом, так і за замовчуванням, багато важкохворих пацієнтів не отримують у повному обсязі енергетичних потреб, і частка доставлених калорій коливається в широких межах. Будь-який можливий дефіцит споживання калорій додатково ускладнюється використанням прогнозних рівнянь для оцінки калорійних цілей. Відомо, що вони менш точні і надають лише приблизний знімок метаболічних потреб [8], на відміну від фактичного вимірювання витрат енергії у спокої (РЗЕ) за допомогою непрямої калориметрії (ІС), яке також може використовуватися для надання оновленої інформації про зміну енергетичні потреби. Хоча все більше заохочується використання непрямої калориметрії [9–11], технічні та економічні міркування перешкоджають її більш широкому використанню [12].
Метою цього дослідження було оцінити зв'язок між відсотком введених калорій як функцією вимірюваної РЗЕ та результатами, включаючи 60-денну смертність, тривалість перебування в реанімації та дні ШВЛ у великої когорти критично хворих пацієнтів . Крім того, ми оцінили вплив споживання білка на ці самі параметри.
Методи
Усі пацієнти, які потрапили до багатопрофільної багатопрофільної реанімації медичного центру Рабіна, медичної лікарні, що спеціалізується на університетах, з 2003 по 2015 рр., Які проходили вимірювання ІК (Deltatrac II, Datex-Ohmeda, GE, США) та які отримували ентеральне харчування з додатковим або без додаткового парентерального харчування (TPN) було включено в це дослідження.
Калориметр калібрували етанолом щомісяця та для досліджуваних газів (навколишнє повітря та O2 95% та CO2 5%) перед усіма вимірами. Перед тестуванням пацієнти повинні були знаходитись у стабільному стані принаймні 30 хвилин, провітрюватися фракцією вдиху кисню (FiO2) 96 годин або оцінювати дні харчування, щоб зменшити будь-яке можливе упередження, спричинене короткочасним перебуванням, ранньою смертністю або очікування того, що ефект харчування може зажадати хоча б такої тривалості впливу [2]. Підрахунок тривалості перебування та оцінюваних днів харчування починався з години прибуття в реанімацію.
Зібрані демографічні дані включали вік, стать, зріст і вагу, оцінку гострої фізіології та хронічного здоров’я (APACHE) II, оцінку послідовної оцінки відмови органів (SOFA), категорію прийому (медичну, хірургічну чи травматичну) та діагноз прийому (не взаємовиключні серцево-судинні, респіраторний, сепсис).
Зазначені харчові параметри включали шлях годування (ентеральний та/або парентеральний), повторне вимірювання РЗЕ та інсулінотерапію (одиниць/день) та кількість загальних калорій та білка, що вводяться щодня до смерті ІРТ, виписки з інтенсивної терапії або початку ексклюзивного перорального прийому годування. Непоживні калорії, що вводяться у вигляді інфузій глюкози та пропофолу, були включені в якості введених калорій. Споживання білка оцінювали як грами на день та як відсоток потреби, з метою 1,3 г/кг. Практика нашої одиниці полягає в тому, щоб споживати калорії як 100% РЗЕ. Введення додаткового парентерального харчування для пацієнтів, які не досягають цілей, вирішує лікуючий лікар. Оцінені шлунково-кишкові параметри включали наявність шлункового залишку> 150 мл, аспірованого через назогастральний зонд, діарею, що визначається як мінімум три рідкі випорожнення на день, запор, що визначається як ≥3 дні без руху кишечника та блювоти. Реадмісії до реанімації відкидали.
Відсоток щоденних введених калорій, поділений на РЗЕ (% AdCal/РЗЕ) та середнє значення госпіталізації в реанімацію розраховували для кожного пацієнта та оцінювали його зв'язок із 60-денною смертністю. Для того, щоб пом'якшити можливий вплив тривалості впливу дієти на результати, ми заздалегідь запланували аналізи чутливості, які включали лише вимірювання з 3-го дня і далі, коригуючи загальний обсяг оцінюваних днів харчування та аналізуючи пацієнтів, які вижили> 7 днів. Оскільки дата смерті в наших комп’ютерних записах оновлюється Міністерством охорони здоров’я, ми змогли зафіксувати смерть як у лікарні, так і після виписки. Крім того, ми оцінили зв'язок між% AdCal/REE та тривалістю перебування (LOS) та тривалістю вентиляції (LOV). LOS визначався фізичним виписуванням з відділення інтенсивної терапії, незалежно від медичного стану. Дослідження було схвалено комісією з огляду інституційного медичного центру Рабіна, яка відмовилася від вимоги про надання згоди.
Статистичний аналіз
Неперервні нормально розподілені змінні представлені як середні значення ± стандартні відхилення (SD) та порівнюються за допомогою Стьюдента т тест. Порядкові та/або ненормально розподілені змінні представлені у вигляді середнього та міжквартильного діапазону (IQR) та порівнюються за допомогою критерію суми рангу Вількоксона. Нормальність оцінювали за допомогою критерію Шапіро-Вілька. Категоричні змінні порівнювали за допомогою критерію хі-квадрат. Аналіз дисперсії (ANOVA) для повторних вимірювань використовувався для порівняння повторних записів загальної кількості калорій або РЗЕ, після перевірки того, що дані відповідають припущенням моделі.
Спочатку застосовували некореговану модель пропорційних ризиків Кокса для 60-денного виживання, відсоток AdCal/REE вводили як безперервну змінну. Оскільки ефект AdCal/REE вважався нелінійним (з можливими несприятливими наслідками через недоїдання або перегодовування в певний момент), відсоток моделювали як обмежений кубічний сплайн із заздалегідь заданими вузлами [14]. Нелінійність була перевірена ANOVA. Потім була встановлена скоригована модель із коваріантами, відібраними на основі однофакторного аналізу, з коваріантним відбором шляхом завантаження. Мультиколінеарність оцінювали за варіацією факторів інфляції та Р. 2. Перевірка моделі була виконана шляхом завантаження. Для аналізу чутливості модель була повторно проведена з оцінюваними днями харчування як коваріати, із вирахуваним відсотком, опускаючи перші 2 дні та останні, обмежуючи вибірку пацієнтам з LOS> 7 днів. Ми використали тест Крускала-Уолліса для порівняння LOV та LOS. A стор значення
Результати
Загалом 6994 пацієнти були госпіталізовані до реанімаційного відділення за період дослідження; 6536 із цих пацієнтів отримали унікальний прийом. З них 5053 пацієнти отримували ентеральне та/або парентеральне харчування. Середній вік їх становив 58 (IQR 34) років, а 57% були чоловіками. Медіана LOS становила 5 (IQR 10) днів, а LOS для тих, хто залишався в реанімації протягом> 96 годин (3019 пацієнтів), становив 11 (IQR 13) днів. 60-денна смертність у цій групі становила 32%.
З 5053 пацієнтів 1375 мали вимірювання IC, що дало 5012 вимірювань. Було 6 пацієнтів з неповними вихідними даними та 204 з короткою тривалістю перебування в реанімації або оцінюваних днів харчування, так що до остаточного аналізу було включено 1171 пацієнта. Три та більше вимірювань РЗЕ були проведені у 559 пацієнтів (48%). Вихідні демографічні дані для досліджуваної групи (1171 пацієнт), тих, хто вижив (846 пацієнтів) та неживих (325 пацієнтів) наведені в таблиці 1.
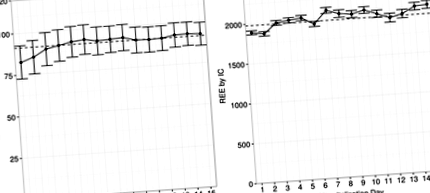
% AdCal/REE становив 89% (± 30%) для досліджуваної групи, 89% (± 28%) у пацієнтів, які вижили, та 91% (± 34%) у пацієнтів, які померли протягом 60 днів (стор = 0,11). Середнє значення РЗЕ та% AdCal/РЗЕ за днем госпіталізації показано на рис. 1. Різниця між днями була значною (стор Рис. 1
Щоденне середнє введення калорій/витрата енергії в спокої (Adcal/REE) відсотків за допомогою непрямої калориметрії (IC)
Коли% AdCal/REE досліджували як безперервну змінну щодо 60-денної смертності, було продемонстровано суттєво нелінійний характер (стор = 0,0078), що призвело до U-подібної кривої (рис. 2), що суттєво пов'язане зі смертністю (стор = 0,008). Найнижча смертність була відзначена при 70% AdCal/REE (мінімальна точка П-подібної кривої). Збільшення відсотка AdCal/РЗЕ з 0% до 70% було пов'язано зі зменшенням смертності (коефіцієнт ризику (HR) 0,98, 95% ДІ 0,97-0,99), тоді як відношення AdCal/РЗЕ ≥70% було пов'язано зі збільшенням смертності (HR 1,01, 95% ДІ 1,01–1,02)). AdCal/REE> 100% був пов'язаний з HR> 1. Після поправки на інші змінні (показано в таблиці 2)% AdCal/РЗЕ все ще суттєво асоціювався із 60-денною смертністю (р = 0,006).
Асоціація відсотків витрачених калорій/витрат енергії у спокої (Adcal/REE) у відсотках із 60-денною смертністю (зліва), а також споживання білка за добовою потребою (1,3 г/кг/добу) при 60-денній смертності (правильно) за співвідношенням шансів. РЗЕ споживання енергії в стані спокою
Зв'язок споживання білка, як відсоток потреби, із смертністю до 60 днів також був значним (HR 0,99, 95% ДІ 0,98-0,99, стор = 0,018). Крива виживання на основі остаточної моделі із конкретними значеннями AdCal/REE представлена на рис. 3. Заміна AdCal/REE загальною добовою калорією або лише РЗЕ не суттєво асоціювалась зі смертністю. Площа під кривою (AUC) для моделі становила 0,75. Після процесу валідації виправлена AUC становила 0,74, що свідчить про стабільну та внутрішньо дійсну модель.
Зв'язок між введеними калоріями/витратою енергії у спокої (Adcal/REE) та 60-денним виживанням. Етикетки відповідають відсоткам Adcal/REE
Аналіз чутливості з урахуванням лише вимірювань після другої доби та додавання оцінюваних днів харчування як провісник не змінює показник HR, а AdCal/REE залишається значним (стор = 0,0031), як і щоденний прийом білка (стор = 0,01). Подальше обмеження вибірки для пацієнтів, які мали> 10 оцінюваних днів харчування (757 пацієнтів), і які все ще контролювали оцінювані дні харчування, дало схожі результати.
Тривалість перебування та тривалість вентиляції
Для оцінки ефекту на LOS та LOV при однофакторному аналізі було визначено три групи на основі AdCal/REE, а саме 100% (n = 671). Медіана LOS у вижилих пацієнтів становила 12, 15 та 16,5 днів для трьох груп відповідно (стор
Обговорення
У цьому ретроспективному спостережному дослідженні, яке, наскільки нам відомо, найбільша когорта, що вивчалася за допомогою непрямої калориметрії, на відміну від прогнозних рівнянь для визначення енергетичних потреб у механічно провітрюваних, критично хворих пацієнтів, ми продемонстрували нелінійну, значну зв'язок між відсотком AdCal/РЗЕ та смертність до 60 днів. Результати дозволяють припустити, що збільшення AdCal/РЗЕ до 70% було пов'язане зі зниженням смертності, тоді як збільшення вище цієї точки, особливо, коли крива зросла> 100%, було пов'язане зі збільшенням смертності. Крім того, прийом білка було незалежно та суттєво пов’язано зі зниженням смертності. Однак досягнення цільових показників калорійності було пов'язано з більш тривалим перебуванням у реанімації та тривалістю вентиляції.
Невизначеність щодо оптимальних цілей харчової підтримки продовжується, що підкріплюється суперечливими результатами в останній літературі. Таким чином, очевидна відсутність користі при підвищеному споживанні калорій була продемонстрована Arabi та співавт. [4], який порівнював дозвільне недоїдання зі стандартним годуванням (835 ± 297 проти 1299 ± 467 ккал/добу відповідно) у пацієнтів, які отримували однакову кількість білка, та Райс та ін. у двох дослідженнях, що порівнювали трофічну із стандартною терапією (300 ± 149 проти 1418 ± 686 та 425 ± 141 проти 1385 ± 46 ккал/добу відповідно) [5, 19]. З іншого боку, позитивний зв’язок між досягненням калорійних цілей та результатом був продемонстрований в спостережних дослідженнях [2, 3] та в РКД нашою групою у дослідженні TICACOS [1] та іншими, які застосовували непряму калориметрію [20, 21]. Як пропонують Heyland та ін., Ця невідповідність може бути пояснена принаймні частково статистичними методами, використаними в дослідженнях, що свідчать про очевидну відсутність ефекту, зокрема методом, що враховує тривалість впливу на харчування або тривалість перебування. У зв'язку з цим у нашому дослідженні ми продемонстрували зв'язок між досягненням 70% AdCal/РЗЕ та поліпшенням виживання, яке залишалося незмінним, навіть коли лише вимірювання після другого дня та додавання оцінюваних днів харчування в якості предиктора розглядалися.
На відміну від багатьох попередніх досліджень, які використовували довільне, заздалегідь визначене обмеження споживання калорій для визначення оптимального харчування, в основному на основі прогнозних рівнянь, ми розглядали AdCal/REE як безперервну змінну, яка дозволила нам оцінити взаємозв'язок між введеними калоріями та смертністю в різні рівні споживання. Отримана U-подібна крива виявила зниження смертності, оскільки споживання калорій було збільшено до 70% від цільових калорій, але це супроводжувалось збільшенням смертності, особливо, коли крива збільшувалася> 100%.
Наше дослідження також підтверджує все більшу важливість білка в поліпшенні виживання, оскільки споживання білка лінійно асоціювалося зі зниженням смертності в мультиваріантній моделі (HR 0,99, 95% ДІ 0,98–0,99, стор = 0,018), що передбачає зниження смертності на 1% за кожен грам щоденно введеного білка. Ці результати повторюють інші спостережні дослідження [22, 23], що підкреслюють важливість споживання білка. Крім того, варто зазначити, що навіть при використанні додаткового парентерального харчування реалії реанімації ускладнюють досягнення 100% калорій та білків.
Нарешті, цікаво відзначити зниження РЗЕ у пацієнтів, які померли, що, як припускають, є результатом поліорганної дисфункції при сепсисі, що призводить до зупинки метаболізму [24]. Це питання потребує подальшого з’ясування. Знову ж таки, це наголошує на важливості вимірювань РЗЕ на основі ІС, оскільки метаболічні потреби можуть переходити через перебіг критичної хвороби.
Наше дослідження має кілька обмежень. За самою природою спостережної схеми включення пацієнтів з непрямою калориметрією та нерандомізоване введення калорій може внести упередження щодо відбору. Оскільки в цих конструкціях, особливо в дослідженнях з оцінки харчування, результати слід інтерпретувати з обережністю, оскільки існує ризик того, що саме випадкове розподіл може вплинути на результати, тобто добре нагодовані пацієнти мають кращий прогноз незалежно від потреб у калоріях або високий рівні споживання калорій попередньо відбирають пацієнтів, які виживають довше. До того ж, хоча ми намагались пояснити плутанину, ми не можемо виключити додаткових, поки що невідомих.
«Наше» - це одноцентрове дослідження, в якому описується унікальна важкохвора популяція та специфічна для центру практика, яка може обмежити зовнішню валідність. Крім того, відмінності можуть не проявитися протягом короткого терміну перебування. Ми спробували усунути ці обмеження при розробці нашого дослідження, як описано в "Методи". Таким чином, щодо відбору та часового зсуву, ми обмежили обсяг вибірки, виключили пацієнтів з короткочасним перебуванням та використали кілька аналізів чутливості, які показали стабільність результатів. Той факт, що відсотки РЗЕ та AdCal/РЗЕ були відносно стабільними у часі> 48 годин госпіталізації, ще більше підтверджує відсутність часового зсуву. Крім того, наші результати показують, що пацієнти з «незначною недостатністю», тобто ті, хто отримує 70% цільових калорій, пройшли краще, ніж пацієнти з оптимальним харчуванням (ті, хто отримує 100% цільових калорій), що аргументує проти уявлення про те, що пацієнти з ситим харчуванням можуть мати кращий прогноз незалежно від потреб у харчуванні. Крім того, ми намагалися врахувати незручності, включаючи тяжкість захворювання.
Висновки
Результати цього дослідження свідчать про те, що недоїдання та перегодовування представляються шкідливими для пацієнтів з критичною хворобою з механічною вентиляцією. Хоча енергетична ціль на 100% від оцінених потреб залишається ідеальною метою, реальність реанімації неминуче виключає цей ідеал. У цьому відношенні ми показали, що досягнення Adcal/РЗЕ щонайменше 70% мало перевагу у виживанні, тоді як більш високе споживання калорій, особливо> 100%, може бути пов'язане із шкодою. Тому оптимальний спосіб визначення калорійних цілей вимагає точної оцінки, яка в ідеалі проводиться за допомогою непрямої калориметрії. Ці висновки дають основу для майбутніх рандомізованих контрольованих досліджень, що порівнюють конкретні режими харчування на основі непрямих вимірювань калориметрії.
Скорочення
введені калорії/витрата енергії в спокої
дисперсійний аналіз
оцінка гострої фізіології та хронічного стану здоров'я
- NBME 23 Споживання калорій, що перевищує витрати енергії (відповіді NBME)
- Відпочинок витрат енергії - огляд тем ScienceDirect
- Швидкість метаболізму в стані спокою; Витрати енергії - освіта Драммонда
- Відпочинок витрат енергії; На вашому харчуванні
- Протеїн2о Енергія, вода з низьким вмістом калорій, залита білком, 15 г ізоляту сироваткового білка, чорниця малина