Жовчний камінь
Камені в жовчному міхурі найчастіше складаються з суміші холестерину, різних солей кальцію, фосфоліпідів та жовчних пігментів.
Пов’язані терміни:
- Панкреатит
- Білірубін
- Жовч
- Холецистит
- Загальний жовчний проток
- Гострий панкреатит
- Октреотид
- Протока підшлункової залози
- Цироз
- Гіпертонія
Завантажити у форматі PDF
Про цю сторінку
ЖОВЧНИЙ МІХУР
Вік, стать та сімейна історія
Хоча жовчнокам’яну хворобу можна виявити у будь-якої статі та в будь-якому віці, поширеність у жінок вдвічі частіше, ніж у чоловіків, і зростає з віком у обох статей. У жінок, які ніколи не мали дітей, рідше розвиваються камені, ніж у жінок, які родили багато жінок. На пізніх термінах вагітності жовчний міхур не спорожняється повністю, залишаючи залишкову жовч для сприяння утворенню каменів. Естрогени зменшують секрецію жовчних кислот, знову стимулюючи утворення каменів, і спостерігається більша частота їх утворення у жінок, які приймають оральні контрацептиви. Ризик розвитку жовчнокам’яної хвороби більший у родичів хворих на жовчнокам’яну хворобу, ніж у сім’ях, у яких анамнезу не було.
Жовчний міхур, дитячий
Камені в жовчному міхурі
Камені в жовчному міхурі у дітей можуть утворюватися внутрішньоутробно і діагностуватися у плода за допомогою пренатальних ультразвукових досліджень, а також можуть бути виявлені за допомогою УЗД черевної порожнини у безсимптомних немовлят або дітей. Незрозуміло, які фактори сприяють утворенню жовчнокам’яної хвороби або яка частота або поширеність у дітей. У дітей молодшого віку генетична схильність, ймовірно, є важливим фактором їх формування.
Недавня робота Пейгена та його колег на моделях мишей припустила, що гени, які можуть сприяти утворенню цих каменів у жовчному міхурі, поділяються на кілька загальних категорій. Запропоновані процеси включають швидкість секреції холестерину, підвищену доставку холестерину до печінки, підвищення регуляції синтезу холестерину, розвиток діабету та ожиріння типу 2, гіперсекрецію холестерину в жовчі, пригнічення синтезу жовчної солі та зв'язування біліарного холестерину з інші жовчні ліпіди. Подальша робота як на моделях мишей, так і на популяціях людей з високим ризиком повинна допомогти з'ясувати, як різні генетичні мутації або поліморфізми впливають на процес утворення жовчнокам'яної хвороби (холестеринові камені).
У дітей більшість каменів у жовчному міхурі - це або пігментні камені, або холестеринові камені. Пігментні камені віднесені до категорії коричневих або чорних. Чорні пігментні камені в основному виготовляються з карбонату кальцію та фосфату, тоді як в коричневих камінцях міститься велика кількість кальцієвого мила (солей жирних кислот). В обох основний каркас складається з глікопротеїдів муцину, що виділяються жовчним епітелієм. Бурі пігментні камені утворюються при наявності як стазу, так і інфекції. Чорні пігментні камені утворюються найчастіше за наявності хронічної гемолітичної хвороби (наприклад, спадковий сфероцитоз, серповидноклітинна анемія або дефіцит глюкозо-6-фосфатдегідрогенази), під час голодування під час загального парентерального харчування, а також через цироз або хронічний холестаз [в т.ч. такі захворювання, як хвороба Вільсона та прогресуючий сімейний внутрішньопечінковий холестаз 1 типу (хвороба Байлера)]. Застосування деяких препаратів, таких як цефтріаксон, спричинює розвиток осаду (так званий псевдолітіаз), а також може сприяти утворенню каменів.
Існують деякі відмінності в етіології в різному віці. Камені в жовчному міхурі у немовлят спостерігаються у поєднанні із загальним парентеральним харчуванням, сепсисом, хронічними захворюваннями легенів, гемолітичною анемією, порушенням всмоктування, абдомінальними операціями, гепатобіліарними проблемами та некротизуючим ентероколітом. Однак при багатьох із цих розладів діти будуть отримувати внутрішньовенне харчування або будуть дуже обмежені в пероральному прийомі, що саме по собі може бути основним фактором утворення каменів. У дітей старшого віку та підлітків спостерігається посилений зв’язок як із ожирінням, так і з вагітністю.
Хоча підраховано, що до 80% каменів у жовчному міхурі у дорослих мовчать, вони можуть спричинити значні клінічні симптоми. Найбільш послідовні симптоми стосуються закупорки кістозної або жовчовивідних шляхів. Невідомо, скільки дітей без симптомів насправді мають жовчнокам’яну хворобу, а також те, чи у тих, хто має „мовчазні” жовчнокам’яні захворювання, коли-небудь з’являються симптоми протягом життя. Ті, у кого розвивається симптоматичний жовчнокам’яна хвороба, описувались у будь-якому віці в дитинстві. Частота симптоматичних пацієнтів у будь-якому віці, як видається, пов'язана з ризиком розвитку каменів у жовчному міхурі. Для всіх симптоматичних випадків жовчнокам’яної хвороби холецистектомія є вибором лікування. При безсимптомних каменях у жовчному міхурі більшість клініцистів не рекомендують лікування, якщо не з’являються симптоми.
Харчування, харчові волокна та жовчнокам’яна хвороба
6.3 Фізіохімічні основи жовчнокам’яної хвороби
Камені в жовчному міхурі, головним чином утворення холестеринових каменів, є результатом ряду фізіологічних подій, таких як печінкова секреція жовчі, насиченої холестерином, зародження кристалів моногідрату холестерину в жовчному міхурі та порушення спорожнення вмісту жовчного міхура. Насичення жовчі та зародження показують наслідки жовчнокам’яної хвороби холестерином.
Жовч - водний розчин, збагачений нерозчинними у воді гідрофобними ліпідами, такими як холестерин та фосфоліпіди, в іншому випадку суспендований у миючих жовчних кислотах. Такі розчинені тверді речовини становлять близько 3% від маси печінкової жовчі. Жовчі солі є видатною розчиненою речовиною, у середньому в печінковій жовчі 20–30 ммоль l -1. Концентрація фосфоліпідів у середньому становить 7 ммоль л -1, а холестерину в середньому 2-3 ммоль л -1 у розчинній формі. Білірубін присутній у концентраціях приблизно 0,2% по масі. Частина цих білків відіграє важливу роль у зародженні кристалів холестерину та утворенні жовчнокам’яної хвороби.
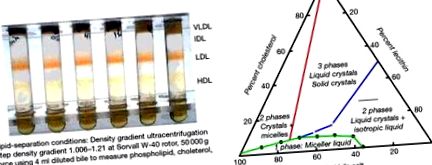
Основні ліпідні компоненти (фосфоліпіди та холестерин) розчиняються міцелами жовчної солі. Жовчні солі є надзвичайно ефективними солюбілізаторами фосфоліпідів. Крім того, наявність фосфоліпідів помітно збільшує ступінь, до якої солі жовчі можуть включати холестерин в міцели. Відносні кількості холестерину, фосфоліпідів та жовчної солі, які можуть співіснувати в міцелярному розчині, були емпірично визначені Кері та Смолл (Carey and Small, 1978), як показано на малюнку 9.3. У наступному описі гомеостаз жовчі на рівні гена описаний для зацікавлених читачів.
Малюнок 9.3. Ліворуч (а) Аналіз ліпідів жовчних для оцінки складу жовчі; Вправо: (b) Трикоординатна фазова діаграма, що показує точку перетину відносних концентрацій холестерину, фосфоліпідів та солей жовчі в жовчі згідно з Carey and Small (1978). Зверніть увагу на лівий нижній кінець міцели. Жовч, пересичений холестерином, випадає в осад з розчину.
На генетичному рівні як жовчні кислоти CDCA, так і холева кислота (СА) можуть регулювати експресію генів, що беруть участь у їх синтезі, створюючи петлю зворотного зв'язку. З'ясування цього регуляторного шляху виникло як наслідок виділення класу рецепторів, званих рецепторами фарнезоїдних Х (FXR). FXR належать до суперсімейства ядерних рецепторів, що включає сімейство рецепторів стероїдів/гормонів щитовидної залози, а також рецептори печінки X (LXR), рецептори X ретиноїдів (RXR) та активовані проліфератором пероксисом рецептори (PPAR).
Існує два гени, що кодують FXR, ідентифіковані як FXRα та FXRβ. У людини було виявлено, щонайменше чотири ізоформи FXR отримані з гена FXRα в результаті активації від різних промоторів та використання альтернативного сплайсингу: FXRα1, FXRα2, FXRα3 та FXRα4. Ген FXR також відомий як ген NR1H4 (для підсімейства ядерних рецепторів 1, група H, член 4). Гени FXR експресуються на найвищому рівні в кишечнику та печінці.
Подібно до всіх рецепторів цієї надродини, ліганд пов'язує рецептор у цитоплазмі, а потім комплекс мігрує до ядра і утворює гетеродимер з іншими членами сімейства. FXR утворює гетеродимер з членами сімейства RXR. Після утворення гетеродимерів, комплекс зв'язується зі специфічними послідовностями в генах-мішенях, званих елементами відповіді FXR (FXRE), що призводить до регульованої експресії. Однією з основних цілей FXR є ген малого гетеродимерного партнера (SHP). Активація експресії SHP за допомогою FXR призводить до інгібування транскрипції генів-мішеней SHP. Значуще для синтезу жовчних кислот, SHP пригнічує експресію гена холестерину-7α-гідроксилази (CYP7A1). CYP7A1 є обмежуючим швидкість ферментом у синтезі жовчних кислот з холестерину за класичним шляхом.
У аюрведичній традиції медицини будь-яка смола, зібрана постукуванням по стовбуру дерева, називається гуггул. Знижуюча холестерин дію гуггула з дерева мури Мири (Commiphora mukul) в Індії полягає в тому, що ліпідний компонент цього екстракту, який називається гуггульстерон (також званий гуггуль ліпід), є антагоністом FXR. Однак, окрім впливу на функцію FXR, було показано, що гуггульстерон активує рецептор прегнану X (PXR), який є ще одним членом надсімейства ядерних рецепторів. PXR є визнаним рецептором літохолевої кислоти та інших попередників жовчних кислот. Активація PXR призводить до репресії синтезу жовчних кислот через його фізичну асоціацію з ядерним фактором гепатоцитів 4α (HNF-4α), внаслідок чого цей фактор транскрипції більше не може асоціюватися з транскрипційним коактиватором PGC-1α (коактиватором PPARγ 1α), що в кінцевому підсумку призводить до до втрати активації фактора транскрипції CYP7A1.
Як і при жовчнокам’яній хворобі, як тільки концентрації холестерину перевищують свою максимальну рівноважну розчинність, багатошарові пухирці холестерину зливаються і агрегуються в скупчення, яке служить осередком для утворення кристалів (зародження). Зародження може бути як однорідним, так і неоднорідним. Однорідне зародження відбувається, якщо кристалізація відбувається без стороннього матеріалу. Неоднорідне зародження відбувається без стороннього матеріалу. Неоднорідне зародження відбувається, якщо кристалізація відбувається на чужорідній поверхні, такі як епітеліальні клітини, білок, солі кальцію або чужорідне тіло. Оскільки зародження відбувається швидко при низьких рівнях перенасичення холестерином, воно відбувається гетерогенним шляхом.
Останнім часом промотори та інгібітори утворення та росту кристалів холестерину впливають на в'язкість людської жовчі. Ці стимулюючі та інгібуючі фактори можуть безпосередньо впливати на "час зародження" жовчі. Біліарні білки з молекулярною масою 130 кДа були запропоновані як потенційні пронуклеатори. На відміну від них, у нормальній жовчі є білки, які пригнічують зародження. Ці антинуклеаторні фактори можуть стабілізувати холестерино-фосфоліпідні пухирці в «нормальній» жовчі та уповільнювати кристалізацію. Потенційні кандидати антинуклеативних білків включають аполіпопротеїни A-I та A-II (Gudheti et al., 2005).
Сучасні концепції щодо утворення жовчнокам’яної хвороби посилаються на думку, що зародження кристалів холестерину відбувається в слизовому гелі через взаємодію білків і ліпідів. На швидкість зародження кристалів холестерину може впливати баланс між про- та антинуклеаторними факторами. У жовчному міхурі муцин також може сприяти утворенню каменів. Муцин викликає прискорення кристалізації холестерину від часу та концентрації. Кувер та ін. (2004) продемонстрували, що гіперсекреція слизу відбувається до утворення жовчнокам'яної хвороби у тварин, які харчуються дієтою, що стимулює жовчний камінь. Однак інгібування секреції слизу за допомогою гіпохолестемічних східних принципів може запобігти утворенню жовчнокам'яної хвороби, але не змінює розвиток перенасичення холестерину жовчі, викликаного дієтою.
Застій жовчного міхура сприяє зростанню мікроскопічних кристалів у макроскопічні камені. Дослідження на тваринах показують, що дефект моторики жовчного міхура може спричинити утворення жовчнокам’яної хвороби (Wang et al., 2009). Крім того, рухливість жовчного міхура погіршується в міру розвитку каменів. Біліарний застій ускладнює лікування жовчнокам'яної хвороби загальним парентеральним харчуванням та пероральними контрацептивами та вагітністю (Honoré, 1980).
Насичення жовчі холестерином може бути наслідком дефіциту секретованих жовчних солей або фосфоліпідів або непропорційно підвищеної секреції холестерину. Камені холестерину характерно частіше зустрічаються у жінок після статевого дозрівання. Однак відмінності в поширеності жовчнокам'яної хвороби між статями зменшуються після менопаузи. Вагітність, пов'язана з насиченням жовчного холестерину, естрогенами, контрацептивами та спорожненням жовчного міхура, сприяють збільшенню частоти каменів у жінок дітородного віку (Karayalçin et al., 2010).
Наявна обмежена інформація щодо складу ліпідів у жовчі та насиченості холестерином у нормальних немовлят та дітей (Davit-Spraul et al., 2010; Koivusalo et al., 2010). Жовч є відносно ненасиченою холестерином у немовлят та дітей у порівнянні з дорослими. Цей факт можна пояснити спостереженням, що басейни жовчної солі швидко розростаються після народження, а басейни, що відповідають розміру тіла, в дитячому та дитячому віці перевищують такі, що спостерігаються у молодих людей, внаслідок високого коефіцієнта секреції жовчо-сольової солі-холестерину з менш насиченою жовчю (Sichieri та ін., 1991).
Однак популяції з низьким ризиком холестеринового жовчнокам'яної хвороби та ожиріння не виявляють насичення жовчним холестерином серед чоловіків у період статевого дозрівання, тоді як у жінок до статевого дозрівання спостерігається ненасичена жовч, а після статевого дозрівання у тих самих жінок спостерігається перенасичена жовч (Sichieri et al., 1991). Посилена секреція та насичення холестерину може спостерігатися при ряді інших пов’язаних станів ожиріння, резекції клубової кишки, шлунково-кишкового шунтування, хвороби Крона, муковісцидозу та вагітності.
- Синдром тріщин зуба - огляд тем ScienceDirect
- Діоген - огляд тем ScienceDirect
- Фронтотемпоральна деменція - огляд тем ScienceDirect
- Дистальна панкреатектомія - огляд тем ScienceDirect
- Щур, чутливий до солі Даля - огляд тем ScienceDirect