JOP. Журнал підшлункової залози
Таліс Хрістофідес 1, Адам Е Фрамптон 1, Патріція Коен 2, Тамара М.Х. Галл 1, Лонг Р Цзяо 1, Надь А Хабіб 1, Мадхава Пай 1
1 хірургічне відділення HPB, відділення хірургії та раку та 2 відділення гістопатології; Імперський коледж охорони здоров’я NHS Trust, кампус лікарні Хаммерсміт. Лондон, Об'єднане Королівство
* Автор-кореспондент: Мадхава Пай
Хірургічний блок HPB
Кафедра хірургії та раку
Імперський коледж, кампус лікарні Хаммерсміт
Du Cane Road; Лондон, W12 0HS; Об'єднане Королівство
Телефон: +44-208.383.3937
Факс: +44-208.383.3212
Електронна пошта: [електронна пошта захищена]
Отримано 17 грудня 2012 р. - Прийнято 27 грудня 2012 р
Анотація
Контекст Локалізована реактивна лімфоїдна гіперплазія - рідкісний стан, що характеризується наявністю лімфоїдних фолікулів. Звіт про справу Ми описуємо випадок із 60-річною жінкою, у якої спостерігався біль у правому верхньому квадранті, і було виявлено реактивну вузлувату гіперплазію підшлункової залози із залученням нецинованого відростка, тіла та хвоста залози. Через мультифокальний розподіл цих гіпоехогенних судинних уражень проведено тотальну панкреатектомію, оскільки злоякісне утворення не можна безпечно виключити. Висновок Було кілька випадків, коли повідомлялося про реактивну лімфоїдну гіперплазію, що вражає підшлункову залозу; однак рідко проводять таку радикальну резекцію підшлункової залози при цьому доброякісному стані.
Ключові слова
Псевдолімфома; Підшлункова залоза; Панкреатектомія
Скорочення
СОЛОД: асоційована зі слизовою лімфоїдна тканина
ВСТУП
Вузлова лімфоїдна гіперплазія підшлункової залози - рідкість. В англійській літературі дуже мало звітів, що описують подібні випадки [1, 2, 3, 4, 5, 6]. Локалізована лімфоїдна гіперплазія, яку раніше називали «псевдолімфома», характеризується наявністю лімфоїдних фолікулів, які більше нагадують реактивний процес, не маючи жодного злоякісного потенціалу. Це було виявлено в різних органах, включаючи шлунок [7], шкіру [8], молочну залозу [9], легені [10, 11], печінку [12] та орбіту [13]. До 5% панкреатектомій, проведених з передопераційним клінічним діагнозом карциноми, виявиться непухлинним при патологічному обстеженні [14]. Рентгенологічні дані при гіперплазії підшлункової залози недостатньо відомі; тому важко відрізнити цей доброякісний процес від інших новоутворень підшлункової залози. Тут ми обговорюємо випадок, що представляє собою мультифокальні гіперсудинні ураження, підозрілі на нейроендокринну пухлину.
ЗВІТ ПРО СПРАВУ
Звіт пацієнта
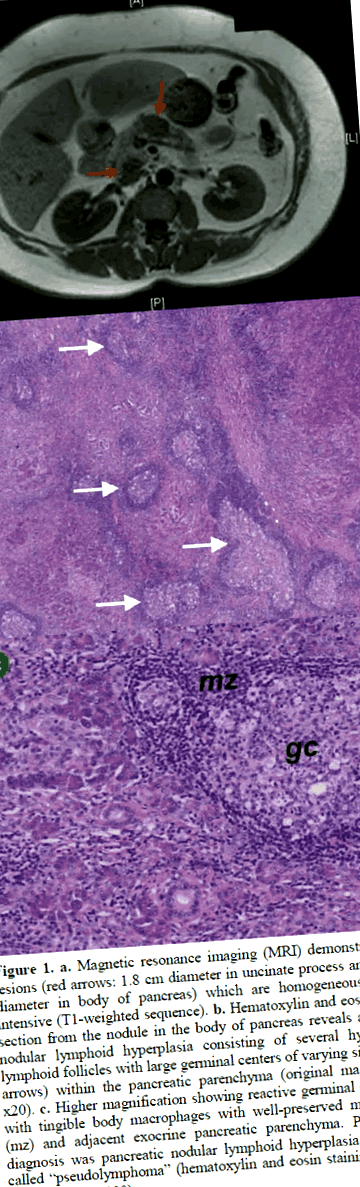
Фігура 1. a. Магнітно-резонансна томографія (МРТ) демонструє два ураження (червоні стрілки: діаметр 1,8 см у нецинованому відростку та 2,3 см у тілі підшлункової залози), які є однорідно гіпоінтенсивними (Т1-зважена послідовність). b. Пофарбований гематоксиліном та еозином зріз вузлика в тілі підшлункової залози виявляє ділянку вузлуватої лімфоїдної гіперплазії, що складається з декількох гіперпластичних лімфоїдних фолікулів з великими зародковими центрами різного розміру (білі стрілки) всередині паренхіми підшлункової залози (початкове збільшення x20). c. Більше збільшення показує реактивний зародковий центр (gc) з макрофагами тілесного тіла з добре збереженою мантійною зоною (mz) та сусідньою екзокринною паренхімою підшлункової залози. Патологічним діагнозом була вузликова лімфоїдна гіперплазія підшлункової залози, яку раніше називали «псевдолімфомою» (фарбування гематоксиліном та еозином; оригінальне збільшення x100).
Гістопатологічні висновки
Малюнок 2. Імуногістохімічне фарбування виявило фолікулярний інфільтрат, який складався з центрів з клітинами, що виражали B-клітинні характеристики, які були CD10 позитивними (a.) і BCL-2 негативний (b.) (Негативність BCL-2 передбачає реактивні, а не новоутворені фолікули), тоді як CD21 (c.) та CD23 (d.) фарбування продемонструвало регулярну та впорядковану мережу фолікулярних дендритних клітин як у реактивних лімфоїдних фолікулах, тим самим підтримуючи діагностику реактивної лімфоїдної фолікулярної гіперплазії.
Малюнок 3. Подальше імуногістохімічне фарбування. Хоча лімфоїдні фолікули в основному складаються з великих В-клітин у центрі, периферія складалася з дрібних Т-клітин, позитивних на CD3 (a.) та CD5 (b.). Імунозабарвлення для цикліну D1 (c.) був негативним у лімфоїдних клітинах, отже, за винятком лімфоми мантійних клітин.
ОБГОВОРЕННЯ
Реактивна лімфоїдна гіперплазія підшлункової залози є надзвичайно рідкісним станом, лише у деяких випадках описуються повністю, деталізуючи вигляд, оперативні висновки та гістологічну оцінку. Вкрай важко відрізнити від злоякісної пухлини, тому пацієнтам зазвичай пропонують хірургічне втручання.
Лише один із шести попередніх повідомлень про реактивну лімфоїдну гіперплазію мав подібний мультифокальний розподіл до нашого випадку, що вимагав тотальної панкреатектомії [4]. Унікальні особливості серед інших випадків включають супутні знахідки в печінці, як повідомляють Amer та співавт. [1], а також спонтанний регрес вогнища псевдолімфоми в залишковій підшлунковій залозі після хірургічної резекції, як повідомляють Nakata et al. [6].
Точний механізм розвитку реактивної лімфоїдної гіперплазії не ясний. Випадків, пов’язаних із підшлунковою залозою, небагато; тому висновки не можуть бути вилучені. Оглянувши клініко-патологічні характеристики пацієнтів з лімфоїдною гіперплазією печінки, Ishida та співавт. припустив, що аутоімунна або імунна реакція на шлунково-кишкову злоякісну пухлину може бути потенційним пусковим фактором [15]. Виходячи здебільшого з повідомлень про випадки ураження печінки, здається, що цей стан частіше зустрічається у дорослих жінок, фактор, який може бути на користь підозри на аутоімунний механізм. У деяких інших випадках призначення вакцинації або протисудомних препаратів пропонується як пусковий механізм [16, 17]. Реактивна лімфоїдна гіперплазія в першу чергу вважається доброякісним станом, і спостерігається спонтанна регресія уражень печінки та легенів [12, 18]. Однак про злоякісну трансформацію псевдолімфоми також спорадично повідомлялося [19, 20]. З цієї причини термін реактивна лімфоїдна гіперплазія видається більш доречним, оскільки він краще позначає доброякісну природу цієї сутності.
Здається, важко диференціювати точну природу цього незвичайного ураження підшлункової залози лише на основі візуалізації. Згідно з подібними звітами, що стосуються печінки, ці ураження демонструють низький сигнал на Т1-зважених зображеннях та проміжні або високосигнальні Т2-зважені зображення [21]. КТ із посиленням контрастності не може виявити ураження підшлункової залози у нашого пацієнта, підтверджуючи інші повідомлення про те, що лімфоїдна гіперплазія виглядає як гіпердензірованное ураження, яке неможливо відрізнити від злоякісної пухлини підшлункової залози [1, 4]. Однак EUS продемонстрував чітко визначене округле гіпоехогенне ураження судин, що дуже сугестує щодо NET у нашому випадку, але, на жаль, аспірація тонкою голкою (FNA) не була остаточною. Важливо, що первинну лімфому підшлункової залози слід диференціювати від лімфоїдної гіперплазії. Хоча це може поділяти деякі рентгенологічні характеристики [22], діагноз повинен бути підтверджений на основі гістології, отриманої за допомогою FNA-біопсії.
ВИСНОВОК
Хоча надзвичайно рідкісний стан, реактивна лімфоїдна гіперплазія повинна бути включена в диференціальну діагностику гіпоехогенних уражень, локалізованих у підшлунковій залозі. Не можна робити висновки щодо його діагностики та лікування, оскільки до цього часу опубліковано лише декілька статей, що описують цю структуру в підшлунковій залозі. Його доброякісний характер може дозволити більш консервативне ведення (з активним спостереженням), а не радикальну операцію, за умови досягнення остаточного та безпечного діагнозу.
Конфлікт інтересів та джерело фінансування
Автори повідомляють, що вони не мають значних відносин з будь-якими комерційними компаніями, що стосуються цієї статті, або мають фінансовий інтерес до них
- Гострий гострий панкреатит при анорексії та булімії Insight Medical Publishing
- Парентеральне харчування у госпіталізованих дітей Insight Medical Publishing
- Підгострий тиреоїдит та пошкодження міокарда Insight Medical Publishing
- Харчовий протокол для остеоартрозу (дегенеративні захворювання суглобів) Insight Medical Publishing
- Ожиріння, стигматизація ваги та дискримінація Insight Medical Publishing