Відсутність обмеження дієтичного йоду при короткостроковому розвитку гіпотиреозу після терапії радіоактивним йодом із фіксованою дозою при хворобі Грейвса
Jubbin Jagan Jacob
Кафедра ендокринології Християнського медичного коледжу та лікарні, Веллоре, Тамілнад, Індія
Чарльз Стівен
1 Відділ біохімії Християнського медичного коледжу та лікарні, Веллоре, Тамілнад, Індія
Томас В. Павло
Кафедра ендокринології Християнського медичного коледжу та лікарні, Веллоре, Тамілнад, Індія
Ніхал Томас
Кафедра ендокринології Християнського медичного коледжу та лікарні, Веллоре, Тамілнад, Індія
Регі Уммен
2 Відділ ядерної медицини, Християнський медичний коледж та лікарня, Веллоре, Тамілнад, Індія
Мандалам С. Сешадрі
Кафедра ендокринології Християнського медичного коледжу та лікарні, Веллоре, Тамілнад, Індія
Анотація
Передумови:
Збільшення частоти аутоімунних захворювань щитовидної залози із збільшенням споживання йоду з їжею було продемонстровано як епідеміологічно, так і експериментально. Гіпотиреоз, який виникає в перший рік після терапії радіоактивним йодом, ймовірно, пов'язаний із руйнівними ефектами радіації та основним поточним аутоімунітетом.
Завдання:
Для вивчення результатів наприкінці шести місяців після фіксованої дози I, 131 терапія хвороби Грейвса з подальшою дієтою з обмеженим вмістом йоду протягом шести місяців.
Матеріали і методи:
Послідовні дорослі пацієнти з хворобою Грейвса, заплановані на терапію I 131, були рандомізовані або для отримання вказівок щодо обмеження дієтичного йоду, або без рекомендацій до введення I 131 із встановленою дозою (5mCi). Функції щитовидної залози та показники йоду в сечі оцінювали на 3-й та 6-й місяці згодом.
Результати:
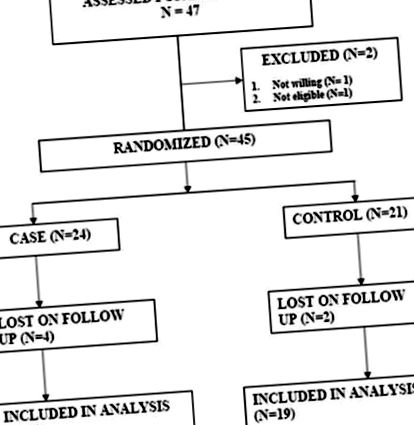
Оцінено 47 пацієнтів (13M та 34F), 2 виключено, 45 рандомізовано (випадки 24 та контроль 21) та 39 пацієнтів завершили дослідження. Базові дані були порівнянними. Середня концентрація йоду в сечі становила 115 та 273 мкг/г мкр (р = 0,00) серед випадків та контролів відповідно. Результати на 3-й місяць були такими (випадки та контроль); Еутиреоїдний (10 і 6: Р = 0,24), Гіпотиреоїдний (3 і 5: Р = 0,38) та Гіпертиреоїдний (7 і 8: Р = 0,64). Результати наприкінці шести місяців були такими (випадки та контроль); Еутиреоїдний (10 і 5: Р = 0,12), Гіпотиреоїдний (3 і 5: Р = 0,38) та Гіпертиреоїдний (7 і 9: Р = 0,43). З пацієнтів з гіпотиреозом 5 (випадки 1 та контролі 4: Р = 0,13) потребували заміщення тироксину.
Висновки:
Не було статистично значущої різниці в результатах лікування пацієнтів з обмеженим вмістом йоду в їжі після терапії I 131 за хворобою Грейвса.
ВСТУП
Радіоактивний йод 131 (RAI) широко використовується для лікування гіпертиреоїдної хвороби Грейвса. Лікування радіоактивним I 131 є безпечним та високоефективним, і єдиним суттєвим ускладненням цієї терапії є розвиток перманентного гіпотиреозу. [1] На додаток до постійного гіпотиреозу, тимчасовий гіпотиреоз може виникнути через 2–5 місяців після терапії I 131, а потім спонтанно затихати протягом наступних кількох місяців. [2,3] Більше 50% пацієнтів, у яких гіпотиреоз розвинувся протягом шести місяців після лікування I 131, спонтанно відновлюються . Середній час розвитку перманентного гіпотиреозу коротший у пацієнтів з тимчасовим гіпотиреозом, ніж у пацієнтів, у яких не розвивається транзиторний гіпотиреоз. [4]
Гіпотиреоз, який виникає в перший рік після терапії радіоактивним йодом, ймовірно, пов'язаний із руйнівними ефектами випромінювання, тоді як подальший розвиток гіпотиреозу обумовлений поєднанням променевої травми та основного та триваючого аутоімунітету [5]. Гіпотиреоз, мабуть, мав би місце у всіх пацієнтів, якби вони прожили достатньо довго. [6,7] Розвиток транзиторного гіпотиреозу із відновленням функції щитовидної залози дехто пов’язував із постійним аутоімунітетом. Тривала присутність тиреотропних антитіл у пацієнтів з тимчасовим гіпотиреозом може відігравати певну роль у відновленні функції щитовидної залози у цієї групи пацієнтів. [4]
Серед різних груп населення епідеміологічні дослідження показали збільшення частоти аутоімунності щитовидної залози зі збільшенням вмісту йоду [8,9,10] Клінічні дослідження також припустили взаємозв'язок збільшення споживання йоду при аутоімунних захворюваннях щитовидної залози [11,12,13]. Однак ефект спостерігався лише у генетично сприйнятливих осіб. [14] Було запропоновано багато механізмів, що пояснюють зв'язок споживання йоду та аутоімунного захворювання щитовидної залози. Вони включають пошкодження утворенням вільних радикалів, пряме пошкодження тироцитів та фармакологічне інгібування йодної помпи. Найважливішим механізмом є, мабуть, сприяння аутоімунітету щитовидної залози через підвищений вміст йоду в тиреоглобуліні. [15]
У цьому дослідженні ми розглядаємо роль дієтичного йоду у розвитку транзиторного та постійного гіпотиреозу у пацієнтів із хворобою Грейвса, які отримували радіоактивний йод протягом шести місяців. Метою дослідження було порівняти частоту постійного та перехідного гіпотиреозу після фіксованої дози радіоактивного йоду серед пацієнтів, рандомізованих на дієтичне обмеження йоду, та тих, хто сидів на нормальній йодовій дієті.
МАТЕРІАЛИ І МЕТОДИ
Набір навчальної когорти проводився з амбулаторного відділення ендокринології університетської навчальної лікарні. Пропозиція щодо дослідження була повідомлена Комітету з огляду установи та затверджена Комітетом до початку дослідження. Всіх дорослих пацієнтів (≥18 років) з аутоімунними захворюваннями щитовидної залози та тиреотоксикозом, які бажали пройти радіоактивне лікування тиреотоксикозу I 131, оцінювали для включення в дослідження. Жінки у репродуктивній віковій групі, які планували зачаття на найближчі 12 місяців, пацієнти з серцевою декомпенсацією, пацієнти з активною офтальмопатією Грейвса (індекс активності понад 4) та ті, хто отримував препарати, що містять йод, були виключені з дослідження.
Після пояснення процедури дослідження пацієнтам були надані бланки інформованої згоди англійською мовою. Рандомізацію проводили за допомогою «методики рандомізації блоків», узявши блоки по чотирьох пацієнтів. У всіх пацієнтів проводилися базові дослідження, включаючи сироватковий стимулюючий гормон (ТТГ), загальний рівень сироватки та рівень вільного тироксину (ТТ4 та ФТ4) та радіоактивне сканування поглинання 131 I через 2 години та 24 години. Для оцінки співвідношення йоду/креатиніну в сечі збирали сечу. Усім досліджуваним пацієнтам була проведена абляція радіоактивним йодом у відділенні ядерної медицини нашої лікарні у фіксованій дозі 5 мкМі (Millicurie). Лікар відділення ядерної медицини переглянув пацієнтів щодо можливості прийому радіоактивної абляції.
Після абляції пацієнти, рандомізовані як випадки, отримували інструкції щодо мінімізації вмісту йоду в дієті. У дієті наголошували на наступних моментах.
Уникання йодованої солі та використання нейодованої кристалічної солі на місцевому рівні.
Уникайте сумішей від кашлю та інших ліків, що продаються без рецепта, без консультації зі слідчим.
Уникайте морської риби та яєчного жовтка.
Відмова від шоколаду та комерційних хлібобулочних виробів.
Уникайте м’ясних та овочевих консервів.
Пацієнту, рандомізованому в якості контролів, давали загальні дієтичні поради та рекомендували використовувати йодовану сіль.
Вимірювання рівня ТТГ у сироватці крові проводили за допомогою IMMULITE ® 2000 (Siemens Healthcare Diagnostics Inc, Deerfield, IL, USA), який являє собою твердофазний двомісний хемілюмінесцентний імунометричний аналіз. Аналіз має аналітичну чутливість 0,04 мкМЕ/л та коефіцієнт варіації (CV) 4,6-12,5%. Загальний вміст сироватки Т4 та вільний Т4 також проводили на IMMULITE ® 2000 (Siemens Healthcare Diagnostics Inc, Deerfield, IL, USA). Аналізи мають аналітичну чутливість 3,86 ммоль/л та 3,86 ммоль/л відповідно з CV 5,6-11,7% для загального аналізу T4 та CV 4,8-9,0% для вільного аналізу T4. Вимірювання креатиніну в сечі для оцінки співвідношення йоду/креатиніну в сечі проводили за допомогою аналізатора Hitachi 912 Auto (F. Hoffmann-La Roche AG, Базель), використовуючи кінетичний аналіз in vitro. Вимірювання йоду в сечі проводили вручну за допомогою реакції Санделя-Колтоффа.
Статистичний аналіз проводили за допомогою Статистичного пакету для соціальних наук версії 11.0. Для визначення статистичної значущості ми використовували точний тест Фішера та Квадрат Chi.
Пацієнти класифікувались як еутиреоїдні під час візиту -2 (через три місяці після абляції) та візиту-3 (через шість місяців після абляції), якщо рівень FT4 знаходився в нормальному для лабораторії діапазоні. Нормалізація ТТГ не розглядалася, оскільки пацієнтам може знадобитися більше часу для відновлення центрального гіпотиреозу. Пацієнтів класифікували як гіпертиреоїдних у візиті -2 (через три місяці після абляції) та візиті-3 (через шість місяців після абляції), якщо рівень FT4 був вище норми для лабораторії. Якщо пацієнти отримували протитиреоїдні препарати під час відвідування-3 для виявлення симптомів, то вони вважалися гіпертиреозом через шість місяців. Пацієнти класифікувались як гіпотиреоїди під час візиту -2 (через три місяці після абляції) та візиту-3 (через шість місяців після абляції), якщо рівень FT4 був нижчим за норму для лабораторії. Крім того, пацієнти з нормальним рівнем FT4 та підвищеним рівнем ТТГ вважалися гіпотиреозом. Хворих на гіпотиреоз також класифікували як центральний, субклінічний або первинний гіпотиреоз. Пацієнти, яким потрібна замісна терапія через три місяці, були класифіковані як такі, що мають первинний гіпотиреоз через шість місяців.
Р РЕЗУЛЬТАТИ
Базові дані
Для дослідження було проаналізовано 47 пацієнтів, було 13 чоловіків та 34 жінки. Середній вік становив 41 рік, а медіана - 40 років. Середня тривалість симптомів при презентації становила понад 22 місяці, а середня тривалість симптомів при появі 12 місяців. Детальна інформація про зарахування пацієнтів, рандомізацію та завершення дослідження наведена на рисунку 1. Порівняння важливих вихідних значень між випадками та контролем 39 пацієнтів, які закінчили дослідження, наведено в таблиці 1. Адекватність обмеження йоду в їжі серед випадків проілюстровано в таблиці 2 .
Деталі зарахування, рандомізації та завершення навчання
Таблиця 1
Таблиця 2
Співвідношення креатиніну йоду з сечею та виведення йоду з сечею у випадках та контролі
Результат у пацієнтів на третьому та шостому місяцях
Результати тестів функції щитовидної залози для пацієнтів на третьому та шостому місяці спостереження були класифіковані на гіпотиреоїдний, еутиреоїдний та гіпертиреоїдний на основі раніше визначених визначень. Детальна інформація наведена в таблиці Таблиця 3 3 та та 4 4 .
Таблиця 3
Результати пацієнтів на третьому місяці
Таблиця 4
Результати пацієнтів на шостому місяці
Деталі гіпотиреозу, що спостерігаються у випадках та контролях
Загалом у дев'яти пацієнтів розвинувся гіпотиреоз. Один пацієнт мав транзиторний гіпотиреоз із відновленням функції щитовидної залози під час другого візиту. Серед восьми пацієнтів, які мали гіпотиреоз у шість місяців, усі, крім одного, також були гіпотиреозом під час тримісячного візиту. Детальна інформація наведена в таблиці 5. На малюнку 2 представлені пацієнти із симптоматичним первинним гіпотиреозом, що потребує заміщення лево-тироксином серед випадків та контролів протягом періоду дослідження.
Таблиця 5
Деталі пацієнтів, у яких розвинувся гіпотиреоз
Розвиток первинного гіпотиреозу, що вимагає лево-тироксину у випадках та контролях
Кореляція між показниками ТТГ у сироватці крові через 6 місяців та співвідношеннями йоду/креатиніну в сечі
На малюнку 3 показана кореляція між найвищими значеннями ТТГ та середньою екскрецією йоду з сечею, оціненою за співвідношенням йод/креатинін.
Кореляція між найвищими значеннями ТТГ та середньою екскрецією йоду з сечею, оціненою за співвідношенням йоду/креатиніну (* Один пацієнт із значенням ТТГ 48 МО (не в іншому місці) був виключений з графіку)
D ІСКУСІЯ
Основною метою лікування тиреотоксикозу хвороби Грейва є зменшення гіперсекреції гормону щитовидної залози. Одна з трьох доступних форм терапії, використання радіоактивного йоду, пов’язана з розвитком гіпотиреозу у значної більшості пацієнтів. У цьому дослідженні ми не змогли знайти значної користі від обмеження йоду в раціоні пацієнтів, які проходять терапію радіоактивним йодом. Не було відмінностей у розвитку гіпотиреозу через три і шість місяців після абляції 131, або в загальних показниках лікування серед пацієнтів, які зазнали обмеження йоду порівняно з контролем.
У дослідженні споживання йоду суб'єктами було обмежено в раціоні переважно шляхом переходу з упакованої йодованої солі на місцево приготовлену розпаковану кристалічну сіль. Було наголошено на униканні інших дієтичних джерел йоду; однак ці джерела не були важливими для більшості пацієнтів. Адекватність дієтичного обмеження відображалася у подальших вимірах співвідношення йоду креатиніну йоду (UIC). Співвідношення UIC має хорошу співвідношення з 24-годинною оцінкою виведення йоду у дорослих.
Транзиторний гіпотиреоз
Загальні показники лікування
Основними недоліками цього дослідження є, по-перше, відсутність ясності щодо того, що становить адекватну дозу радіоактивного йоду серед індійських пацієнтів. Дозування, яке використовувалось у цьому дослідженні, призвело до того, що показники лікування були значно меншими, ніж очікувалось. По-друге, обмежене спостереження протягом шести місяців може призвести до втрати пацієнтів із тимчасовим гіпотиреозом, які відновили функції щитовидної залози через шість місяців. Більший обсяг вибірки у пацієнтів, яким вводили більшу дозу радіоактивного йоду, що проходили спостереження протягом одного року, може бути більш доцільним.
Підсумовуючи, статистично значущої різниці у розвитку явного первинного гіпотиреозу не було після терапії радіоактивним йодом хвороби Грейвса з дієтичним обмеженням йоду. Хоча тенденція до кращого рівня виліковування через 6 місяців була відзначена при дієтичному обмеженні йоду, різниця не була статистично значущою.
ВЗНАННЯ
Пані Бану за допомогу у наборі пацієнтів та введенні даних.
- Короткочасне підвищення споживання дієтичного білка не погіршує резистентність до інсуліну та ліпідів у крові
- Поживні речовини Повний текст Вплив дієтичних фукозильованих олігосахаридів та глікопротеїнів
- PLOS ONE t-10, c-12 CLA Дієтична добавка гальмує розвиток атеросклеротичного ураження, незважаючи на
- Короткотермінові наслідки годування чоловічих суб’єктів фракціями глюкозного сиропу та D-глюкозою - Анотація
- Лікувальна дієта для священного серця на короткий термін для зменшення жиру в організмі; Зберігайте здоровий спосіб життя