NDC 0338-0125 Лактатовані рингери та декстроза
Хлорид натрію, лактат натрію, хлорид калію, хлорид кальцію та моногідрат декстрози
- Індекс етикетки
- Корпорація охорони здоров'я Baxter
- NDC: 0338-0125 Лактатовані рингери та декстроза
Код товару NDC 0338-0125
Запатентована назва: Лактовані рингери та декстроза Що таке запатентована назва?
Запатентована назва, також відома як торгова назва, - це назва продукту, вибраного маркувальником ліків для маркетингових цілей.
Патентована назва: хлорид натрію, лактат натрію, хлорид калію, хлорид кальцію та моногідрат декстрози Що таке непатентована назва?
Непатентована назва іноді називається загальною назвою. Загальна назва зазвичай включає діючу речовину (и) продукту.
- 0338 - Baxter Healthcare Corporation
- 0338-0125 - Звонки з лактацією та декстроза
- 0338-0125-03
- 0338-0125-04
- 0338-0125 - Звонки з лактацією та декстроза
NDC 0338-0125-03
Опис упаковки: 500 мл в 1 мішку
NDC 0338-0125-04
Опис упаковки: 1000 мл в 1 мішку
Інформація про продукт NDC
Лактовані рингери та декстроза з NDC 0338-0125 - це лікарський засіб, що відпускається за рецептом людини, маркується корпорацією Baxter Healthcare Corporation. Загальна назва лактованих рингерів та декстрози - хлорид натрію, лактат натрію, хлорид калію, хлорид кальцію та моногідрат декстрози. Лікарська форма препарату є ін’єкцією, розчином та вводиться через внутрішньовенну форму.
Лікарська форма: ін'єкція, розчин - рідкий препарат, що містить одну або кілька лікарських речовин, розчинених у відповідному розчиннику або суміші взаємозмішуваних розчинників, придатну для ін'єкцій.
Лактатний рингер та активний інгредієнт (и) декстрози
Неактивні інгредієнти)
Шляхи адміністрування
Фармакологічні класи
Інформація про маркування товару
Назва етикетки: Baxter Healthcare Corporation
Код етикетки: 0338
Номер заявки FDA: NDA016679 Що таке номер заявки FDA?
Це відповідає номеру NDA, ANDA або BLA, який повідомляє етикетка для продуктів, які мають відповідну маркетингову категорію. Якщо призначеною маркетинговою категорією є OTC Monograph Final або OTC Monograph Not Final, тоді номер заявки буде цитатою CFR, що відповідає відповідній монографії (наприклад, “частина 341”). Для не затверджених препаратів це поле буде нульовим.
Маркетингова категорія: NDA - продукт, що продається за схваленою Новою заявкою на наркотики. Що таке маркетингова категорія?
Типи продуктів розбиті на кілька потенційних маркетингових категорій, такі як NDA/ANDA/BLA, OTC Monograph або Unapproved Drug. Для товару може бути обрана одна і одна маркетингова категорія, не всі маркетингові категорії доступні для всіх типів товарів. В даний час включені лише кінцеві товарні категорії продуктів. Повний список кодів та перекладів можна знайти на веб-сайті www.fda.gov/edrls у розділі Структуровані ресурси маркування продуктів.
Дата початку маркетингу: 03-22-1971 Яка дата початку маркетингу?
Це дата, яку маркувальник вказує на початок збуту лікарського препарату.
Дата закінчення лістингу: 12-31-2021 Що таке дата закінчення лістингу?
Це дата, коли термін дії запису про лістинг закінчується, якщо його не оновити чи не засвідчити етикетка товару.
Прапор виключення: N Що таке прапор виключення NDC?
У цьому полі вказується, чи виріб було вилучено/виключено з каталогу NDC за відмову відповідати на запити FDA про виправлення дефектних чи невідповідних подань. Значення = "Y" або "N".
* Будь ласка, ознайомтесь із застереженням нижче.
Зображення етикеток на лактатованих дзвіночках та декстрозі
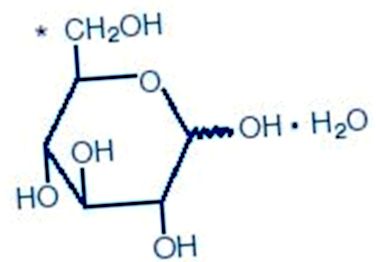
Хімічна структура - зображення 01
Ін’єкція лактатного Рінгера та 5% декстрози, етикетка контейнера USP - зображення 02
Етикетка для упаковки лактатного Рінгера та 5% ін’єкції декстрози USP - зображення 03
Інформація про маркування лактатних рингерів та декстрози
Інформація щодо маркування товару включає всі опубліковані матеріали, пов’язані з лікарським засобом. Документи щодо маркування продуктів включають таку інформацію, як загальні назви, активні інгредієнти, дозування інгредієнта, способи введення, зовнішній вигляд, використання, попередження, неактивні інгредієнти тощо.
Індекс маркування товару
Лактат Рінгер та ін’єкція декстрози 5%, USP має значення як джерело води, електролітів та калорій. Він здатний викликати діурез в залежності від клінічного стану пацієнта. Лактат Рінгера та 5% ін’єкція декстрози USP надає метаболічний лужний ефект. Лактатні іони в кінцевому підсумку метаболізуються до вуглекислого газу та води, що вимагає споживання катіонів водню.
Показання та застосування
Лактатний Рінгер та ін’єкція декстрози 5%, USP вказується як джерело води, електролітів та калорій або як лужний засіб.
Як і для інших інфузійних розчинів, що містять кальцій, одночасне введення цефтріаксону та ін’єкцій лактатного Рінгера та 5% ін’єкції декстрози, USP протипоказаний новонародженим (вік ≤ 28 днів), навіть якщо використовуються окремі інфузійні лінії (ризик летального результату солі цефтріаксон-кальцію у пацієнтів старше 28 днів (включаючи дорослих) цефтріаксон не можна вводити одночасно з внутрішньовенними розчинами, що містять кальцій, включаючи лактат Рінгера та 5% ін’єкцію декстрози, USP, через ту саму інфузійну лінію (наприклад, через Y-роз'єм). Якщо одна і та ж інфузійна лінія використовується для послідовного введення, лінію необхідно ретельно промити між інфузіями сумісною рідиною. Лактатовий Рінгер та 5% ін’єкція декстрози, USP протипоказаний пацієнтам з відомою гіперчутливістю до лактату натрію.
Немає адекватних та добре контрольованих досліджень з ін’єкцією лактатного Рінгера та 5% ін’єкцією декстрози, USP у вагітних жінок, а також дослідження репродукції тварин з цим препаратом не проводились. Отже, невідомо, чи може лактатний Рінгер та 5% ін’єкція декстрози, USP, завдати шкоди плоду при введенні вагітній жінці. Лактат Рінгера та ін’єкцію декстрози 5%, USP слід вводити під час вагітності, лише якщо потенційна користь виправдовує потенційний ризик для плода.
Праця та доставка
Внутрішньовенна внутрішньовенна інфузія розчинів, що містять глюкозу, може спричинити гіперглікемію матері з подальшою гіперглікемією плода та метаболічним ацидозом плода, а також гіпоглікемію у новонароджених. Гіперглікемія плода може призвести до підвищення рівня інсуліну у плода, що може призвести до новонародженої гіпоглікемії після пологів. Розгляньте потенційні ризики та переваги для кожного конкретного пацієнта перед введенням лактатного Рінгера та ін’єкції 5% декстрози, USP.
Невідомо, чи присутній цей препарат у жіночому молоці. Оскільки в грудному молоці присутній багато препаратів, слід дотримуватися обережності при прийомі лактатного Рінгера та 5% ін’єкції декстрози, USP годуючій матері.
Застосування лактатного Рінгера та 5% ін’єкції декстрози, USP, у педіатричних пацієнтів базується на клінічній практиці (див. ДОЗИРОВАННЯ ТА АДМІНІСТРАЦІЯ). Новонароджені, особливо народжені недоношеними та з низькою вагою, мають підвищений ризик розвитку гіпо- або гіперглікемії, тому потребують пильного контролю під час лікування внутрішньовенними розчинами глюкози, щоб забезпечити належний глікемічний контроль, щоб уникнути потенційних довгострокових несприятливих наслідків. Гіпоглікемія у новонародженого може спричинити тривалі судоми, кому та пошкодження головного мозку. Гіперглікемія була пов’язана з внутрішньошлуночковими крововиливами, пізнім початком бактеріальних та грибкових інфекцій, недоношеною ретинопатією, некротизуючим ентероколітом, бронхолегеневою дисплазією, тривалим терміном перебування в лікарні та смертю. Розчини, що містять лактат, слід з особливою обережністю вводити новонародженим та немовлятам до 6 місяців.
Клінічні дослідження ін'єкцій лактатного Рінгера та 5% ін'єкції декстрози, USP не включали достатню кількість пацієнтів віком від 65 років, щоб визначити, чи вони реагують інакше, ніж молоді. Інший зареєстрований клінічний досвід не виявив відмінностей у відповідях між пацієнтами похилого та молодшого віку. Як правило, підбір дози для пацієнта літнього віку повинен бути обережним, як правило, починаючи з нижнього кінця діапазону дозування, що відображає більшу частоту зниження функції печінки, нирок або серця, а також супутніх захворювань або іншої лікарської терапії.
Побічні реакції після маркетингу
Наступні побічні реакції були зареєстровані в процесі постмаркетингового досвіду під час використання лактатного Рінгера та 5% ін’єкції декстрози, USP: Реакції гіперчутливості/інфузії, включаючи анафілактичні/анафілактоїдні реакції, та такі прояви: ангіоневротичний набряк, біль у грудях, дискомфорт у грудях, бронхоспазм, задишка, кашель, кропив'янка, висип, свербіж, еритема, нудота та пірексія. Також повідомляється про реакції на місці інфузії, включаючи свербіж у місці інфузії, еритему в місці інфузії, знеболення в місці інфузії (оніміння). Інші побічні реакції, про які повідомляють при ін’єкції лактатного Рінгера без ін’єкцій декстрози та лактату натрію є: зниження частоти серцевих скорочень, тахікардія, зниження артеріального тиску, респіраторний дистрес, набряк гортані, гіперемія, подразнення горла, парестезії, гіпестезія через рот, дисгевзія, тривога, головний біль та чхання, гіперкаліємія, гіперволемія та інше місце інфузії. реакції, такі як інфекція в місці ін’єкції, флебіт, екстравазація, інфузія ite запалення, набряк місця інфузії, висип місця інфузії, біль місця інфузії, печіння місця інфузії.
Надмірний об’єм або занадто висока швидкість введення ін’єкцій лактатного Рінгера та 5% ін’єкції декстрози, USP може призвести до перевантаження рідиною та натрієм з ризиком набряків (периферичних та/або легеневих), особливо коли порушується ниркова екскреція натрію. Надмірне введення лактату може призвести до метаболічного алкалозу. Метаболічний алкалоз може супроводжуватися гіпокаліємією. Надмірне введення калію може призвести до розвитку гіперкаліємії, особливо у пацієнтів з важкими порушеннями функції нирок. Надмірне введення солей кальцію може призвести до гіперкальціємії. Надмірне введення розчину, що містить декстрозу, може призвести до гіперглікемії, гіперосмолярності, осмотичного діурезу та дегідратації. При оцінці передозування також слід враховувати будь-які добавки в розчині. Наслідки передозування можуть вимагати негайної медичної допомоги та лікування.
Дозування та введення
Ін’єкція лактатного Рінгера та 5% декстрози, USP у пластикових контейнерах VIAFLEX доступна наступним чином: CodeSizeNDC2B2073 500 mLNDC 0338-0125-032B20741000 mLNDC 0338-0125-04Від впливу фармацевтичних продуктів на нагрівання слід мінімізувати. Уникайте надмірного нагрівання. Рекомендується зберігати продукт при кімнатній температурі (25 ° C); нетривала експозиція до 40 ° C не впливає негативно на продукт.
Вказівки щодо використання пластикового контейнера Viaflex
Baxter Healthcare Corporation, Дірфілд, Іллінойс, США 60015, США Друк у США 07-19-73-100 Рев. Грудень 2017 р. Baxter, Viaflex та PL 146 є товарними знаками Baxter International Inc.
- Переглянуті контрольні значення споживання натрію та хлориду
- Поживні речовини Безкоштовні повнотекстові ідентифікаційні взаємодії між дієтичним натрієм та калієм,
- Топографія поверхні білка як інструмент для посилення селективної активності калієвого каналу
- Дзвоник; s Лактатна стаття
- Рецензовані зміни в розмірі порцій, калоріях та вмісті натрію в перероблених продуктах з 2009 по 2009 рік