Короткочасні наслідки споживання компонентів кави на мікробіоти кишечника у пацієнтів з неалкогольною жирною печінкою та діабетом: Пілотне рандомізоване плацебо-контрольоване клінічне випробування
Асі Мансур
1 Кафедра клінічного харчування та дієтології, Факультет харчування та харчових технологій, Національне харчування та харчові технології, Науково-дослідний інститут Університету медичних наук Шахіда Бехешті, Тегеран, Іран
2 Дослідницький центр ендокринології та метаболізму, Інститут клінічних наук ендокринології та метаболізму, Тегеранський університет медичних наук, Тегеран, Іран
Мохаммад Реза Мохаджері-Техерані
2 Центр досліджень ендокринології та метаболізму, Інститут клінічних наук ендокринології та метаболізму, Тегеранський університет медичних наук, Тегеран, Іран
Сара Карімі
1 Кафедра клінічного харчування та дієтології, Факультет харчування та харчових технологій, Національне харчування та харчові технології, Науково-дослідний інститут Університету медичних наук Шахіда Бехешті, Тегеран, Іран
Мілад Сангінабаді
3 Відділ рентгенології, лікарня Шаріаті, Тегеранський університет медичних наук, Тегеран, Іран
Хоссейн Поусті
4 Центр досліджень хвороб печінки та панкреатобіліарних захворювань, Інститут досліджень хвороб органів травлення, Тегеранський університет медичних наук, Тегеран, Іран
Самане Енаяті
5 Дослідницький центр метаболічних розладів, Інститут молекулярних клітинних наук ендокринології та метаболізму Тегеранського університету медичних наук, Тегеран, Іран
Саїде Асгарбейк
5 Науково-дослідний центр метаболічних розладів, Інститут молекулярних клітинних наук ендокринології та метаболізму Тегеранського університету медичних наук, Тегеран, Іран
Джавад Насролахзаде
1 Кафедра клінічного харчування та дієтології, Факультет харчування та харчових технологій, Національне харчування та харчові технології, Науково-дослідний інститут Університету медичних наук Шахіда Бехешті, Тегеран, Іран
Азіта Хекматдуст
1 Кафедра клінічного харчування та дієтології, Факультет харчування та харчових технологій, Національне харчування та харчові технології, Науково-дослідний інститут Університету медичних наук Шахіда Бехешті, Тегеран, Іран
Пов’язані дані
Анотація
Вступ
Кава - найпопулярніший напій у всьому світі. Таким чином, його вплив на організм людини може бути важливим у популяційному масштабі. Кава виробляється з насіння кавових рослин, рід Coffee, що містить понад 1000 біоактивних сполук (Gomez-Juaristi et al., 2018 [11]; Jeszka-Skowron et al., 2015 [16]). Найважливішими біоактивними сполуками кави є хлорогенові кислоти та кофеїн; однак біохімічні склади кінцевої кави різні, залежно від типу насіння та методів приготування.
Зв'язок між споживанням кави та смертністю від усіх причин та конкретною причиною досліджувались у кількох спостережних дослідженнях. Більшість із цих досліджень повідомляють про зворотний зв'язок між смертністю від усіх причин та специфікою для певної причини, а також споживанням кави, що містить кофеїн та без кофеїну (Grosso et al., 2016 [12]). Більше того, раніше повідомлялося про негативну асоціацію споживання кави з метаболічними, шлунково-кишковими та печінковими порушеннями (Awaad et al., 2011 [3]; Gutierrez-Grobe et al., 2012 [13]; Hodge et al., 2017 [ 14]; Kennedy et al., 2016 [19]; Molloy et al., 2012 [24]; Santos and Lima, 2016 [31]; Vitaglione et al., 2012 [34]). Нещодавній парасольковий огляд та мета-аналіз зв'язку між споживанням кави та здоров'ям дійшов висновку, що корисні зв'язки між споживанням кави та результатами печінки мають відносно великі та постійні розміри ефекту порівняно з іншими результатами (Poole et al., 2017 [28]).
У попередніх дослідженнях, що оцінювали взаємозв’язок між споживанням кави та хронічними розладами, є кілька обмежень. По-перше, більшість цих досліджень були спостережними дослідженнями. Таким чином, вони не могли висувати причинних вимог. По-друге, існує кілька незрозумілих змінних у визначенні експозиції, включаючи склад кави, способи приготування та нерегулярність звичок споживання кави.
Всі ці обмеження свідчать про необхідність проведення контрольованих клінічних випробувань із відомими кількостями компонентів кави, щоб знайти будь-яку можливу взаємозв'язок причини та наслідки, одночасно розглядаючи механізм дії. З іншого боку, нещодавнє дослідження, проведене на 16 здорових суб’єктах, повідомило, що 3 чашки на день споживання кави протягом 3 тижнів збільшували кількість Bifidobacterium spp. популяція у фекальних зразках учасників (Jaquet et al., 2009 [15]). Таким чином, ми припустили, що корисні асоціації споживання кави з порушеннями обміну речовин можуть бути зумовлені її впливом на мікробіоти кишечника; однак, ймовірний його діючий компонент невідомий. Тому ми розробили це пілотне дослідження для оцінки впливу двох основних компонентів кави, кофеїну та хлорогенної кислоти, на мікробіоти кишечника у пацієнтів з неалкогольною жировою хворобою печінки (НАЖХП) та діабетом 2 типу.
Матеріал та методи
Відбір та набір працевлаштування
Пацієнтів віком 30-65 років з діабетом в анамнезі було виявлено та набрано з клініки ендокринології в лікарні Шаріаті, Тегеран, Іран. Діагноз НАЖХП був поставлений за наявністю стеатозу при ультразвуковому дослідженні (УЗД), асоційованого зі стеатозом 2 або більше ступеня при обстеженні Фіброскан. Критеріями виключення було споживання будь-якого виду антибіотиків за 2 тижні до і під час дослідження, професійний спортсмен, прийом будь-яких інших препаратів, крім пероральних препаратів від діабету, вірусний гепатит, вживання алкоголю, цироз печінки, інші причини хронічних захворювань печінки, гіпотиреоз, ниркові, кишкові та серцево-судинні розлади, індекс маси тіла (ІМТ)> 35 кг/м 2, перебування на спеціальній дієті, будь-яка зміна гіпоглікемічних препаратів, психічні розлади, що погіршують здатність пацієнта надавати письмову інформовану згоду, а також вагітність, лактація.
Вивчати дизайн
Набрано всіх пацієнтів із діабетом 2 типу. Після пояснення протоколу дослідження пацієнти підписали інформовану форму згоди, яку схвалив комітет з етики Національного інституту розвитку медичних досліджень (NIMAD). Пацієнти пройшли іспит у США. Якщо на іспиті в США були які-небудь докази печінкового стеатозу 2 ступеня або більше, їм проводили тест Фіброскан. У це дослідження були включені ті пацієнти, які мали стеатоз 2 або більше ступеня на іспиті Фіброскан (оцінка контрольованого параметра ослаблення (CAP)> 263).
Учасники були випадковим чином розподілені до чотирьох груп для отримання або 200 мг кофеїну плюс 200 мг хлорогенової кислоти (CFCA), або 200 мг кофеїну плюс 200 мг плацебо (крохмаль) (CFPL), або 200 мг хлорогенової кислоти плюс 200 мг плацебо (CAPL ), або 200 мг плацебо плюс 200 мг плацебо (PLPL) протягом 12 тижнів. Списки рандомізації були створені комп'ютером статистиком і передані інтерв'юеру. Суб'єкти, слідчі та персонал були засліплені призначенням лікування до кінця дослідження. На момент рандомізації були зібрані вихідні дані, і учасники отримували 4-тижневий запас добавок. За учасниками спостерігали кожні 4 тижні, щоб оцінити їх відповідність. Прихильність оцінювали за кількістю капсул, підтвердженою під час кожного відвідування. Всі добавки були надані Arjuna Natural Extract, Індія.
Клінічна, параклінічна та дієтична оцінка споживання
Антропометричні вимірювання проводились для всіх учасників на початку дослідження та на 12-му тижні втручання. Індекс маси тіла (ІМТ) обчислювали шляхом ділення ваги пацієнта в кілограмах на його або її зріст у метрах у квадраті. Обставини талії вимірювали відповідно до рекомендацій ВООЗ (ВООЗ, 2012 [36]).
На початку та в кінці дослідження відбирали кров натще і зразки калу і зберігали при морозильній камері до -80 ° C до аналізу. Всі біохімічні вимірювання проводились в одній лабораторії одним і тим же техніком із застосуванням стандартних методів. Концентрацію глюкози натще оцінювали за методом GOD/POD. Концентрацію інсуліну натще оцінювали за допомогою імуноферментного аналізу (Mercodia AB, Швеція). Оцінка моделі гомеостазу - інсулінорезистентність (HOMA-IR) була використана для визначення ступеня інсулінорезистентності за такою формулою (Matthews et al., 1985 [21]): HOMA-IR = [інсулін натще (мО/л) × глюкоза в крові натще (мг/дл)]/405. γ-глутамілтрансферазу (GGT) вимірювали за допомогою ферментативного колориметричного аналізу (Parsazmoun, Тегеран, Іран). Концентрації аланінамінотрансферази (ALT) та аспартатамінотрансферази (AST) вимірювали за допомогою фотометричного аналізу (Reckon, Вадодара, Індія). Концентрацію високочутливого C-реактивного білка (hs-CRP) вимірювали за допомогою імуноферментного аналізу (Diagnostics Biochem Canada Inc.).
Для оцінки споживання їжі на початку та в кінці дослідження збирали записи дієтичної їжі протягом трьох днів, включаючи вихідні. Потім дієтичне споживання аналізували за допомогою Nutritionist 4 (First DataBank, Сан-Бруно, Каліфорнія), включаючи використання харчових ваг та моделей для підвищення точності розміру порції. Фізичну активність також оцінювали за допомогою опитувальника "Метаболічний еквівалент завдання" (MET) (Ainsworth et al., 2000 [2]) на початку та в кінці цього дослідження.
Витрати енергії у спокої (РЗЕ) вимірювали на початку та в кінці дослідження за допомогою метаболічного аналізатора FitMate ™ (Cosmed, Рим, Італія). Деталі процедури були описані раніше (Shaneshin et al., 2011 [32]). Склад тіла оцінювали за допомогою аналізатора імпедансу тіла (BIA) (Таніта, штат Ілінойс, США) на початку та в кінці дослідження.
Кишковий мікробний аналіз
На початку та в кінці дослідження зразки калу збирали у стерильні контейнери. Зразки доставляли в лабораторію замороженими і зберігали при -80 ° C до аналізу.
Вилучення ДНК з 1 грама випорожнень проводили за допомогою міні-набору QIAamp DNA Stool Mini (Qiagen) відповідно до інструкцій виробника.
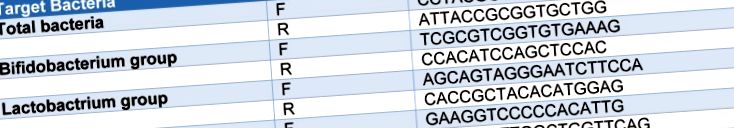
Аналіз ланцюгової реакції зворотної транскриптази (RT-qPCR) проводили за допомогою системи Light Cycler 480 (Рош, Німеччина). Групові та видоспецифічні праймери для ПЛР наведені в таблиці 1 (табл. 1) (Yoon et al., 2014 [37]). Праймери були комерційно синтезовані Такапузістом (Тегеран, Іран). Кількісну ПЛР проводили в 96-лункових планшетах у кінцевих обсягах 20 мкл, що складаються з 1 мкл фекальної ДНК, 0,5 мкл праймерів (по 10 пмоль кожен), 10 мкл SYBR Green I master (Рош, Німеччина) та 8 мкл H2O . ПЛР-ампліфікація включала: попередню інкубацію при 94 ° C протягом 4 хв з наступним 55 циклами ампліфікації (денатурація при 94 ° C протягом 15 секунд, відпал грунтовки при 55 ° C протягом 15 секунд і подовження при 72 ° C протягом 20 секунд) . Криві плавлення отримували нагріванням зразків від 50 ° С до 90 ° С зі швидкістю 5 ° С/с.
Статистичний аналіз
Аналіз проводили за допомогою SPSS 20.0 (для Windows SPSS Inc., Чикаго, Іллінойс). Дані для нормально розподілених та категоріальних змінних подаються відповідно як середнє значення ± стандартне відхилення та відсоток частоти. Для оцінки відмінностей між групами на вихідному рівні використовували дисперсійний аналіз (ANOVA). Порівняння змін (кінцева точка мінус вихідний рівень) після втручання між групами було зроблено за допомогою ANOVA, а за допомогою тесту Post Hoc Tukey для порівняння змін груп. Для контролю незрозумілих змінних застосовували тест аналізу коваріації (ANCOVA). Аналіз ANCOVA був скоригований на базове значення кожної змінної, споживання енергії, кави, чаю та клітковини. Статистичну значимість було встановлено на рівні p (рис. 1). Жоден з учасників не був виключений з дослідження протягом 12 тижнів спостереження. Усі учасники споживали більше 98% своїх добавок відповідно до кількості капсул під час кожного наступного візиту. Базові характеристики пацієнтів чотирьох груп представлені в таблиці 2 (табл. 2). Як показано, всі дослідні групи були добре підібрані щодо базових характеристик. У таблиці 3 (табл. 3) показано вплив кожного добавки на антропометричні та біохімічні вимірювання через 12 тижнів. Вага значно зменшився у групі CFCA порівняно з усіма іншими групами (p = 0,005 для PLPL; p = 0,023 для CAPL; і p = 0,031 для CFPL). Більше того, ІМТ знижувався у CFCA значно більше, ніж у PLPL та у групах CAPL (p = 0,009 та p = 0,033, відповідно). Крім того, споживання енергії зменшилось у групі CFPL значно більше, ніж у групі PLPL (p = 0,032). Інших суттєвих відмінностей у змінах біохімічних та антропометричних вимірювань серед чотирьох груп не було. До того ж, дієтичне споживання клітковини, чаю, кави, макроелементів та мікроелементів не суттєво відрізнялося між групами та всередині груп.
CF, хлорогенова кислота; CA, кофеїн; PL, плацебо
Log10 кількість бактерій Bifidobacteria, Lactobacillus і Bacteriodes на один грам калу до та після втручання у кожній групі показано на малюнку 2 (рис. 2). Незважаючи на те, що кількість кишкових біфідобактерій зростало в групі CFCA, не було статистично значущих відмінностей в межах та між групами в кількості бактерій. Жодних побічних ефектів протягом періоду дослідження не повідомлялось у жодного учасника.
CF, хлорогенова кислота; CA, кофеїн; PL, плацебо
Для отримання додаткових результатів див. Додаткові дані.
Обговорення
Це експериментальне рандомізоване, плацебо-контрольоване клінічне випробування показало, що добавки кофеїну в дозі 200 мг/день плюс 200 мг/день хлорогенних кислот протягом 12 тижнів були ефективними у зниженні ваги у хворих на цукровий діабет та НАЖХП, ймовірно через збільшення кількості кишкові біфідобактерії.
Добавки як кофеїну, так і хлорогенної кислоти (CFCA) мали певний благотворний вплив на метаболічні порушення учасників; однак ефект був статистично значущим лише у випадку втрати ваги. Попередні експериментальні дослідження також повідомляли про вплив споживання кави на втрату ваги (Salomone et al., 2017 [30]), але дослідження на людях обмежуються здоровими добровольцями без оцінки втрати ваги (Wedick et al., 2011 [35]) та зі спірними результатами в оцінці інших метаболічних порушень (Agudelo-Ochoa et al., 2016 [1]; Kempf et al., 2010 [18]; Lecoultre et al., 2014 [20]; Moisey et al., 2008 [22]; Папаконстантину та ін., 2016 [26]). У нашому дослідженні значне зниження ваги могло бути зумовлене збільшенням кількості кишкових біфідобактерій (Karbaschian et al., 2018 [17]; Mokhtari et al., 2019 [23]; Rashvand et al., 2018 [29]). Чи дозування наших добавок було недостатньо, щоб викликати суттєвий вплив на порушення обміну речовин, чи інші компоненти кави могли б бути ефективними для отримання корисних результатів, залишається з’ясувати у майбутніх дослідженнях.
Найважливішою перевагою цього дослідження є те, що це перше рандомізоване, контрольоване плацебо, клінічне випробування пацієнтів з НАЖХП та діабетом, що оцінює вплив двох основних компонентів кави на мікробіоти кишечника. Оскільки це було пілотне дослідження, воно мало деякі обмеження, такі як низький обсяг вибірки, коротка тривалість дослідження та обмеження дозування добавок та кількість вимірюваних бактерій; однак це може пролити світло на майбутній шлях клінічних випробувань для оцінки впливу кави та її компонентів у пацієнтів із НАЖХП та/або діабетом.
Висновок
На закінчення, наше дослідження показало, що споживання 12 тижнів кофеїну 200 мг/день хлорогенної кислоти 200 мг/день ефективно зменшує вагу пацієнтів з НАЖХП та діабетом без будь-яких побічних ефектів. Ці ефекти можуть бути принаймні частково зумовлені зростанням кількості кишкових біфідобактерій. Це пілотне дослідження дало підказку для подальших клінічних випробувань у цих пацієнтів.
Скорочення
НАЖХП, Безалкогольна жирова хвороба печінки; Туалет, окружність талії; ІМТ, індекс маси тіла; MET, метаболічний еквівалент завдань; АЛТ, аланінамінотрансфераза; AST, аспартатамінотрансфераза; GGT, γ-глутамілтрансфераза; ФБС, рівень цукру в крові натще; LDL-C, ліпопротеїди низької щільності; HDL-C, ліпопротеїни високої щільності; hs-CRP, високочутливий С реактивний білок; РЗЕ, витрата енергії в спокої; МВ, кофеїн; СА, хлорогенова кислота; PL, плацебо.
Подяка
Дослідження було підтримане Національним інститутом розвитку медичних досліджень (NIMAD) для AH з грантовим номером 963356.
Внески авторів
AM, MRM та AH розробили пропозицію, отримали етичні схвалення, подали заявки на фінансування, контролювали збір даних та підготували перший проект. AM та AH задумали цю ідею, надавши досвід у розробці та аналізі дослідження. SK, MS, HP, SE та SSA брали участь у дослідних експериментах та аналізі.
Схвалення етики та згода на участь
Етичне підтвердження було взято з Національного інституту розвитку медичних досліджень (NIMAD) з номером IR-NIMAD-REC.1396.191. Інформована згода була взята від усіх учасників.
Конкуруючі інтереси
Автори заявляють, що у них немає конкуруючих інтересів.
- Полісорб Побічні ефекти Поширені, важкі, тривалі
- Поживні речовини Безкоштовний повнотекстовий ефект добавки синбіотиків на мікробіоти кишечника людини, склад тіла
- Плавання з обмеженими можливостями - короткостроковий огляд Форумів про повільний перемикач на форумі Тріатлону
- Побічні ефекти ритуксимабу загальні, важкі, тривалі
- Чи варто пити каву перед бігом