Їжа для роздумів: дієтичне втручання в рідкісних випадках серйозної вентиляційної недостатності
Генрі Юнг
1 Дихальне відділення, лікарні Кембриджського університету, Кембридж, Великобританія
2 Інститут Рейна, Університетський коледж Лондона, Лондон, Великобританія
Кешав Шарма
1 Дихальне відділення, лікарні Кембриджського університету, Кембридж, Великобританія
Вільям Квіти
1 Дихальне відділення, лікарні Кембриджського університету, Кембридж, Великобританія
Малкольм Маркетт
1 Дихальне відділення, лікарні Кембриджського університету, Кембридж, Великобританія
Лора Стараце
3 Команда з питань харчування та дієтології, лікарні Кембриджського університету, Кембридж, Великобританія
Клер Сандер
1 Дихальне відділення, лікарні Кембриджського університету, Кембридж, Великобританія
Горобина Бернштейн
4 відділення нейрокритичної допомоги, лікарні Кембриджського університету, Кембридж, Великобританія
Юрген Герре
1 Дихальне відділення, лікарні Кембриджського університету, Кембридж, Великобританія
Анотація
Пластичний бронхіт - рідкісний стан, що характеризується утворенням ендобронхіального гіпсу. Ми повідомляємо про випадок із 53-річними жінками, які погіршились після процедури планової бронхоскопії. У неї розвинулася рефрактерна вентиляційна недостатність, і вона вимагала повторної бронхоскопії, яка визначала товсті чіпкі гіпси як причину її компрометації в дихальних шляхах. Вона не реагувала на звичайну терапію, включаючи ендоскопічний кліренс, муколітичну терапію та небулайзований тканинний активатор плазміногену (ТРА). Загальне парентеральне харчування та нежирна ентеральна дієта були встановлені, коли пацієнтка перебувала на екстракорпоральній мембранній оксигенації (ECMO), що призвело до значного поліпшення її стану та продемонструвало важливість дієтичних стратегій у цьому випадку.
НАВЧАЛЬНІ ТОЧКИ
Пластичний бронхіт рідко може спостерігатися у дорослих з гострою вентиляційною недостатністю та небезпечною для життя обструкцією дихальних шляхів.
Хоча не існує встановлених вказівок щодо ведення лікування, дієтичне втручання (наприклад, нежирна дієта) слід розглядати як терапевтичний варіант.
Екстракорпоральна мембранна оксигенація (ECMO) є можливою, і її слід враховувати при пластичному бронхіті з порушенням дихальних шляхів.
ВСТУП
Пластичний бронхіт - рідкісний стан, що характеризується утворенням ендобронхіального гіпсу [1]. Альтернативні дескриптори включають гіпсовий бронхіт, бронхіт Гофмана, фібринозний бронхіт та псевдомембранозний бронхіт [2]. Вперше він був описаний Галеном у ІІ столітті нашої ери як „venae arteriosae expectorantii”, в перекладі як „відхаркувані артерії та вени”. Запропоновані механізми включають запальну реакцію при астмі, підвищений легеневий венозний тиск після процедури Фонтана та лімфатичну аномалію, що призводить до витоку хайла.
ОПИС СПРАВИ
53-річну жінку скерували в грудну клініку з тримісячним анамнезом відхаркування бронхіальних зліпків. Їй діагностували астму 21 рік тому і їй лікували інгалятори Бекотид та Вентолін. Її історія хвороби включала синдром полікістозу яєчників, гірсутизм, цукровий діабет 2 типу та ожиріння. З 1990-х років у неї повторювались напади перикардиту з нормальною коронарною ангіограмою та результатами МРТ серця. Раніше її досліджували на предмет артралгії, втоми, двостороннього переднього увеїту та виразки ротової порожнини без ураження статевих органів. Було запропоновано хворобу Бехчета, але розслідування щодо неї були негативними.
У клініці вона повідомляла про стискання грудної клітки та задишку без хрипів. Вона виробляла густу мокроту, схожу на зліпки, 10–12 разів на день. Вона ніколи не курила. Серологічні дослідження, включаючи IgE, специфічний IgE для Aspergillus fumigatus та ANCA, не були помітними. Історична кількість еозинофілів була в межах норми. Тести функції легенів показали мінімальний обструктивний дефект: обсяг форсованого видиху за 1 секунду 2,13 л (88,2%), вимушена життєва ємність 2,89 л (прогнозовано 101,6%) та коефіцієнт форсованого видиху 67,2% при нормальних обсягах легенів і переносі газу. Піковий потік коливався від 350 до 400 л/хв з мінімальними добовими варіаціями. Базова комп’ютерна томографія (КТ) грудної клітки виявила помірне захоплення повітря відповідно до захворювання малих дихальних шляхів. Проведена бронхоскопія, яка не показала ендобронхіальних уражень, виділень та аномального запалення дихальних шляхів. Звичайні біопсії слизової оболонки ендобронхіальних тканин були взяті для гістопатології.
Госпіталізація
Пацієнта повторно прийняли на наступний день після бронхоскопії з кашлем, задишкою та пірексією. Рентгенографія грудної клітки показала докази консолідації правої нижньої частки (рис. 1). Почали внутрішньовенне введення ципрофлоксацину та метронідазолу, а потім ванкоміцину та гідрокортизону. Ехокардіограма біля ліжка не виявила значного розширення або порушення функції шлуночків. Пацієнт погіршився, незважаючи на високий потік кисню та неінвазивну вентиляційну підтримку, і йому потрібна була штучна вентиляція через 6 днів після прийому.
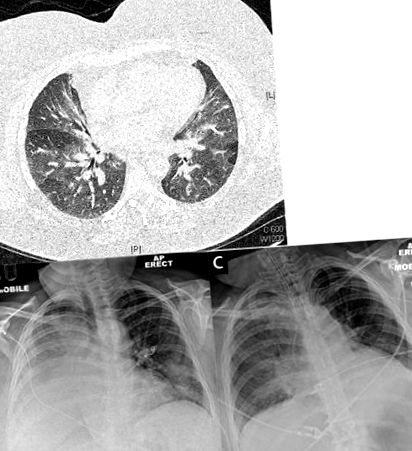
(а) Знімок КТ на початковому рівні показав докази захоплення повітря на видиху, що свідчить про захворювання малих дихальних шляхів. (b) Рентгенограма грудної клітки під час раннього прийому показала колапс і консолідацію правої нижньої частки. (c) Вирішення рентгенологічних змін після бронхоскопічного кліренсу дихальних шляхів.
Культури бронхо-альвеолярного промивання вирощували змішану дихальну флору. Респіраторна вірусна ПЛР, скринінг ВІЛ та сечові антитіла до легіонели були негативними. Було відкладено виявлення Pneumocystis jirovecii (цикл 33), який, ймовірно, являв собою колонізацію. Антибіотики були замінені на меропенем та кларитроміцин. Вентиляція була утруднена через фібринозних гіпсів, що закупорювали її дихальні шляхи. Повторні бронхоскопії виявляли товсті чіпкі зліпки, які видаляли щипцями для біопсії та великими обсягами сольових припливів (рис. 2 та 3). 3). Не було доказів пошкодження дихальних шляхів або стенозів. Повернута рідина мала хилозний характер, що відображає можливу лімфатичну патологію.
(а – с) Бронхоскопія показала товсті білі чіпкі пробки, що перешкоджають правій нижній частці, що вимагало видалення щипцями для біопсії. (г) Процедура повторення показує значне поліпшення деяких залишкових гранулятів на тканині в нижніх частках.
(а) Промивна рідина бронхів показала білий непрозорий шар, що припускає, що вона може мати хилозний характер. (b) Бронхіальні зліпки у вигляді агрегованих сегментів, що нагадують анатомію бронхіальної стінки. (c) Крупний план однієї бронхіальної гіпсової пов’язки
Випробовували небулайзований ацетилцистеїн, фізіологічний розчин і тканинний активатор плазміногену (ТРА). Розчин альбуміну людини давали експериментально для зменшення дифузії рідини в легені. Пацієнт наполегливо потребував високих концентрацій вдиху кисню (80–100%) та провітрювався з низькими дихальними обсягами (4–5 мл/кг) та високим рівнем PEEP (до 12 см H2O). Незважаючи на звичайне лікування, у пацієнта було кілька епізодів після зупинки через неадекватну вентиляцію, і венозно-венозний ECMO (VV ECMO) був розпочатий 14 дня.
Спочатку пацієнту потрібно було двічі на день проводити бронхоскопічний кліренс гіпсів. Була розглянута рентгенологічна емболізація грудної протоки або хірургічна перев'язка, але її клінічний стан був занадто нестабільним, щоб це можна було зробити безпечно. Тим часом розпочато нежирне ентеральне харчування, а седативний препарат змінили з пропофолу на мідазолам, щоб зменшити вироблення хилу.
Дихальний статус пацієнта поступово покращувався із зменшенням потреби в кліренсі дихальних шляхів. 27 дня була проведена трахеостомія, і вона відійшла від ВВ ECMO на 32 день. Її повернули до нашого місцевого центру з мінімальними потребами в кисні та підтримкою тиску. Врешті-решт її відлучили від апарату штучної вентиляції легенів і через 45 днів її знекровили. Її виписали і вона залишається стабільною на нежирній дієті.
ОБГОВОРЕННЯ
Оскільки ця пацієнтка погіршувалась, незважаючи на оптимальне підтримуюче лікування, ми були змушені розглянути альтернативні методи лікування, які можуть врятувати їй життя. Хілозний характер зворотної бронхо-альвеолярної промивної рідини; переважання лімфоцитів у гіпсах (рис. 4); і короткий проміжок часу від біопсії слизової оболонки до прийому передбачав ненормальне витікання хилу з пошкодженого епітелію. Це, ймовірно, обтяжуючий фактор її зниження, якщо не основна етіологія. Дійсно, існує гіпотеза, що травма низького ступеня може спричинити розрив поверхневих лімфатичних судин при пластичному бронхіті, що призводить до просочування лімфи у просвіт бронхів [3]. Тому ми висунули гіпотезу, що зменшення споживання жиру зменшить потік хилу через пошкоджені лімфатичні судини та покращить ситуацію.
(а) Бронхіальна рідина для промивання показала альвеолярні макрофаги, епітеліальні клітини бронхів, розсіяні плоскі клітини та змішані запальні клітини, переважно невеликі лімфоцити. (b) Бронхоскопічна біопсія слизової показала слабкий змішаний запальний інфільтрат субепітеліальної строми без ознак утворення або злоякісної пухлини гранульоми. (c, d) Мікроскопічний вигляд зліпків, що показують клітинні зразки, що містять рясні лімфоцити, поряд з розсіяними альвеолярними макрофагами, еозинофілами та мізерними нейтрофілами. Лімфоїдні клітини включають змішану популяцію CD20, CD3 та CD5 позитивних клітин за допомогою імуногістохімії
Успішний результат у нашого пацієнта ми пов’язуємо з дієтичними стратегіями, що зменшують відтік лімфи, та ECMO, який використовується як мостик, коли мали місце ці ефекти. Подібні анекдотичні докази існують для лікування інших хилозних розладів (наприклад, хілоторакс). Не існує конкретних дієтичних вказівок для лікування пластичного бронхіту, і дієтичний режим був обраний відповідно до вказівок наших колег-дієтологів. Парентеральне харчування - це альтернативний метод, який запобігає ентеральному засвоєнню жиру. Інші фармакологічні втручання, про які повідомляється в літературі, включають інгаляційну рекомбінантну ДНКазу, октреотид та інгібітор рапаміцину [4]. Якщо консервативні заходи не вдаються, в деяких випадках можуть бути ефективними лімфангіографія та емболізація або торакоскопічна лігація грудної протоки за допомогою відео [5] .
Подяки
Автори висловлюють подяку доктору Пенні Райт та доктору Адаму Дакворту за надання гістологічних зображень, а також пацієнту за згоду на публікацію цієї справи.
Виноски
Конфлікти інтересів: Автори заявляють, що немає конкуруючих інтересів.
- Дієтичний жир - друг чи ворог Війна проти дієтичних настанов - Їжа та здоров'я
- Ринок харчових волокон за типом продукту (звичайний роман; розчинний нерозчинний) та застосування (харчові продукти
- Дієтичний фосфат впливає на вибір їжі, долю фосфору після прийому та ефективність
- Оцінка звичайного вживання їжі на кордоні на основі комбінації повторних 24-годинних списків продуктів харчування та
- Дієтичне втручання для зниження ваги покращує маркери субклінічного атеросклерозу та окисного стресу