Фізичні вправи та дієта посилюють окислення жиру та знижують резистентність до інсуліну у дорослих людей із ожирінням
Анотація
Тренування аеробних вправ покращує окислювальну здатність та чутливість до інсуліну у осіб молодшого та старшого віку із ожирінням та/або IGT/T2DM (8, 14, 15, 20, 36). Втручання з обмеження калорій також демонструють подібне покращення чутливості до інсуліну; проте такі висновки суперечливі, і вплив на метаболізм субстрату менш чіткий (27, 32). Основним недоліком гіпокалорійних втручань у зниженні ваги є те, що знежирена маса, яка є головним фактором використання субстрату, зокрема окислення базального жиру, також часто зменшується (8, 15). Старіння пов'язане з негативним азотним балансом, і тому дорослі люди старшого віку мають підвищений ризик розвитку саркопенії (25). Вправи сприяють підвищенню рівня синтезу білка, що може допомогти підтримувати масу без жиру у людей старшого віку. Отже, програма схуднення, яка включає фізичні вправи, може бути сприятливою для оптимального поліпшення чутливості до інсуліну та субстратного метаболізму у літньої популяції IGT із ожирінням, тим самим зменшуючи і без того високий ризик розвитку такої групи макросудинних ускладнень.
Порушення дії інсуліну в основному виникає при ожирінні через накопичення внутрішньоклітинних похідних жирних кислот. Однак адіпоцитокіни також задокументовано відіграють певну роль. Показано, що концентрації лептину в циркуляції позитивно пов’язані з масою жиру та зворотно пов’язані з чутливістю до інсуліну (33). Лептин бере участь у насиченні через сигнальний шлях гіпоталамусу (10) та в метаболізмі субстрату безпосередньо дією периферичної тканини (23). Однак було продемонстровано, що лептин може посилити окислення жиру (23), що ілюструє парадокс: не виключено, що при ожирінні може виникнути резистентність до лептину (34). У цьому дослідженні досліджували взаємозв'язок між лептином та окисленням жиру. Окрім лептину, було показано, що інший адипоцитокін, адипонектин, також пов’язаний із чутливістю до інсуліну та метаболізмом субстрату (37, 41). Отже, у цьому дослідженні також вимірювали взаємозв'язок між адипонектином та окисленням жиру.
В даний час у людей старшого віку із ожирінням, що страждають ожирінням, невідомо, чи поєднання тренувальних вправ з гіпокалорійною дієтою є більш ефективним для покращення факторів, пов’язаних із метаболічними захворюваннями, порівняно з аналогічним режимом фізичних вправ при вживанні евкалоричних макроелементів. Це дослідження служить для вивчення таких відмінностей. Було висловлено гіпотезу, що фізичні вправи та обмеження калорій покращують чутливість до інсуліну та метаболізм субстрату в більшій мірі, ніж лише фізичні вправи, як результат більшої втрати ваги, особливо маси жиру.
Предмети.
Двадцять три старших, ожирілих, IGT (глюкоза в плазмі натще> 5,6 ммоль/л та 2-годинний тест на пероральний тест на толерантність до глюкози концентрація глюкози від 7,8 до 11,1 ммоль/л) були набрані із загальної популяції для участі у 12-тижневій тренуватися вправа під час споживання або евкалорійної, або гіпокалорійної дієти. Медичний скринінг не включав осіб із захворюваннями серця, нирок, печінки, кишечника та легенів або тих, хто приймав ліки від гіпертонії, діабету чи інших захворювань, пов’язаних із ожирінням. Усі добровольці були сидячими, і вони мали вагу стабільною протягом 6 місяців до дослідження. Дослідження було схвалено Інституційною комісією з огляду, і всі суб’єкти надали письмову інформовану згоду відповідно до наших вказівок щодо захисту людей.
Втручання.
Добровольців розділили на дві групи, що відповідають індексу маси тіла (ІМТ): евкалорична група (n = 12: 4 чоловіки, 8 жінок; вік = 66 ± 1 рік; ІМТ = 34,7 ± 1,6 кг/м 2) і група гіпокалорій (n = 11: 3 чоловіки, 8 жінок; вік = 67 ± 1 рік ІМТ = 33,6 ± 1,3 кг/м 2). Обидві групи проводили аеробні вправи середньої інтенсивності під наглядом (ходьба на біговій доріжці/велоергометрія/стаціонарне веслування) при 75% максимальної потужності засвоєння кисню 5 днів на тиждень (з понеділка по п’ятницю) протягом 12 тижнів. Дієтологічні записи збирали за 3 дні до дослідження, а щотижня проводили індивідуальні консультації з питань харчування для контролю споживання калорій. Евкалоричній групі було наказано продовжувати типове споживання їжі протягом усього дослідження, тоді як гіпокалорійній групі було наказано зменшити щоденне споживання енергії на 500 ккал. Кілька антропометричних та метаболічних заходів були вжиті до та після втручання, як описано нижче, під час триденного перебування в стаціонарі в Загальному клінічному дослідницькому центрі.
Склад тіла.
Зріст вимірювали з точністю до 1,0 см без взуття. Вагу тіла вимірювали з точністю до 0,1 кг із суб’єктом, одягненим у нижню білизну та лікарняну сукню. Окружність талії вимірювали посередині між нижнім краєм ребра та гребінем клубової кістки з точністю до 1,0 см. Щільність тіла визначали гідростатичним зважуванням, а масу жиру в тілі обчислювали за допомогою рівнянь Сірі, як описано раніше (29).
Аеробний фітнес.
Кожен випробовуваний виконував додатковий тест на біговій доріжці, щоб визначити своє максимальне споживання кисню (V̇ o 2max). Швидкість встановлювалася між 2 та 4 милями/год, а нахил бігової доріжки збільшувався на 2,5% кожні 2 хв до втоми. Виділяється повітря збирали, і концентрації кисню та вуглекислого газу вимірювали за допомогою електрохімічного кисневого аналізатора (модель A S-3, Прикладна електрохімія,) та інфрачервоного аналізатора вуглекислого газу (модель LB-2, Бекман). Максимальна аеробна ємність (V̇ o 2max) була досягнута, коли було досягнуто принаймні два з наступних критеріїв: 1) плато в поглинанні кисню 2) частота серцевих скорочень в межах 10 ударів/хв від передбаченого віком максимуму та/або 3) коефіцієнт дихального обміну> 1,0. Через гострий вплив фізичних вправ на чутливість до інсуліну проміжок часу між тестом V̇ o 2max та евглікемічним затискачем завжди становив щонайменше 48 годин. Постінтервенційне тестування V̇ o 2max проводили вранці за процедурою затиску.
Метаболізм базального субстрату.
Увімкнено день 2 перебування в стаціонарі, після 12-годинного нічного голодування, випробовуваних пробуджували о 06:00 і перевозили на візках, щоб позбавити ваги та зважити, а потім вони відкинулися в напівтемрявому, термонейтральному (22 ± 1 ° C) середовищі під прозорим пластиком капюшон (Brooks Instruments, Hatfield, PA) протягом 30 хв для непрямих вимірювань калориметрії, як описано раніше (40). Молярне співвідношення споживаного кисню до виробленого вуглекислого газу було використано для визначення міри відносної кількості субстрату, що окислюється [дихальний коефіцієнт (RQ)]. Рівняння Вейра використовували для розрахунку витрат енергії в спокої (39), а швидкості окиснення субстрату розраховували за Фрейном (7). Вимірювання екскреції азоту із сечею також проводили для оцінки швидкості окислення білка (7). Коротше кажучи, сечу збирали з 06:00 до завершення заходів калориметрії. Були зареєстровані загальний об'єм і час збору, а аликвоти аналізували на вміст азоту сечовини (Roche Modular Diagnostics, Індіанаполіс, Індіана).
Чутливість до інсуліну.
Гістологія скелетних м’язів.
Статистика.
Статистичний аналіз проводили за допомогою Statview (SAS Institute, Cary, NC), і всі дані виражали як середні значення ± SE. Нормальність кожної змінної оцінювали за допомогою критерію Колмогорова-Смірнова. Змінні, що відхиляються від нормального розподілу (концентрації лептину в плазмі), були природними log-трансформованими (ln) перед статистичним аналізом. Порівняння між групами (евкалорійний та гіпокалорійний) для всіх змінних аналізували за допомогою двостороннього (група × час) повторного вимірювання ANOVA. Post-hoc тести Tukey застосовувались до значних взаємодій групи × час. Двовимірні кореляційні зв'язки використовувались для вивчення взаємозв'язку між змінами до і після дослідження (Δ) в окисленні базального жиру, затискачем М та лептином ln з іншими змінними. Крім того, окремі двовимірні аналізи також застосовувались до змінних на вихідному рівні та до змінних після втручання (наприклад, базовий лептин проти базового окислення жиру та постінтервенційний лептин проти постінтервенційного окислення жиру). Це було проведено для виявлення змін у стосунках в результаті втручання. Статистичне значення було прийнято на P 0,05).
Таблиця 1. Склад тіла, аеробна підготовленість, лептинемія та чутливість до інсуліну
Значення є середніми ± SE. Добровольці пройшли вправу аеробних фізичних вправ 12 тижнів з еукалорійною (k 1900 ккал/добу) або гіпокалорійною (,3001 300 ккал/добу) дієтою. ІМТ, індекс маси тіла; FM, жирова маса; FFM, нежирна маса; Туалет, окружність талії; V̇ o 2 max, максимальне споживання кисню під час виснажливих вправ; Clamp M, середня швидкість утилізації глюкози протягом останніх 30 хв гіперінсулінемічного еуглікемічного затиску.
* Істотні відмінності від базового рівня: P † Істотні відмінності від вихідного рівня: P ‡ Значні відмінності від базового рівня: P o 2max збільшився аналогічно в обох групах (таблиця 1; евкалорій: збільшення на 10,6 ± 3,0%, P = 0,003; гіпокалорійність: збільшення на 11,8 ± 5,7%, P = 0,04).
Чутливість до інсуліну.
Глюкоза, що метаболізується під час гіперінсулінемічного еуглікемічного затиску, була покращена на подібні кількості в обох групах (Таблиця 1; евкалорій: збільшення на 55,1 ± 19,0%, P = 0,03; гіпокалорійність: збільшення на 65,1 ± 14,4%, P = 0,001).
Лептин і адипонектин.
Концентрації лептину в плазмі крові перед втручанням були однаковими між групами (таблиця 1). Після втручання концентрація лептину знизилася в обох групах, причому більше зниження спостерігалось у гіпокалорійній групі (зниження на 31,6 ± 6,0% проти 12,2 ± 3,8%). Аналіз концентрації адипонектину в плазмі крові не виявив жодного впливу часу чи випробувань (табл. 1; P > 0,05).
Після вправи на тренуванні вправи внутрішньом’язові ліпіди (LAI,%) зменшились на 25,9 ± 12,4 та 34,3 ± 17,6% у групах еу- та гіпокалорій відповідно (двосторонній ANOVA, ефект часу P = 0,04; Таблиця 2). Групових відмінностей не виявлено (P = 0,66).
Таблиця 2. Внутрішньоклітинний ліпід
Значення є середніми ± SE. Групи досліджень описані в таблиці 1. IMCL, внутрішньом’язовий ліпід; LAI, індекс накопичення ліпідів, тобто середній відсоток площі окремого скелетного м’язового волокна, який фарбує ліпіди.
* Статистично значуща відмінність від значення попереднього втручання, P 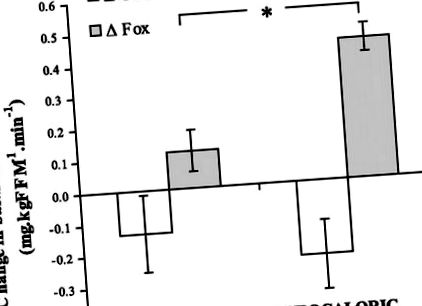
Рис. 1.Зміни метаболізму базального субстрату. Двадцять три особи старшого віку, з ожирінням і раніше малорухливими людьми з толерантністю до глюкози дотримувались 12-тижневих вправ з аеробних вправ у поєднанні з еукалорійною (1900 ккал/добу) або гіпокалорійною (1300 ккал/добу) дієтою. Значення є середніми ± SE. FFM, нежирна маса. Базове окислення жиру показало більші покращення в гіпокалорійній групі (ΔFox: *P = 0,03). Відмінностей у зміні базального окислення вуглеводів не виявлено (ΔCox: P = 0,87).
Таблиця 3. Метаболізм базального субстрату
Значення є середніми ± SE. Групи досліджень описані в таблиці 1. RQ, коефіцієнт дихання; ЕЕ, витрати енергії; Кокс, базальне окислення вуглеводів; Лисиця, базальне окислення жиру; Віспа, базальне окислення білка.
* Значні відмінності від базового рівня, *P 0,05).
Кореляційний аналіз.
Рис.2.Взаємозв'язок між внутрішньоміоклітинними ліпідами та окисленням базального жиру. Дані 2 досліджуваних груп були об’єднані для кореляційного аналізу. Дані вказують на те, що у людей похилого віку, що страждають ожирінням, малорухливими, з товщиною глюкози, зниження внутрішньоклітинних ліпідів (дельта IMCL) та збільшення окиснення базального жиру (дельта базальна лисиця) внаслідок тренувального втручання були пов’язані (р = −0,53, P = 0,04).
Рис.3.Зв'язок між лептином у плазмі крові та окисленням базального жиру. Дані 2 досліджуваних груп були об’єднані для кореляційного аналізу. Дані про концентрацію лептину в сирому плазмі відхилялися від нормального розподілу, і тому природний log (ln) трансформували для статистичного аналізу. Значення є середніми ± SE. A: у людей похилого віку, що страждають ожирінням та малорухливими людьми, не існувало зв'язку між лептином у плазмі крові та окисленням базального жиру (р = 0,05, P = 0,84). B: після 12-тижневого тренувального режиму спостерігався значний взаємозв’язок між лептином у плазмі та окисленням базального жиру (р = 0,65, P = 0,0007).
Таблиця 4. Двовимірні кореляційні аналізи
Значення - коефіцієнти кореляції продукту-моменту Пірсона (р значення) для взаємозв’язків між змінами змінних (Δ) під час 12-тижневого вправляючого тренування. Через відсутність взаємодії групи × часу у більшості змінних, передбачалося, що тренування вправи керувала змінами незалежно від споживання калорій; тому групи втручання об'єднали для кореляційного аналізу.
* Значні кореляції: P † Значущі кореляційні зв’язки: P ‡ Значущі кореляційні зв’язки: P o 2max), лептинемія, внутрішньом’язове накопичення ліпідів (IMCL) та чутливість до інсуліну (затискач M) у людей старшого віку, що страждають ожирінням, раніше не сиділи, IGT, незалежно від загального добового споживання калорій; але те, що покращення окислення базального жиру залежить від обмеження калорій на додаток до фізичних вправ. Крім того, зміни в IMCL були пов’язані з поліпшенням окислення базального жиру та лептинемії. Крім того, хоча не було встановлено, що зміни в окисленні базального жиру пов'язані зі змінами чутливості до інсуліну, позитивний взаємозв'язок між окисленням базального жиру та лептином у плазмі крові розвинувся після втручання, що свідчить про поліпшення чутливості до лептину. Ця тенденція була більш вираженою, коли на додачу до фізичних вправ проводилось обмеження калорій. Подібні висновки у молодих когорт із ожирінням опублікували Goodpaster et al. (8) та He et al. (11), який виявив взаємозв'язок між використанням жиру та чутливістю до інсуліну; тому наша робота припускає можливу вікову дисоціацію цих двох змінних.
Втрата ваги за рахунок зменшення жирової маси знижує появу системних вільних жирних кислот у кровообіг, тим самим зменшуючи доступність вільних жирних кислот до скелетної м’язової тканини (2). У інсулінорезистентних м’язів, як це виявлено у людей старшого віку з ожирінням, IGT, де окислення базального жиру порушено, це обмежить накопичення внутрішньом’язових ліпідів та інших похідних жирних кислот, які, як відомо, перешкоджають передачі сигналів інсуліну (21). Описано, що вміст IMCL підвищений у пацієнтів, резистентних до інсуліну (38), проте, схоже, ці дві змінні можуть роз'єднатись після тренувань (4). У цьому дослідженні ми демонструємо знижену постінтервенцію IMCL, яка, хоча і не пов'язана безпосередньо з чутливістю до інсуліну, була пов'язана зі змінами окислення жиру та циркуляції лептину. Було висловлено припущення, що зменшення IMCL із збільшенням швидкості базального окислення жиру зменшує залежність від вільних жирних кислот у плазмі та збільшує використання внутрішньом’язових ліпідних басейнів (31). Таким чином, з наших даних, ми можемо припустити, що зменшення IMCL у наших суб'єктів після тренувальних вправ може бути пов'язане зі збільшенням використання IMCL. Ці зміни відбуваються незалежно від споживання калорій, що свідчить про те, що фізичні вправи є ключовим компонентом втручання.
Основним повідомленням цього дослідження є те, що регулярні аеробні вправи середньої інтенсивності є рушійною силою покращення чутливості до інсуліну, коли люди старшого віку, з ожирінням та раніше малорухливими IGT дотримуються режиму фізичного навантаження та дієти. Незважаючи на більші зміни у складі тіла після втручання з обмеженим вмістом калорій, такі зміни не екстраполювали більших змін чутливості до інсуліну порівняно з евкалоричним вправою. Втрата маси жирової маси на додаток до підтримання нежирної маси має важливе значення для старших когорт. Такі зміни були продемонстровані в цьому дослідженні. Ми також зафіксували, що люди старшого віку з ожирінням, які страждають ожирінням, виявляють стійкість до лептину щодо окислення базального жиру, і що фізичні вправи покращують чутливість до лептину незалежно від споживання калорій. Це нове розуміння розуміння початку метаболічних захворювань у сидячих груп з ожирінням. Подальша робота в цій галузі є необхідною для виявлення механістичних шляхів.
Це дослідження було підтримано Національним інститутом з питань старіння AG-12834 (J. P. Kirwan) та Грантами Загального клінічного дослідницького центру MO1 RR-10732, RR-00080 та RR-018390.
СНОПКИ
Витрати на публікацію цієї статті були частково сплачені за рахунок оплати сторінок. Тому стаття має бути позначена цим «реклама”Відповідно до 18 U.S.C. Розділ 1734 виключно для зазначення цього факту.
Автори дякують волонтерам за їх надзвичайну відданість та зусилля. Ми вдячні медперсоналу/дієтологу Загального клінічного дослідницького центру, технічному/інженерному персоналу та студентам, які допомагали у проведенні дослідження та допомагали у зборі даних.
- Для людей похилого віку, які страждають на діабет, схуднення за допомогою дієти, фізичні вправи можуть поліпшити кровообіг -
- Дієта та фізичні вправи при лікуванні ефекту ожиріння від 3 втручань на резистентність до інсуліну -
- Вплив Momordica charantia на резистентність до інсуліну та вісцеральне ожиріння у мишей на дієті з високим вмістом жиру
- Шаблон журналу дієт та вправ для Excel 2013
- Депресія, дієта та фізичні вправи Медичний журнал Австралії