Захисна дія та терапевтичний індекс індраліну у неповнолітніх мавп-резусів
Михайло Васильович Васин
1 Державний науковий центр Російської Федерації - Інститут біомедичних проблем Російської академії наук, Хорошовський шлях, 76а, Москва 123007, Росія
Леонід Федорович Семенов
2 Науковий інститут медичної приматології Російської академії медичних наук, 1 Веселе, Сочі 354376, Росія
Микола Суворов
3 Центр хімії лікарських засобів, вул. Зувовська, 7, Москва, 119815, Росія
Всеволод В. Антипов
1 Державний науковий центр Російська Федерація - Інститут біомедичних проблем Російської академії наук, Хорошовський шлях, 76а, Москва 123007, Росія
Ігор Б. Ушаков
1 Державний науковий центр Російської Федерації - Інститут біомедичних проблем Російської академії наук, Хорошовський шлях, 76а, Москва 123007, Росія
Леонід Олександрович Ільїн
4 Бурназький федеральний медичний біофізичний центр, Федеральне біомедичне агентство, вул. Гамалея, 17а, Москва 123098, Росія
Борис Олександрович Лапін
2 Науковий інститут медичної приматології Російської академії медичних наук, 1 Веселе, Сочі 354376, Росія
Пов’язані дані
Анотація
ВСТУП
МАТЕРІАЛИ І МЕТОДИ
Експерименти на тваринах
Експерименти проводились на неповнолітніх мавпах-самцях і самках-резусах (Macaca mulatta) у віці від 2 до 3 років з масою тіла 2,1–3,5 кг. Середня вага тварин із нижчими та верхніми квартилями становила 2,8 (2,2–3,0) кг у контрольній радіаційній групі та 2,7 (2,2–3,1) кг у дослідній групі мавп (тих, хто отримував радіопротектор). Всіх тварин годували стандартною кормовою дієтою та питною водою. Дієта складалася з фруктів (яблука) та овочів (моркви, червоного буряка, капусти, картоплі), а також білка з курячих яєць. Евтаназія в цьому дослідженні не застосовувалась.
Це дослідження було проведено з урахуванням вимог відповідно до нормативно-правових актів про порядок проведення експериментальних робіт на тваринах, включаючи національні (Наказ Міністерства охорони здоров'я РФ № 267 від 19 червня 2003 р.) Та міжнародні етичні рекомендації щодо медичних біомедичні дослідження за участю тварин (Декларація Всесвітньої медичної асоціації, Гельсінкі, 2000).
Опромінення
Мавпи піддавались двосторонньому гамма-опроміненню всього тіла в експериментальній установці 60 Co моделі GUBE-2000 (2000 Ci з зарядом 60 Co) (Росія) у смертельній дозі 6,8 Гр (доза опромінення спричиняє 100% смертність тварин через 30 днів після опромінення = LD100/30) і потужність дози 22,8 cGy хв –1. Тварин опромінювали без наркозу. Поглинена доза в організмі (Dab) розраховувалася наступним чином: Dab = Dex × 1,137 × 0,877, де Dex = експозиційна доза опромінення в повітрі, 0,877 = коефіцієнт переходу для розрахунку поглинутої дози в повітрі від дози опромінення в повітрі, та 1,137 = коефіцієнт переходу енергії гамма-променю 60 Co 1,25 МеВ для розрахунку поглиненої дози в організмі з поглиненої дози в повітрі.
Введення ліків
Індралін (CAS 156799–03–0, Фармзащита, Федеральне біомедичне агентство, Москва, Росія) вводили мавпам в область стегна внутрішньом’язово (ім) у дозах 40, 60, 80 або 120 мг кг –1 у вигляді 2,5% розчину За 5 хв до впливу радіації. Після опромінення тварини отримували протимікробні засоби за єдиним протоколом лікування: левоміцетин (Ferein, Москва, Росія) 200 мг кг –1, що вводився перорально один раз на день у дні 1–10; пеніцилін (Biosynthes, Пенза, Росія) 150 мг кг –1 та стрептоміцин (Biochimic, Саранськ, Росія) 50 мг кг –1 м.д. один раз на день у дні 10–20. Чотири непроменені макаки отримали токсичні дози індраліну i.m. (800 та 1000 мг кг –1).
Визначення радіопротекторної дії індраліну
Радіозахисні властивості індраліну оцінювали на підставі аналізу виживання тварин протягом 60 днів після опромінення та наявності клінічних симптомів гострого променевого синдрому (ГРС). Зміни маси тіла та ректальної температури контролювали. Ми також обстежили область живота пальпацією, оцінили легеневу функцію, спостерігаючи за диханням, та візуально оглянули шкіру та слизові оболонки, включаючи ротову порожнину та анальну область. Кількість лейкоцитів, тромбоцитів, еритроцитів та ретикулоцитів, значення гемоглобіну та швидкість осідання еритроцитів (ШОЕ) визначали з периферичної крові тварин. Клінічними проявами гострого променевого ураження кишечника були діарея та напруга живота. Ці симптоми були очевидні з 5–10 днів. Під час продромального періоду спостерігали за допомогою реєстрації блювоти, діареї та рухових та поведінкових розладів протягом першої доби після опромінення. Токсичні дози індраліну базувались на клінічних ознаках отруєння та смерті тварин протягом трьох днів після лікування.
Статистичний аналіз
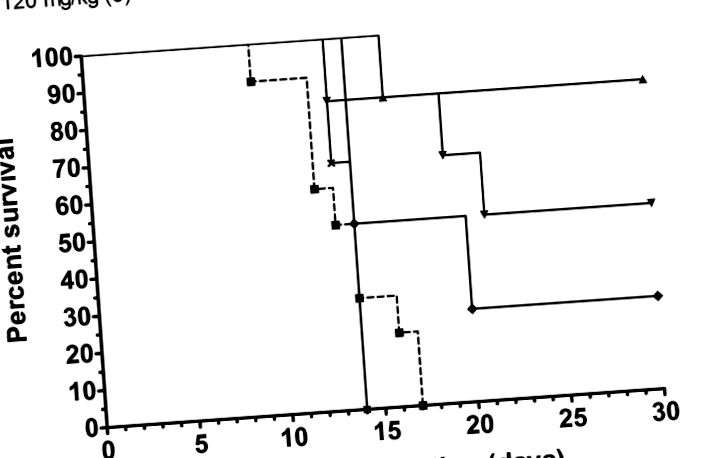
Дані виражаються як середнє значення ± стандартна помилка. Наявність радіозахисного ефекту оцінювали шляхом аналізу кривої виживання за допомогою методу Каплана – Мейєра (F-тест Кокса). Статистичний аналіз проводили за допомогою комп’ютерної програми „Statistica” версії 7. Статистичну ймовірність визначали за допомогою непараметричного U-критерію Манна – Уітні з мінімальним об’ємом вибірки три, двостороннім точним тестом Фішера та дисперсійним факторіальним аналізом . Р-значення Рис.1. 1. Після гамма-опромінення 6,8 Гр (LD100/30; потужність дози 22,8 cGy хв –1), i.m. введення індраліну в дозі 120 мг кг –1 захистило п’ять з шести мавп порівняно зі смертю всіх 10 тварин контрольної групи опромінення (Р –1), радіаційно-захисний ефект індраліну дорівнював 50% (три з шести мавп вижили). Після введення 60 мг кг –1 кожна з чотирьох мавп вижила до 60-го дня експерименту. Індралін у дозі 40 мг кг –1 був неефективним, і три експериментальні тварини загинули від ГРЗ. ED50 індраліну у мавп, які зазнали гамма-опромінення (LD100/30) протягом 30 хв, дорівнював 77,3 (63,3–94,3) мг кг –1. Індралін знижував тяжкість летальних ушкоджень у мавп до легкого перебігу ГРЗ.
Виживання мавп (Macaca mulatta) після лікування різними дозами індраліну (40–120 мг/кг) після гамма-опромінення всього тіла (6,8 Гр; LD100/30).
Зірочка позначає Р (рис. 2А). 2 А). Температура тіла суттєво не змінювалася. У підданих мавп зниження рухової активності та пригнічення інтересу до їжі. Вага тіла тварин до 7-го дня зменшилася в середньому на 10%, і це продовжувалось до тих пір, поки втрата ваги не становила 15–20%, коли настала смерть від ГРЗ (P Рис. 2 2 B).
Важкі лейкопенія та тромбоцитопенія спостерігались у зразках периферичної крові (рис. (Рис. 3А, 3 А, А, 3В). 3 Б). Геморагічний синдром призвів до різкого та глибокого зниження рівня еритроцитів та рівня гемоглобіну до 50% від початкових рівнів (рис. (Рис. 3C, 3 C, C, 3D). 3 D). У мавп з контрольної групи надір кількості лейкоцитів та еритроцитів у периферичній крові становив 0,7 (0,4–0,9) × 10 9 л –1 та 2,5 (2,1–2,9) × 10 12 л –1 відповідно до 14-го дня ARS (Додаткова таблиця S1, рис. Рис. 3A, 3 A, A, 3 3 C).
Статеві відмінності у радіочутливості мавп у цьому дослідженні не оцінювались. Середня тривалість життя померлих тварин після опромінення становила 13,4 ± 1,4 дня для самок (n = 5) та 14,8 ± 1,0 d для чоловіків (n = 5). На сьомий день після опромінення кількість лейкоцитів становила 1,53 ± 0,82 × 10 6 л -1 для жінок (n = 5) і 1,31 ± 0,23 × 10 6 l -1 для чоловіків (n = 5).
Анатомічне обстеження радіаційних ушкоджень на тілах мавп
Розтин встановив, що причиною смерті у цих тварин була ГРЗ, з важкою аплазією кісткового мозку, селезінки та лімфатичних вузлів та множинними крововиливами у слизову оболонку кишки, ендокард, перикард, серцевий м’яз та легеневу тканину; також спостерігались особливості катарального гастроентериту та геморагічного виразкового коліту. Був один випадок низько-крупозної пневмонії з гемотораксом, який був виявлений у мавпи, яка померла на 21 день АРВ після лікування 80 мг кг -1 індраліну.
Радіопротекторний вплив індраліну на клінічні прояви ГРЗ
У той час було зафіксовано помірне підвищення температури тіла та ШОЕ (рис. (Рис. 2E, 2 E, E, 3E). 3 E). Загалом, зміни кількості тромбоцитів та еритроцитів, вмісту гемоглобіну, ШОЕ та температури тіла корелювали з клінічними проявами геморагічного синдрому, асоційованого з ГРЗ, включаючи мелену (Рис. (Рис. 2C, 2 C, D та E, and3B, 3 B, C, D і E). Помітний приріст кількості лейкоцитів і ретикулоцитів спостерігався, починаючи з третього тижня. Анемія зберігалася і в той час, але на 45-й день після впливу радіації захищені індраліном мавпи одужали від обох лейкопенія та анемія. Крім того, кількість тромбоцитів зросла до 340 × 10 9 л -1 до кінця періоду спостереження (рис. 3Б).
Гостра токсичність індраліну у мавп
Толерантність до індраліну у резус-мавп оцінювали після i.m. введення радіопротектора у токсичних дозах 800 та 1000 мг кг –1. Всі три мавпи, які отримали дозу 800 мг кг –1, вижили. Одна мавпа померла через отруєння через 20 хв після введення індраліну в дозі 1000 мг кг –1. Ця тварина мала ознаки значного дихального дистрессу.
Клінічна картина дії індраліну, введеного у дозі 800 мг кг –1, була наступною. Індралін, будучи прямим альфа1-адреноміметиком [22, 23], викликав пілоерекцію в місці в’янення тварини через кілька хвилин після введення, яка зберігалася протягом 3 годин. Повторна блювота спостерігалася кожні 2 хв (шість разів) у однієї з трьох мавп. Пригнічений ефект протектора спостерігався через 5 хв після введення. Мавпи лежали на спині, зберігаючи здатність реагувати на зовнішні подразники, хоча явно демонструючи порушення рухової координації. Тварини продовжували перебувати в стані легкої сонливості з напівзакритими очима і часто були неспокійними. Через годину мавпи воліли сидіти з постійною важкою атаксією.
У той період тварини відмовлялися їсти яблука та цукор, коли триває атаксія. Важка атаксія тривала до 2 год. Мавпи сиділи згорблено, опустивши голову і закривши очі. На четверту годину їх рухи залишались незручними. Однак їх інтерес до навколишнього середовища зріс із відновленою швидкою реакцією на звуковий сигнал у формі агресивної пози. Стан тварин був задовільним через 24 год; вони брали їжу і швидко реагували на дослідника, не демонструючи атаксії. Ми спостерігали помірне зменшення маси тіла у мавп, які зазнали радіаційного опромінення, і отримували профілактичне введення індраліну в дозі 120 мг кг –1. Це зменшення ваги, ймовірно, було пов’язано зі зниженням апетиту, що є побічним ефектом високої дози радіопротектора.
ОБГОВОРЕННЯ
Індралін надає радіопротекторну дію на кровотворну тканину, кишечник, шкіру, яєчка та слинні залози [26, 27, 32–34]. Радіозахисний ефект індраліну вивчали у семи видів експериментальних тварин (мишей, щурів, хом'яків, морських свинок, кролів, собак та мавп) [21, 23, 26, 32, 35]. Індралін є прямим адреноміметичним агентом, який індукує його захисну дію через альфа1-адренергічні рецептори [22]. Радіозахисні дії індраліну пригнічуються тропафеном та хлорпромазином (які є неселективними адреноблокаторами [21, 23]), празозином (який є селективним альфа1-адреноблокатором [22]) та теофіліном (який є інгібітором циклічного аденозинмонофосфату (AMP) погіршення [21]). Радіозахисний ефект перорально введеного індраліну тривав до 1 години [35]. Встановлено, що інгібітор моноамінооксидази (МАО) іпроніазид подвоює тривалість дії індраліну [21]. Нарешті, індралін є прямим альфа1-адреноміметиком, який підвищує артеріальний тиск і зменшує частоту пульсу [35].
Захисний механізм індраліну є результатом гострої гіпоксичної дії на радіочутливі тканини. Як прямий альфа1-адреноміметик, індралін викликає зміни мікроциркуляції внаслідок звуження судин прекапілярів та одночасного збільшення споживання кисню клітинами за рахунок стимуляції тканинного дихання [21, 23–25]. Дихання 100% кисню під час опромінення зменшує радіопротекторну дію індраліну [23, 24]. Як радіопротектор, індралін, поряд з частковим захистом живота, захищає собак, опромінених потрійною летальною дозою опромінення [35]. Як пом’якшувач радіаційного впливу індралін збільшує виживання собак більш ніж на 50% при введенні після опромінення [36]. Властивість індраліну, що пом’якшує пошкодження, різко зростає в умовах нерівномірного опромінення [37].
На основі даних, представлених у цьому дослідженні, терапевтичний індекс (ТІ) радіозахисної дії індраліну у мавп був встановлений як співвідношення максимально переносимої дози індраліну та ЕД50 індраліну, введеного до впливу абсолютної летальної дози опромінення. У цьому випадку TI дорівнював 10. TI індраліну в експериментах на собаках за тих самих умов становив би трохи більше 10 [2]. На основі опублікованих даних про токсичність та радіаційно-захисні властивості аміфостину в експериментах на собаках [12, 13, 20, 38] та з використанням того самого принципу для його розрахунку було встановлено, що ТІ наближається до трьох. З огляду на високий потенціал для радіаційно-захисної ефективності аміфостину та індраліну в експериментах на собаках, останній має ТІ втричі вищий. Великий ТІ для індраліну в експериментах на собаках та мавпах обумовлений високою специфічністю та потенціалом дії радіопротекторного альфа1-адренергічного рецептора порівняно з радіопротекторами сімейства амінотіолів, які реалізують свою захисну дію за допомогою біофізичних та біохімічних процесів у клітини [2].
- Захисна дія поліфенольних екстрактів Адлаю (Coix lachryma-jobi L
- Гель для миття обличчя Шунгіт з омолоджуючим ефектом 200 мл, натуральна косметика для обличчя Шунгіт
- Чисті терапевтичні ефірні олії 7Компанія Втрата ваги; Оздоровчий
- Ефект голоду Працівниця The Baltic Times випробувала на собі метод медичного голодування
- Роза Каніна в каві Втрата ваги Органічна кава Неінвазивний терапевтичний детокс