Вплив різних методів приготування на оздоровчі сполуки брокколі *
Гао-фен Юань
1 кафедра садівництва Університету Чжецзян, Ханчжоу 310029, Китай
Бо Сонце
1 кафедра садівництва Університету Чжецзян, Ханчжоу 310029, Китай
Цзін Юань
1 кафедра садівництва Університету Чжецзян, Ханчжоу 310029, Китай
Цяо-мей Ван
1 кафедра садівництва Університету Чжецзян, Ханчжоу 310029, Китай
2 Ключова лабораторія росту, розвитку та поліпшення якості садових рослин, Міністерство сільського господарства, Ханчжоу 310029, Китай
Анотація
Досліджено вплив п’яти вітчизняних методів приготування їжі, включаючи приготування на пару, мікрохвильову піч, кип’ятіння, обсмажування та обсмажування з подальшим відварюванням (обсмажування/відварювання) на поживні речовини та зміцнюючі здоров’я сполуки брокколі. Результати показують, що всі кулінарні процедури, крім приготування на пару, спричинили значні втрати хлорофілу та вітаміну С та значне зменшення загальних розчинних білків та розчинних цукрів. Загальні аліфатичні та індольні глюкозинолати були суттєво модифіковані під час усіх процедур приготування їжі, але не шляхом приготування на пару. Загалом, випарювання призвело до найменших втрат загальних глюкозинолатів, тоді як обсмажування та обсмажування/кип’ятіння представляли найбільші втрати. Обсмажування та обсмажування/кип’ятіння - два найпопулярніші способи приготування більшості домашніх страв у Китаї - спричиняють великі втрати хлорофілу, розчинного білка, розчинного цукру, вітаміну С та глюкозинолатів, проте найкращим способом утримування поживні речовини при приготуванні брокколі.
ВСТУП
МАТЕРІАЛИ І МЕТОДИ
Рослинні матеріали
Голови брокколі (Brassica oleracea var. Italica cv. Youxiu) першокласної якості збирали рано вранці, відразу ж покривали льодом і транспортували до лабораторії протягом 10 хв. Головки брокколі очищали, видаляючи неїстівні частини, а потім подрібнювали на однорідні шматочки.
Обробні обробки
При кип’ятінні 200 г однорідних шматочків брокколі занурювали в 400 мл окропу, що моментально кипіло. Броколі злили після варіння протягом 5 хв. Пропарювання проводили шляхом суспендування 200 г нарізаної брокколі над 200 мл окропу протягом 5 хв у пароварці з кришкою. Для мікрохвильовки використовували мікрохвильову піч (LG Electronics, Tianjin Appliances Co., Ltd., Тяньцзінь, Китай) на повну потужність (1000 Вт) протягом 5 хв. 200 г брокколі поміщали в тарілку і додавали 10 мл води, щоб запобігти спаленню брокколі під час варіння. Брокколі в тарілці поміщали в мікрохвильову піч на 5-хвилинну варіння, а потім зливали. Для обсмажування соєву олію (10 мл) попередньо розігрівали до 140 ° C у воку, поміщали брокколі (200 г) і обсмажували протягом 5 хв. В кінці кожного випробування зразки зливали і змащували промокальним папером, щоб забезпечити поглинання масла, що перевищує кількість. Для обсмажування/кип’ятіння соєву олію (10 мл) попередньо розігрівали до 140 ° C у воку, поміщали брокколі (200 г) і обсмажували протягом 2 хв. Потім додали водопровідну воду (50 мл), і потім їх варили в закритому воці протягом 3 хв, а потім зливали так само, як і для обсмаженої брокколі.
Кожен процес проводився тричі рандомізованим способом для всіх п’яти способів приготування. Свіжу та зварену брокколі негайно взяли для аналізу на вітамін С. Решта матеріалів брокколі заморожували рідким N2 і зберігали в поліетиленових пакетах при -70 ° C. Частини заморожених зразків сушили ліофілізацією для аналізу глюкозинолатів.
Визначення хлорофілу
Брокколі (0,5 г) подрібнювали і екстрагували в 10 мл 80% (об/об) ацетону. Екстракт центрифугували при 1500 × g протягом 10 хв при кімнатній температурі і залишок видаляли. Загальний вміст хлорофілу визначали, реєструючи поглинання при 652 нм за допомогою спектрофотометра. Загальний вміст хлорофілу оцінювали в мг/г свіжої ваги (FW).
Визначення загального розчинного білка
Заморожені зразки (0,5 г) подрібнювали, гомогенізували в 5 мл 50 ммоль/л фосфатно-забуференного сольового буфера (PBS) (pH 7,8), а потім центрифугували при 12000 × g протягом 20 хв при 4 ° C. Вміст розчинного білка в надосадовій рідині визначали за методом Bradford (1976), використовуючи бичачий сироватковий альбумін в якості стандарту. Результати виражаються як мг розчинного білка/г FW.
Визначення загального розчинного цукру
Заморожені зразки (2,0 г) подрібнювали і екстрагували 6 мл киплячого 80% (об./Об.) Етанолу протягом 30 хв з наступним центрифугуванням при 10000 × g при 4 ° С протягом 10 хв. Процес повторювали для повного вилучення. Загальний вміст розчинного цукру визначали із застосуванням реагенту антрону та глюкози в якості стандарту (Roe, 1955). Результати виражаються як мг розчинного цукру/г FW.
Визначення загального каротиноїду
5 г квіток подрібнювали і екстрагували сумішшю ацетону та петролейного ефіру (1: 1, об./Об.) Неодноразово, використовуючи ступку та маточку, до отримання безбарвного залишку. Верхню фазу збирали і поєднували з неочищеними екстрактами після декількох промивань водою. Екстракти доводили до відомого обсягу петролейним ефіром. Загальний вміст каротиноїдів визначали, реєструючи поглинання при 451 нм за допомогою спектрофотометра. Загальний каротиноїд оцінювали в мг/100 г FW.
Визначення вітаміну С.
Вміст вітаміну С визначали згідно офіційного методу Асоціації офіційних аналітичних хіміків (AOAC) 985.33 (титриметричний метод 2,6-дихлороіндофенолу) (AOAC, 1990). Вміст вітаміну С виражається у мг/100 г FW.
Аналіз на глюкозинолат
Глюкозинолати екстрагували та перетворювали на десульфоглюкозинолати, як описано в нашому ранньому звіті (Jia et al., 2009). Аналіз високоефективної рідинної хроматографії (ВЕРХ) на десульфоглюкозинолат проводився за допомогою рідинного хроматографа в режимі Shimadzu з подвійним спектром спектрофотометра, як повідомлялося раніше (Jia et al., 2009). Ото-нітрофеніл-β-D-галатопіранозид (Sigma, США) використовували як внутрішній стандарт для аналізу ВЕРХ. Вміст окремих глюкозинолатів розраховували відповідно до опублікованих факторів відповіді (Haughn et al., 1991). Інтегрована площа піку десульфоглюкозинолатів була перетворена в молярну кількість, припускаючи, що ця сполука має молярний коефіцієнт екстинкції при 226 нм, рівний такому синігріну.
Статистичний аналіз
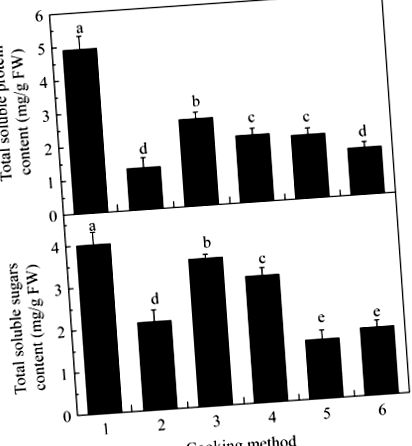
Статистичний аналіз проводили за допомогою пакетної програми SPSS версії 11.5 (SPSS Inc., Чикаго, Іллінойс, США). Дані аналізували за допомогою одностороннього дисперсійного аналізу (ANOVA), після чого проводився пост-hoc тест Данкана з великим діапазоном. Результати виражаються як середнє значення ± SD триразових зразків. Різниці вважали суттєвими на P Рис.1. 1. Вміст хлорофілу у вареній, обсмаженій/обсмаженій, обсмаженій та в мікрохвильовій брокколі зменшився відповідно на 27%, 23%, 18% та 16% (P (рис. 2). 2). Найвищий вміст загальних розчинних білків та розчинних цукрів (2,6 м/г FW та 3,5 mg/g FW відповідно) в брокколі був отриманий після приготування на пару. Найнижче утримання загальних розчинних білків спостерігалось у брокколі після кип’ятіння та обсмажування/кип’ятіння, тоді як найнижче утримання загальних розчинних цукрів було виявлено у брокколі після обсмажування/кип’ятіння та обсмажування (рис. 2). 2).
Вміст загальних розчинних білків та розчинних цукрів у брокколі, приготовленому різними методами
Вміст вітаміну С та загальних каротиноїдів у брокколі, приготовленій різними методами
Вплив варіння на загальні та окремі глюкозинолати
Вміст загального та окремих глюкозинолатів кількісно визначали у брокколі, звареній різними методами. Основними аліфатичними глюкозинолатами в брокколі були глюкорафанін, потім глюкоіберин, тоді як основними індольними глюкозинолатами були глюкобрасицин та неоглюкобрасицин (таблиця (табл. 1). 1). Глюкозинолатний профіль брокколі у нашому дослідженні відповідав попереднім звітам (Jia et al., 2009; Schreiner et al., 2006).
Таблиця 1
Глюкозинолати, виявлені в брокколі (Brassica oleracea L. var. Italica cv. Youxiu)
| Тип | Тривіальна назва | Глюкозинолатний бічний ланцюг |
| AG | Глюкорафанін | 4-метилсульфінілбутил |
| Глюкойберин | 3-метилсульфінілпропіл | |
| Прогойтрін | 2 (R) -2-гідрокси-3-бутені | |
| IG | Глюкобрасицин | 3-індолілметил |
| Неоглюкобрасицин | 1-метокси-3-індолілметил | |
| 4-метоксиглюкобрасицин | 4-метокси-3-індолілметил |
АГ: аліфатичні глюкозинолати; IG: індол-глюкозинолати
Вміст загальних аліфатичних та індольних глюкозинолатів у брокколі, зварених різними методами
Таблиця 2
Індивідуальний вміст глюкозинолату в брокколі, приготовленому різними методами
| Лікування | Аліфатичні глюкозинолати (мкмоль/г DW) | Індол-глюкозинолати (мкмоль/г DW) | ||||
| ПРОГ | IB | RAPH | ГБ | 4-мегабайт | NEO | |
| Сирий | 0,43 ± 0,03 а | 2,20 ± 0,10 а | 13,60 ± 0,30 а | 4,10 ± 0,16 а | 0,41 ± 0,02 а | 2,23 ± 0,18 а |
| Варений | 0,23 ± 0,01 b | 1,01 ± 0,09 b | 8,30 ± 0,88 b | 1,52 ± 0,23 c | 0,19 ± 0,02 кд | 1,03 ± 0,19 кд |
| На пару | 0,36 ± 0,02 а | 1,98 ± 0,03 а | 12,80 ± 0,29 а | 2,40 ± 0,11 b | 0,37 ± 0,02 b | 1,49 ± 0,17 b |
| Мікрохвильова піч | 0,20 ± 0,01 b | 1,15 ± 0,07 b | 5,10 ± 0,19 д | 1,80 ± 0,13 c | 0,20 ± 0,01 c | 1,16 ± 0,15 c |
| Смажені | 0,19 ± 0,02 до н | 1,01 ± 0,04 b | 6,10 ± 0,42 c | 1,18 ± 0,29 д | 0,16 ± 0,02 д | 0,91 ± 0,09 кд |
| Смажена/варена | 0,17 ± 0,02 c | 0,88 ± 0,03 б | 6,50 ± 0,29 c | 1,40 ± 0,30 кд | 0,17 ± 0,03 кд | 0,84 ± 0,13 c |
Повідомлялося, що кипіння спричиняло великі втрати глюкозинолатів овочів (Ciska та Kozlowska, 2001; Oerlemans et al., 2006; Volden et al., 2008b), і в цьому дослідженні ми спостерігали, що загальні аліфатичні та індольні глюкозинолати зменшувались за рахунок варіння та обсмажування/кип’ятіння (41% та 60% відповідно). Глюкозинолати - це водорозчинні сполуки, які зазвичай втрачаються під час звичайного варіння через вимивання в навколишню воду внаслідок лізису клітин (Gliszczyńska-Świgło et al., 2006). З іншого боку, термічна деструкція глюкозинолатів відбувалася при високій температурі (Oerlemans et al., 2006).
Мікрохвильова піч, а також обсмажування та обсмажування/кип’ятіння спричинили великі втрати глюкозинолатів у цій роботі. Процес приготування в мікрохвильовій печі дає суперечливі результати в літературі через різні умови, що застосовуються, такі як час, потужність та обсяг доданої води (López-Berenguer et al., 2007). Валлехо та ін. (2002) повідомили, що приготування за мікрохвильовою піччю призвело до великих втрат як аліфатичних, так і індол/ароматичних глюкозинолатів у брокколі. Висока швидкість випаровування води, що вимиває глюкозинолати з квіток брокколі, може пояснити ці значні втрати (López-Berenguer et al., 2007), що узгоджується з нашими висновками. Навпаки, Verkerk та Dekker (2004) повідомляють про збільшення (приблизно на 78%) загального вмісту глюкозинолатів у червонокачанній капусті після приготування в мікрохвильовій печі, і це може бути результатом збільшення хімічної здатності до видобутку. За наших умов приготування більше 5 хв варіння з мікрохвильовою піччю, встановленою на 1000 Вт, не дозволить інтактній мірозиназі гідролізувати глюкозинолати, оскільки це денатуралізують умови для цього ферменту. Втрата глюкозинолатів, ймовірно, відбулася через вимивання у воду (López-Berenguer et al., 2007); тому необхідно уникати додавання надлишку води під час варіння.
Song і Thornalley (2007) повідомили, що вміст глюкозинолатів в овочах Brassica, включаючи брокколі, приготовлену за допомогою обсмажування протягом 3
5 хв з попередньо нагрітим до 200 ° C рослинним маслом суттєво не змінились. На відміну від цього, обсмажування та обсмажування/кип’ятіння викликали великі втрати глюкозинолатів у брокколі в нашому дослідженні. Фермент мірозинази швидко інактивувався попередньо підігрітим кулінарним маслом до 200 ° C без будь-якого впливу на вміст глюкозинолату в брокколі. Однак кулінарне масло попередньо нагрівали і підтримували на рівні 130
140 ° C у нашому дослідженні, що може спричинити термічний розпад брокколі та/або ферментативну деградацію. Щодо них, краще попередньо нагріти олію до високої температури (200 ° C або більше), що може зменшити втрати загальних глюкозинолатів. У цьому дослідженні не спостерігалося різниці в деградації загальних аліфатичних та індольних глюкозинолатів між обсмажуванням та обсмажуванням/кип’ятінням, припускаючи, що це була стадія обсмажування при високій температурі (130
140 ° C), а не стадія кипіння, яка вимивала глюкозинолати у воду і спричиняла втрату глюкозинолатів.
Аліфатичні глюкозинолати, як правило, були більш стабільними, ніж індол-глюкозинолати, під час післязбиральних та кулінарних обробок овочів капусту (Cieslik et al., 2007; Ciska and Kozlowska, 2001; Jia et al., 2009; Rungapamestry et al., 2007; Vallejo et al., 2002). Валлехо та ін. (2002) повідомляють, що втрата загальних індольних глюкозинолатів після кип’ятіння під високим тиском, варіння на пару, мікрохвильовки та кип’ятіння під низьким тиском була вищою, ніж втрата загальних аліфатичних глюкозинолатів. У нашому дослідженні було встановлено, що швидкість втрат загальних індольних глюкозинолатів була значно вищою, ніж втрата загальних аліфатичних глюкозинолатів у брокколі після обсмажування, обсмажування/кип’ятіння, варіння на пару та кип’ятіння. Однак для мікрохвильового випромінювання спостерігався зворотний результат, після чого втрата загальних індольних глюкозинолатів була значно нижчою, ніж втрата загальних аліфатичних глюкозинолатів, на відміну від результатів, повідомлених Валлехо та ін. (2002).
Окремі глюкозинолати показали аналогічну реакцію на різні кулінарні процедури із загальними аліфатичними та індольними глюкозинолатами. Однак рівень втрат різнився серед окремих глюкозинолатів. Швидкість втрат глюкобрасицину була найвищою серед усіх глюкозинолатів, що є дещо приємним із висновком, що глюкоіберин, синігрін та глюкобрасицин демонстрували найвищі зниження після варіння (Rosa and Heaney, 1993). Однак Volden et al. (2008b) повідомили, що прогоїтрин мав винятково вищий рівень зниження порівняно з усіма іншими глюкозинолатами білокачанної капусти. Вони також виявили, що зниження проготріну, глюкоеруцину та 4-гідроксиглюкобрасицину в червонокачанній капусті було більш значним для всіх видів лікування, ніж лікування інших глюкозинолатів (Volden et al., 2008a). Ці звіти суперечать нашим результатам. Можливо, важливі відмінності в індивідуальній дифузії та гідрофільних властивостях окремих глюкозинолатів (Volden et al., 2008a). Що стосується глюкорафаніну та глюкобрасицину, то найвищий вміст було виявлено при варінні на пару. У цьому відношенні, ймовірно, що брокколі, приготована на пару, буде більше придатною для споживання людиною, ніж інші способи приготування.
На закінчення, поточне дослідження чітко показує, що поживні та зміцнюють здоров’я сполуки в брокколі суттєво впливають на домашню кулінарію. Всі кулінарні процедури, крім приготування на пару, спричинили великі втрати хлорофілу та вітаміну С. Тільки кип’ятіння та обсмажування/кип’ятіння спричинили втрату загальних каротиноїдів. Всі кулінарні процедури спричиняли значне зменшення загальних розчинних білків та розчинних цукрів, тоді як на пару було найкраще збережено. Загальні аліфатичні та індольні глюкозинолати були суттєво модифіковані всіма варінням, за винятком того, що загальні аліфатичні глюкозинолати не були модифіковані на пару. Загалом, випарювання призводило до найменших втрат загальних глюкозинолатів, тоді як смаження та обсмажування/кип’ятіння представляли найвищі. Серед окремих глюкозинолатів втрата глюкобрасицину була помітно вищою порівняно з іншими глюкозинолатами.
Пропарювання мало мінімальний вплив на хлорофіл, розчинні білки та цукри, вітамін С, а також глюкозинолати. З іншого боку, обсмажування та обсмажування/кип’ятіння, два популярні китайські методи приготування страв, спричинили великі втрати цих сполук. Щоб найкраще зберегти харчові цінності на максимальному рівні, китайські споживачі можуть обробляти брокколі шляхом варіння на пару, «дружнього» та «кращого» процесу, замість традиційного смаження або смаження/варіння.
Подяка
Ми вдячні 985-му Інституту агробіології та наук про довкілля Університету Чжецзян за надання зручності у використанні експериментального обладнання.
- Вплив мінералів на ожиріння в різних співвідношеннях трьох енергозабезпечуючих поживних речовин - PubMed
- Забезпечення збереження паростків брокколі своїх протиракових сполук - ScienceDaily
- Вплив послідовності ізокалорійних страв з різним вмістом білка на біохімічну плазму
- Вплив домашнього кулінарного процесу на хімічні та біологічні властивості дієти
- Едієти - різні плани дієти та програма схуднення