Розподіл жирових тканин передбачає виживання при аміотрофічному бічному склерозі
Єва Ліндауер
1 Неврологічний факультет Ульмського університету, Ульм, Німеччина,
Люк Дюпюї
2 Inserm U1118, Mécanismes centraux et périphériques de la neurodégénéresrescence, Страсбург, Франція,
3 Страсбурзький університет, Факультет медицини, Страсбург, Франція,
Ганс-Петер Мюллер
1 Неврологічний факультет Ульмського університету, Ульм, Німеччина,
Хайко Нойман
4 Інститут обробки нейронної інформації Університету Ульма, Ульм, Німеччина (HN),
Альберт К. Людольф
1 Неврологічний факультет Ульмського університету, Ульм, Німеччина,
Ян Кассубек
1 Неврологічний факультет Ульмського університету, Ульм, Німеччина,
Задумав і спроектував експерименти: ACL JK. Виконував експерименти: EL LD HPM JK. Проаналізовано дані: EL LD HPM JK. Внесені реагенти/матеріали/інструменти для аналізу: LD HPM HN. Написав папір: EL LD HPM HN ACL JK.
Пов’язані дані
Анотація
Передумови
бічний аміотрофічний склероз (БАС) - це нейродегенеративне захворювання, яке призводить до смерті протягом декількох років після постановки діагнозу. Гіпотрофія та втрата ваги є частими явищами, що є показником поганого прогнозу. Загальний жир і розподіл жиру у пацієнтів з БАС не вивчались.
Завдання
Нашою метою було описати вміст і розподіл жирової тканини у пацієнтів з БАС.
Дизайн
Ми провели поперечне дослідження у групі пацієнтів з БАС (n = 62, середня тривалість захворювання 22 місяці), а також здорові контролі за віком та статтю (n = 62) за допомогою методу МРТ для кількісного вивчення розподілу жиру.
Результати
Таблиця 1
| пункт | елементи керування | ALS | р-значення |
| номер включений | 62 | 62 | |
| М/Ж | 36/26 | 42/20 | 0,3527 |
| вік (роки) | 59,9 ± 12,2 | 59,9 ± 12,1 | 1000 |
| ІМТ (кг/м 2) | 25,0 ± 6,0 | 23,1 ± 3,6 | 0,0004 |
| місце початку (бульбарна/спинномозкова) | 44 спинномозкові | ||
| 10 бульбарка | |||
| 7 невідомо | |||
| тривалість захворювання (місяці) | 22,5 ± 15,3 | ||
| ALS-FRS-R | 36,3 ± 7,5 |
Вісцеральний накопичення жиру збільшується при ALS
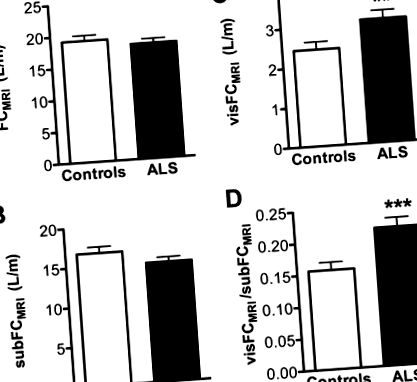
На відміну від вимірювання біоелектричного імпедансу або біохімічних маркерів, МРТ дозволяє вивчити регіональну топографію різних жирових подушечок. У хворих на БАС спостерігались помітно розширені вісцеральні жирові відкладення та подібна підшкірна жирова тканина, як показано в Фігура 1 . Послідовно кількісний аналіз показав, що FCMRI та вміст підшкірного жиру (subFCMRI) були приблизно однаковими між обома групами (p = 0,41 для FCMRI та p = 0,09 для subFCMRI, Малюнок 2A – B ), але обсяг вісцерального жиру був збільшений у пацієнтів з БАС (visFCMRI, Малюнок 2С, р = 0,0083). Таким чином, співвідношення між вісцеральними та підшкірними жировими прокладками було вищим у пацієнтів з БАС ( Малюнок 2D, р = 0,001).
Співвідношення між загальним (FCMRI, A), підшкірним (subFCMRI, B), вісцеральним (visFCMRI, C) вмістом жиру в МРТ-сканах та шкалою функціональної оцінки аміотрофічного бічного склерозу (ALS-FRS-R). вказуються значення p та відповідні коефіцієнти кореляції (r). Якщо коефіцієнт кореляції позитивний, дві змінні мають тенденцію до збільшення або зменшення разом.
Співвідношення між загальним (FCMRI, A), підшкірним (subFCMRI, B), вісцеральним (visFCMRI, C) вмістом жиру в сканерах МРТ та нахилами шкали функціональної шкали аміотрофічного бічного склерозу (ALS-FRS-R, у балах на місяць). вказуються значення p та відповідні коефіцієнти кореляції (r). Якщо коефіцієнт кореляції позитивний, дві змінні мають тенденцію до збільшення або зменшення разом.
Пацієнти чоловічої статі (A, C, E) та пацієнти жіночої статі (B, D, F) були стратифіковані відповідно до їх загальної суми (FCMRI, A, B), підшкірної (subFCMRI, C, D) та вісцеральної (visFCMRI, E, F ) вміст жиру в МРТ. вказуються значення p (log-rank). Чорна лінія представляє пацієнтів нижче медіани групи; сіра лінія представляє пацієнтів над медіаною групи.
Таблиця 2
| FCMRI | visFCMRI | subFCMRI | ||||
| ßi | р-значення | ßi | р-значення | ßi | р-значення | |
| константа (ß0) | 10,775 | 0,092 | 1,967 | 0,294 | 8.808 | 0,088 |
| ALS-FRS-R (x1) | 0,198 | 0,042 | 0,012 | 0,668 | 0,186 | 0,019 |
| стать (x2) | 3.117 | 0,049 | -1.398 | 0,004 | 4.515 | 0,001 |
| вік (x3) | 0,025 | 0,685 | 0,030 | 0,099 | −0,005 | 0,912 |
| місце початку (x4) | -1,216 | 0,514 | −0,379 | 0,492 | −0,837 | 0,577 |
Обговорення
Використовуючи автоматичний МРТ-аналіз жирових відкладень, ми показали, що розподіл жиру змінюється у пацієнтів з БАС: вісцеральний жир збільшувався незалежно від тяжкості захворювання, тоді як підшкірний жир корелював з функціональним станом та виживаністю хворих на БАС.
Перший важливий результат нашого дослідження полягає в тому, що розподіл жиру не відрізнявся між ALS та здоровими контролерами. Хоча загальний вміст жиру виявився приблизно подібним до контролю, у пацієнтів з БАС спостерігалися розширені вісцеральні жирові тканини та тенденція до зменшення підшкірних жирових тканин. Як наслідок, співвідношення між вісцеральним та підшкірним жиром зросло. Ця ситуація виявилася подібною до тієї, що виникає при метаболічному синдромі [14], [15], [16], [17], і узгоджується з непереносимістю глюкози [9] та гіперліпемією [7], [8], зафіксованою раніше в інших когортах пацієнтів . Цей ненормальний розподіл жиру, що нагадує метаболічний синдром, парадоксальним чином був пов’язаний із втратою ваги та гіперметаболізмом. [1], [2], [3],. Однак гіперметаболізм і втрата ваги, ймовірно, відображають збільшення споживання ліпідів на периферії. [23] Таким чином, пацієнти з БАС можуть виявляти роз’єднання між мобілізацією запасів ліпідів та станом метаболізму/поживності. [1], [21] Зауважимо, розподіл жиру, який спостерігається тут у людей, разюче відрізняється від тваринних моделей, які навпаки втрачають вісцеральний жир в процесі захворювання. [12].
Далі ми показали, що жирові відкладення хворих на БАС демонструють диференціальну кореляцію з клінічними параметрами. Хоча кількість вісцерального жиру не корелювало з функціональним статусом, ми спостерігали сильну позитивну кореляцію між підшкірною клітковиною, функціональним статусом та виживаністю. Недавня робота показала, що ІМТ був незалежним предиктором виживання при БАС [2], [5] та дисліпідемії, також пов'язаної з більш тривалим виживанням, [7] є сурогатним маркером збільшення ІМТ. Цікаво, що хворі на АЛС із ожирінням страждають від парадоксального зниження виживання. Хворобливе ожиріння сильно пов'язане зі збільшенням вісцерального жиру, і на основі наших результатів можна припустити, що розвиток захворюваного ожиріння, розширюючи вісцеральний жир за рахунок підшкірного жиру, може мати шкідливі наслідки для функціонального стану та виживання хворих на БАС. Підтримуючи цю останню гіпотезу, ми спостерігали збільшення виживання у пацієнтів чоловічої статі з вищим підшкірним, але не вісцеральним жиром ( Малюнок 5 ).
Наша поточна робота обмежена дизайном поперечного перерізу. Після закриття нашої бази даних, через 24 місяці після завершення МРТ, 57% пацієнтів з БАС померли. Ми спостерігали покращення виживання у пацієнтів чоловічої статі з підвищеним підшкірним жиром. Для підтвердження цього першого дослідження слід виконати подальшу роботу із збільшенням кількості пацієнтів та більш тривалим спостереженням. Крім того, наш дизайн поперечного перерізу не дозволяв контролювати еволюцію розподілу жиру з прогресуванням захворювання у даного пацієнта. Така інформація може також представляти інтерес для розвитку факторів прогнозу на основі розподілу жиру. Іншим обмеженням нашого поточного дослідження є однорідне прогресування захворювання у когорті наших пацієнтів, що послаблює спостережувану кореляцію між прогресуванням захворювання та розподілом жиру. Таким чином, дослідження, що вивчають розподіл жиру у швидких проти повільних прогресорів, є виправданими.
На закінчення ми хотіли б наголосити на тому, що мозок - це орган з другою найвищою концентрацією ліпідів після жирової тканини і що множинні захворювання мозку пов’язані із змінами метаболітів ліпідів. Наприклад, хвороба Альцгеймера тісно пов’язана з метаболізмом холестерину як генетично, так і фізіологічно. [44], [45] Проте, напрочуд мало досліджень було зосереджено на жировій тканині як джерелі та сховищі цих ключових молекул мозку. [46] Наше сучасне дослідження МРТ вказує, що жирова тканина також впливає на її топографію та потенційно її функцію при БАС, і вимагає подальших функціональних досліджень цієї ключової метаболічної тканини.
Предмети та методи
Пацієнти
Шістдесят двом пацієнтам з БАС та 62 здоровим добровольцям було проведено протокол сканування МРТ. Пацієнтів набирали в амбулаторних та стаціонарних умовах Неврологічного відділення Ульмського університету, Німеччина. Контрольна група за віком та статтю без будь-яких неврологічних/психічних захворювань чи інших захворювань була набрана за участю волонтерської групи (Університет для старих, виставка волонтерів) або подружжя пацієнтів. З дослідження були виключені засоби контролю за неврологічними чи психічними захворюваннями або протипоказання для сканування МРТ. У всіх пацієнтів діагностовано певний (23) або ймовірний (39) БАС за допомогою критеріїв Ель Ескоріал і тривалість захворювання 22,55 ± 15,25 місяців. Пацієнти з гастростомією, зниженою дихальною функцією (FVC 3 .
Підготовка даних: Гомогенізація інтенсивності та видалення зброї
У випадках, коли неоднорідності або спотворення магнітного поля або градієнта можуть спричинити неоднорідності зображення на великій площі сканування, для виправлення спотворень та підготовки набору даних до подальших операцій з даними використовувались інтерактивні функції відновлення. Оскільки озброєння часто реєстрували лише частково і не представляли інтересу для подальшого аналізу, озброєння видаляли вручну із наборів даних.
Гомогенізація інтенсивності: дифузійна фільтрація
Для гомогенізації інтенсивності в наборах даних застосовували дифузійну фільтрацію. [19].
Аналіз
Визначення підшкірного жиру проводили за допомогою алгоритму ARTIS (Адаптоване візуалізація для сегментації інтенсивності тканин), який вже виявив високу стабільність результатів. [19] Жирова тканина черевної порожнини була ідентифікована шляхом відбору всіх підключених вокселів щодо їх інтенсивності в межах попередньо визначеного діапазону ARTIS. [19].
Статистичний аналіз
Статистичний аналіз проводили з використанням Graphpad Prism 5 (GraphPad Software, La Jolla, USA). Оскільки розподіл жиру як серед пацієнтів, так і серед добровольців провалив тест на нормальність згідно з тестами Д’Агостіно та Пірсона, ми використали тест Манна-Уітні для групових порівнянь. Точний тест Фішера використовували для дихотомічних змінних, а кореляційний тест Спірмена для кореляцій. Багатовимірний регресійний аналіз був проведений/проведений за допомогою SPSS Statistics 19 (IBM, Нью-Йорк, США). Для оцінки впливу різних змінних на виживання використовували тест лог-рангу (Mantel-Cox). Наприкінці дослідження 34 пацієнти з БАС померли, а 23 ще були живі. Пацієнти, які ще живі, були піддані цензурі для аналізу виживання. Значимість була встановлена на рівні p (900K, tif)
Подяка
Ми дякуємо пацієнтам та волонтерам за це дослідження. Автори не повідомляють про розкриття інформації щодо цього дослідження.
Заява про фінансування
Автори не мають підтримки чи фінансування для звітування.
- Запалення жирової тканини сприяє зниженню маси тіла, викликаному експериментальним хронічним харчуванням
- Жирова тканина як імунологічний орган - Grant - 2015 - Ожиріння - Інтернет-бібліотека Wiley
- Запитайте експерта, як розподіл ваги впливає на швидкість кочення предмета
- Біоінк і технології біодруку для створення різнорідних та біоміметичних конструкцій тканин -
- 6 стратегій для орієнтації бічної голови на трицепс та побудови більших озброєнь