Нанокуркумін покращує показники глюкози, ліпідів, запалення та несфатину у пацієнтів із надмірною вагою та ожирінням з неалкогольною жировою хворобою печінки (НАЖХП): подвійне сліпе рандомізоване плацебо-контрольоване клінічне дослідження
Анотація
Передумови
Оскільки зміни способу життя є основними методами лікування не алкогольної жирової хвороби печінки (НАЖХП), зміна дієтичних компонентів (харчових або біоактивних) може відігравати важливу паралельну роль. Мало досліджень оцінювали вплив куркуміну на НАЖХП (переважно антиоксидантну та протизапальну дію). Ми мали на меті визначити вплив нано-куркуміну (НК) на пацієнтів із НАЖХП із надмірною вагою/ожирінням, оцінюючи показники глюкози, ліпідів, запалення, інсулінорезистентності та показників функції печінки, особливо за допомогою несфатину.
Методи
Це подвійне сліпе, рандомізоване, контрольоване плацебо клінічне випробування було проведено в Центральній лікарні нафтової компанії Тегерану. 84 пацієнти із зайвою вагою/ожирінням із НАЖХП, діагностовані за допомогою ультрасонографії, були набрані відповідно до критеріїв прийнятності (вік 25–50 років, індекс маси тіла [ІМТ] 25–35 кг/м 2). Пацієнтів випадковим чином розділили на два рівні NC (n = 42) та групи плацебо (n = 42). Втручання проводилося двома капсулами по 40 мг/день після їжі протягом 3 місяців. Рекомендували змінити спосіб життя. Загальний опитувальник, цілодобове відкликання їжі (на початку, в середині та в кінці) та короткий опитувальник з міжнародної фізичної активності (на початку та в кінці) були заповнені. Крім того, артеріальний тиск, ступінь жирності печінки, антропометрія, рівень цукру в крові натще (FBS) та інсулін (FBI), глікований гемоглобін (HbA1c), оцінка моделі гомеостазу - резистентність до інсуліну (HOMA-IR), кількісний індекс перевірки чутливості до інсуліну (QUICKI), загальний холестерин (TC), тригліцериди (TG), холестерин ліпопротеїдів низької щільності (LDL-c), холестерин ліпопротеїдів високої щільності (HDL-c), фактор некрозу пухлини-альфа (TNF-α), високочутливий c-реактивний білок (hs-CRP), інтерлейкін-6 (IL-6), трансамінази печінки та несфатин визначали на початку та в кінці.
Результати
NC у порівнянні з плацебо суттєво збільшував ЛПВЩ, QUICKI та несфатин та знижував рівень жиру печінки, трансамінази печінки, окружність талії (WC), FBS, FBI, HbA1c, TG, TC, LDL, HOMA-IR, TNF-α, hs-CRP, та ІЛ-6 (P 0,05). Після коригування для змішувачів зміни були подібні до некорегованої моделі.
Висновок
NC-добавки у пацієнтів із НАЖХП із надмірною вагою/ожирінням покращили показники глюкози, ліпідів, запалення, туалету, несфатину, трансаміназ печінки та рівня жиру печінки. Відповідно, запропонований механізм поліпшення НАЖХП з НК був схвалений збільшенням рівня несфатину в сироватці крові та, можливо, наслідком поліпшення запалення, ліпідів та профілю глюкози. Пропонуються подальші випробування ефектів нано-куркуміну.
Судова реєстрація
Іранський реєстр клінічних випробувань, IRCT2016071915536N3. Зареєстровано 02.08.2016.
Вступ
Безалкогольна жирова хвороба печінки (НАЖХП) - це відкладення тригліцеридів (ТГ) у гепатоцитах понад 5% ваги/об’єму печінки та має три ступені за даними біопсії печінки (легка: 66%). Зазвичай широко застосовуються неінвазивні методи діагностики, такі як УЗД, КТ та МРТ, що точне диференціювання між стадіями є важким. Крім того, ферменти печінки (аланінтрасаміназа [ALT] та аспартат трансаміназа [AST]) можуть бути підвищені в 1,5–2 рази вище норми. Однак у багатьох людей із запущеним неалкогольним стеатогепатитом (НАСГ) і навіть цирозом печінки нормальний рівень ферментів. Тому показники NAFLD, ймовірно, вищі, ніж повідомлялося. Симптоми часто включають втому та дискомфорт у верхній правій частині живота. Середня поширеність серед дорослих становить приблизно 30% (65–85% та 15–20% у людей із ожирінням [ІМТ ≥ 25] та без ожиріння [ІМТ
Матеріали і методи
дизайн дослідження та учасники
Комітет з етики Тегеранського університету медичних наук схвалив це подвійне сліпе рандомізоване плацебо-контрольоване клінічне дослідження як IR.TUMS.REC.1394.791. Дослідження було зареєстровано в Іранському реєстрі клінічних випробувань як IRCT2016071915536N3 08.08.2016. Учасники хворі на НАЖХП із надмірною вагою або ожирінням, скеровані до відділення сонографії Центральної лікарні NIOC у Тегерані.
Критерії включення включали НАЖХП за даними УЗД у віці 25–50 років та 25 ≤ ІМТ 2 . Критерії виключення включали вживання алкоголю протягом попереднього року, нездатність/небажання співпрацювати, інші захворювання печінки, вторинний НАЖХП, неконтрольована гіпертонія (> 140/90 мм рт.ст.), вагітність або лактація, статус професійного спортсмена, використання статинів, урсодезоксихолевої кислоти, пробіотиків, гіпотензивних засобів, куркумін-інтерактивні препарати, споживання полівітамінних/мінеральних та антиоксидантних добавок протягом попередніх 3 місяців, втрата ваги за попередні 3 місяці та не приймання більше 10% допоміжної добавки [1,2,3,4, 7,8, 9].
Рандомізація та втручання
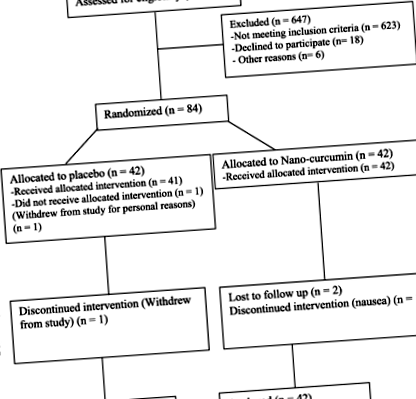
Суб'єкти були розділені на дві рівні групи методом блокової рандомізації, проведеним асистентом (NC [n = 42] або плацебо [n = 42]). Для контролю статі використовували стратифіковану рандомізацію. Співвідношення двох груп становило 1: 1. 3 пацієнти з групи NC та 2 пацієнти з групи плацебо відмовились брати участь (рис. 1).
Блок-схема учасників із надмірною вагою/ожирінням та НАЖХП
Осліплення розподілу втручання проводилось як для учасників, так і для слідчих до початку, зберігалося під час втручання та відкривалося після аналізу даних польовим працівником. Капсули NC та плацебо постачалися компанією Ексир-Нано-Сіна Компанія. Капсули були подібними за формою, розміром та кольором. синакуркумін® доза становила 80 мг/день (дві капсули по 40 мг на день, відповідно до вказівок виробника: одна капсула на сніданок, а інша на вечерю). Добавки розподілялися щомісяця, а стан відповідності оцінювався щомісяця за допомогою очної консультації та щотижня за телефоном. Відсоток відповідності добавок розраховували відповідно до середнього відсотка кількості капсул, споживаних особами будь-яких груп. Поради щодо способу життя були однаково представлені кваліфікованим дієтологом (SAJT) у лікарні.
Оцінки та вимірювання
Загальна характеристика, дієтичне споживання та фізична активність
Головний дослідник виявив пацієнтів з НАЖХП, перевірив їх критерії прийнятності, уточнив деталі дослідження та отримав інформовану згоду. Були проведені інтерв’ю для заповнення анкет, включаючи загальну анкету, цілодобове відкликання їжі (на початку, в середині та в кінці) та коротку форму IPAQ (SF-IPAQ) (на початку та в кінці). На початку випробування кваліфікований дієтолог представив рекомендації щодо способу життя [10], включаючи дотримання низькокалорійної дієти, спрямованої на досягнення зниження ваги близько 0,5–1 кг/тиждень, та збільшення фізичної активності шляхом застосування середньої інтенсивності. аеробні вправи принаймні 3 рази на тиждень протягом 30–45 хв [11].
Дієтичний статус суб'єктів визначався Дієтолог-4 програмне забезпечення, що використовує значення грам/день із цілодобового відкликання продуктів (затверджено в Ірані [12]) [12, 13].
У короткій формі опитувальника IPAQ є 7 стратифікованих питань, які визначають один із трьох загальних рівнів активності. Ця анкета раніше була затверджена в Ірані [14, 15].
Антропометричні вимірювання
Вагу (на початку та в кінці) та зріст (на початку) визначали за допомогою цифрової шкали та стадіометра (Seca® Німеччина, модель: 7551021994). ІМТ обчислювали діленням ваги в кілограмах на зріст у метрах у квадраті. Відсотки складу тіла, включаючи жир і нежирну масу тіла, вимірювали за допомогою Аналізатор біоімпедансу пристрій (Tanita®). На початку та в кінці дослідження систолічний та діастолічний артеріальний тиск отримували за допомогою ртутного манометра (Riester®) і повідомляли у мм рт. Ст. Окружність талії вимірювали в середині останнього ребра та на гребіні клубової кістки з мінімальним одягом, використовуючи нееластичну стрічку, на початку та в кінці дослідження. Забір крові, зберігання та лабораторні дослідження проводились у Центральній лікарні NIOC, Тегеран.
Вимірювання сонографії та біомаркерів крові
Ультразвукове дослідження проводив рентгенолог із використанням сонографічного апарату (General Electric (GE) ®, Модель: Voluson E8) після 12-годинного голодування, щоб зменшити потенційну людську помилку.
10 мл крові (на початку і в кінці) відбирали з периферичної вени після 12-годинного нічного голодування і центрифугували протягом 20 хв (3000 g). Показники глюкози в сироватці крові, ліпіди та трансамінази печінки оцінювали в день взяття крові. Решту сироватки заморожували і зберігали при - 80 ° C перед аналізом.
Несфатин у сироватці крові, IL-6 та TNF-α вимірювали за допомогою сендвіч-ІФА та наступних наборів: Shanghai Crystal Day Biotech Co. Ltd®; Внутрішньоаналіз CV $$ QUICKI = 1/\ зліва (\ mathit \ натще \ інсулін \ \ зліва [\ mu МО/мл \ праворуч] \ праворуч) + \ mathit \ глюкоза натще \ \ зліва [мг/дл \ праворуч] \ Великий). $$
ГОМА - ІЧ = ФБР [μIU/мл] × ФБС [мг/dl] /405.
Ліпіди сироватки крові (TC, TG, HDL-c, LDL-c), ALT, AST та HbA1c оцінювали за Аналізатор Hitachi пристрій (q17®) та конкретні набори (табл. 1).
Обсяг вибірки
За даними Chuengsamarn et al. [16], середнє значення ± SD індексів HOMA-IR у групах куркуміну та плацебо становило 3,22 ± 1,30 та 4,08 ± 1,35, відповідно. У кожній групі зразків було 42 учасника, із ДІ 95%, потужністю 80% та падінням 15%. Всього було вибрано 84 особи, які були розділені на дві рівні групи (NC та плацебо), використовуючи метод рандомізації блоків.
Аналіз даних та доступність
Було проведено управління даними, включаючи введення, безпеку, кодування та зберігання. Дані подальшого спостереження, відсутні у пацієнтів, оцінювались за допомогою аналізу модифікованих намірів для лікування (m-ITT) та методу регресійної імпутації. Для оцінки нормальності безперервних змінних та категоріальних та безперервних базових характеристик, відповідно, були застосовані тести Колмогорова-Смірнова, Хі-квадрат, Фішера Точного та t або Манна-Уітні. Дисперсійний аналіз двостороннього повторного вимірювання (TWRM-ANOVA) був використаний для обчислення ефектів часу та часу за допомогою ефектів взаємодії лікування з усіма залежними змінними. Більше того, TWRM-ANOVA був скоригований на дієтичне споживання учасниками енергії, загального жиру, насичених жирів, мононенасичених жирних кислот, вітамінів D, B1, B6 та фолатів. 95% довірчий інтервал (ДІ) та a P-значення
Результати
Риси учасника
Як показано на рис. 1 731 людина пройшла обстеження на основі їх історії хвороби. Критеріям прийнятності відповідали 108 суб'єктів, з яких 18 відмовились брати участь, а 6 не змогли взяти участь. 84 суб'єкти були рандомізовані у 2 групи та завершили перший візит. На етапі подальшого спостереження 5 суб'єктів не могли продовжувати (з особистих причин та/або подорожі; NC n = 3; плацебо n = 2). Врешті-решт, згідно з модифікованим ITT-аналізом, було проведено аналіз даних для 84 суб’єктів.
Загальні риси та рівні фізичної активності учасників наведені в таблиці 2. Більшість випробовуваних мали однаковий рівень освіти та демонстрували високий економічний статус та низькі показники фізичної активності. Обидві групи добре споживали призначені добавки. Відсоток відповідності добавок становив 95,98% у групі, що не отримувала медичну допомогу, та 97,95% у групі плацебо.
Дієтичне споживання вітаміну D на початковому рівні було більшим у групі плацебо, тоді як інші вихідні особливості між цими двома групами були подібними (таблиці 2, 3, 4).
Змінюються дієтичний статус та вимірювані біомаркери
Дієтичне споживання енергії, загального жиру, насичених жирів, мононенасичених жирних кислот, вітамінів D, B1, B6 та фолатів під час дослідження було вищим у групі плацебо (P 0,05), хоча вага, ІМТ, WC, SBP, ALT, AST, TC, LDL-c, TG, FBS, FBI, HbA1c, FM, TNF-α, IL-6, hs-CRP та HOMA-IR зменшувались, і HDL-c, QUICKI та Nesfatin значно зросли (P 0,05), але вага, ІМТ, WC, DBP, ALT, AST, TC, LDL-c, TG, FBS, FBI, HbA1c, FM, TNF-α, IL-6, hs-CRP та HOMA-IR зменшились, та HDL-c, QUICKI та Nesfatin значно зросли (P 2 та 29,7 ± 2,10 кг/м 2 у групі, що не отримує їжі, та 30,7 ± 2,35 кг/м 2 та 29,9 ± 2,53 кг/м 2 у групі плацебо. Ці середні зміни залишились незначними як для некорегованих (P = 0,2) та скориговані моделі (P = 0,3).
Як можна бачити в часі за ефектом взаємодії лікування як в некорегованій, так і в скоригованій моделях аналізу, WC, ALT, AST, TC, LDL-c, TG, FBS, FBI, HbA1c, TNF-α, IL-6, hs- CRP та HOMA-IR зменшились, а HDL-c, QUICKI та Nesfatin значно зросли серед групи, яка отримувала НС, порівняно з групою плацебо (P Таблиця 5 Зміни у вазі, ІМТ, показниках глюкози, несфатині, запальних факторах та ферментах печінки у пацієнтів із НАЖХП із надмірною вагою/ожирінням
Безпека
Пацієнти не повідомляли про побічні ефекти та побічні явища, пов’язані з лікуванням, протягом дослідження, за винятком одного пацієнта групи NC, який повідомив про нудоту.
Обговорення
Це дослідження було першим, хто оцінив вплив НК на сироваткові рівні деяких важливих факторів, пов’язаних із зайвою вагою, ожирінням та НАЖХП.
Вихідні змінні були подібними між двома групами, за винятком того, що дієтичне споживання вітаміну D було вищим у групі плацебо. Можливі причини високої подібності включають вибір єдиного центру та подібні соціально-економічні рівні учасників.
Згідно з некорегованим та скоригованим аналізом, NC (у порівнянні з плацебо) суттєво підвищував рівень ЛПВЩ, QUICKI та несфатин, а також знижував WC, ALT, AST, TC, LDL-c, TG, FBS, FBI, HbA1c, TNF -α, IL-6, hs-CRP та HOMA-IR. Зміни у вазі, ІМТ та ЧМ серед групи, яка отримує НЗ, порівняно з плацебо не були значними.
Багато досліджень показали значний вплив куркуміну (особливо більш доступних форм, таких як NC) на антропометричні вимірювання (вага, ІМТ, WC, FM) [6, 17,18,19,20,21,22,23,24,25 ]. Запропоновано різні механізми впливу куркуміну на антропометричні вимірювання, включаючи інгібування адипоцитів, ліпогенез, жирову масу та запалення, посилення ліполізу, споживання енергії [26, 27] та коричневої жирової тканини та ефекти, подібні до пробіотиків [24 ]. Крім того, ефекти несфатину на антропометрію включають зниження апетиту [28, 29], ІМТ [26, 30, 31] та WC [26]. Отже, покращення рівня туалету в цьому дослідженні може бути пов’язане з підвищенням рівня сироваткового несфатину внаслідок прийому НК.
У дослідженні щодо НАЖХП куркумін суттєво не змінив SBP та DBP [17], хоча в цьому дослідженні SBP значно зменшився у групі NC. Однак у двох оглядах повідомляється про сприятливий вплив куркуміну на артеріальний тиск [20, 27]. Запропоновано деякі механізми, включаючи поліпшення судинної реактивності [27], запалення, окисного стресу та антропометрії [20]. Дослідження впливу несфатину на артеріальну гіпертензію розділяють [32]. Причиною відсутності змін АТ може бути звичайний АТ учасників на початковому рівні.
NC у безплідних чоловіків значно збільшував загальну антиоксидантну здатність та знижував рівень CRP та TNF-α [61]. Протизапальні мішені куркуміну були згадані TNF-α, IL-1β, NF-κB, IL-6, COX2, 5-LOX, iNOS, IL-17A, IL-17F та IL-22 [23]. Також кілька оглядів показали протизапальну дію куркуміну [27, 36, 41,42,43,44,45,46,47,48,49, 62,63,64]. Запропоновані протизапальні механізми - зменшення експресії та вивільнення запальних факторів [27, 36, 39, 44, 63, 65] та активація PPARγ [66]. Крім того, зниження WC може покращити фактори запалення, включаючи TNF-α, IL-6 та hs-CRP [49, 50]. Про сприятливий вплив несфатину на запалення та окислювальний стрес повідомлялося в попередніх дослідженнях, включаючи зменшення експресії NF-κB, IL-6, IL-1β, TNF-α та апоптозу [67, 68].
Лише в двох окремих дослідженнях мармеладу і Nigella sativa впливаючи на несфатин, зизифус підвищує рівень його печінки та плазми. Повідомлялося про важливі ефекти для несфатину - втрата апетиту, антигіперглікемічні, протизапальні, нейроендокринні регулятори, зменшення жиру в організмі та метаболічна регуляція [69]. Таким чином, покращення показників глюкози [5, 54, 56,57,58], ліпідів [57, 58], запалення [67] та антропометрії [5, 54, 56], а згодом і НАЖХП, можна пояснити підвищеним рівні несфатину шляхом доповнення NC.
Деякі дослідження на тваринах куркумін/курмеричних добавок показали сприятливий вплив на жирову амінотрансферазу печінки та сироватки [61, 70,71,72,73]. У дослідженні на хворих на НАЖХП куркумін суттєво знижував рівень жиру в печінці, АЛТ та АСТ [17]. Згідно з трьома окремими оглядами, куркумін може знижувати рівень АЛТ, АСТ [39, 40], АЛП, ГГТ [40], стеатоз, запалення та АФК [21]. Однак дослідження впливу куркуми на ферменти печінки та ступінь жирності печінки у пацієнтів із НАЖХП не показало значних змін [22]. Причиною відмінностей може бути тип і форма добавки. Іншими запропонованими механізмами поліпшення ферментів печінки та жирної печінки куркуміном були зменшення запальних маркерів, синтез/накопичення ліпідів, антропометричні вимірювання [17] та окислювальний стрес [40, 70], активація PPARγ та вплив на гліколіз [73]. Також про вплив несфатину на поліпшення стеатозу повідомлялося в попередньому дослідженні на тваринах [57].
Сильні сторони спочатку вивчали вплив NC у пацієнтів із НАЖХП із ожирінням, особливо шляхом оцінки рівнів нефатину, стратифікованої блокованої рандомізації, щойно діагностованих пацієнтів з НАЖХП, які не отримували лікування, та оцінки споживання дієти та рівня фізичної активності. Однак деякими обмеженнями були відсутність біопсії печінки та вимірювання GGT та деяких згаданих факторів (PPAR-γ та ін.), Самозвіт про споживання їжі та фізичну активність, вибір конкретного центру та відсутність перевірки біодоступності та рівня НК у крові.
Висновок
Добавки NC у пацієнтів із НАЖХП із надмірною вагою та ожирінням покращили деякі маркери, пов’язані з ожирінням та НАЖХП, включаючи несфатин, QUICKI, ступінь жирності печінки, туалет, показники глюкози, ліпіди, запалення та трансамінази печінки. Вплив NC на вагу, ІМТ, FM, SBP та DBP не був значним. Відповідно, запропонований механізм поліпшення НАЖХП з добавками НК був затверджений шляхом підвищення рівня несфатину в сироватці крові та, ймовірно, згодом поліпшення запального, ліпідного та глюкозного профілів. Пропонуються подальші випробування впливу куркуміну, які включають більший обсяг зразків, більший термін дії, пацієнтів, що не страждають ожирінням, та врахування зазначених обмежень.
Скорочення
Аденозинмонофосфат-активована протеїнкіназа
- PolitiFact Advocate 70 відсотків жителів Техасу із зайвою вагою або ожирінням
- У пацієнтів із ожирінням із надмірною вагою, госпіталізованих із запаленням легенів, на 20-30% менше шансів померти, ніж
- Сім із 10 дорослих американців мають надлишкову вагу або ожиріння
- Пацієнти з надмірною вагою, що страждають ожирінням, мають більший ризик хірургічного втручання для колінного суглоба MDedge Ендокринологія
- Надмірна вага, але готовий до боротьби; Люди, що страждають ожирінням, висувають свої упереджені претензії до суду - Нью-Йорк