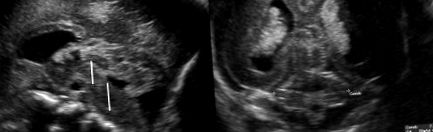
Гіпоплазія
Гіпоплазія (гіпомінералізація) - це порушення формування емалі, яке часто проявляється у поперечних лініях, ямках або інших нерівностях на поверхні емалі.
Пов’язані терміни:
- Магнітно-резонансна томографія
- Ейкозаноїдний рецептор
- DAX1
- Дисплазія
- Агенезія
- Мозочок
- Фенотип
- Психічна недостатність
- Білок
- Хромосома
Завантажити у форматі PDF
Про цю сторінку
Понтоцеребелярні розлади
Етіологія та патофізіологія
PCH успадковується аутосомно-рецесивним чином. Виділено декілька генних мутацій серед осіб, уражених PCH, включаючи TSEN54, RARS2, EXOSC3 та PCLO. 1 PCH2 є найпоширенішим підтипом PCH і спричинений мутацією TSEN54; інші TSEN-пов'язані розлади PCH включають PCH4 та 5. 4 Варто зазначити, що TSEN54, TSEN2 та TSEN34 кодують субодиниці ендонуклеазного сплайсингу рибонуклеїнової кислоти (тРНК), тоді як мутація RARS2, яка пов'язана з PCH6, кодує мітохондріальну аргініл-тРНК-синтетазу. Однак незрозуміло, чому мозочок і понс страждають найбільш сильно, на відміну від інших структур, які також значною мірою покладаються на синтез білка. 5
Мозочок: розлади та лікування
Таллі Лерман-Сагі,. Густаво Малінгер, у Довіднику з клінічної неврології, 2018
Понтоцеребелярна гіпоплазія
PCH - це група аутосомно-рецесивних нейродегенеративних розладів з пренатальним початком, що характеризується гіпоплазією мозочка та мозку (Bosemani et al., 2015) (рис. 1.21 та 1.22). Клінічні ознаки включають важку затримку мотора та розвитку та ранню постнатальну летальність. У PCH виявлено багато генетичних змін. Генетичні асоціації припускають патогенні механізми, пов'язані з дефектами фундаментальних процесів, таких як синтез білка та сплайсинг РНК (Basson and Wingate, 2013). Виявлено більше 10 підтипів ПХГ з різними фенотипами та патогенезами.
Рис. 1.21. Понтоцеребелярна гіпоплазія на 24 тижні у плода з вентрикуломегалією, дисгенезією мозолистого тіла та хвостової кісти. У серединній площині (A) верміс і четвертий шлуночок мають аномальні розміри та форму; вермієвих тріщин не спостерігається. Понс малий у порівнянні з середнім мозком; тектум погано зображений. Поперечний діаметр мозочка нижче другого процентиля (B).
Рис. 1.22. Середньосагітальні зрізи Т2-зважених магнітно-резонансних зображень плода з понтоцеребелярною гіпоплазією на 22 (A) і 30 гестаційних тижнів (ГВ) (B), а також при постнатальному спостереженні через 16 місяців (C.). (A) При 22 ГВт пон має нормальну форму; однак середній сагітальний діаметр понтію (білі двосторонні стрілки) і середньосагітальна вермієва зона (чорні стрілки) трохи нижче вікового діапазону. (B) При 30 ГВт обидва параметри все ще малі для терміну вагітності. Зверніть увагу, що при постнатальному спостереженні (C.), рострокаудальна довжина черевного моста становить приблизно таку ж довжину, як довжина рострокаудального середнього мозку, де вона насправді повинна бути вдвічі довшою (білі дужки). Також зверніть увагу на набряк глабелли (наконечники стріл) як допоміжну знахідку.
Аномалія мозочка характеризується гіпоплазією з накладеною атрофією пренатального початку. У деяких випадках ПХГ спостерігається більш серйозне ураження півкуль мозочка. На корональних знімках ця участь має вигляд «бабки», який створюється сплощеними, невеликими півкулями мозочка та відносно збереженою вермісою. Відсутність або значне зменшення популярності понтію характерно для захворювання середнього заднього мозку з пренатальним початком (рис. 1.21 та 1.22).
PCH дуже рідко діагностується внутрішньоутробно. Лейбовіц та ін. (2014b) описав два випадки, діагностовані на 29 тижні вагітності. Обидва випадки показали зменшення всіх вимірювань середнього та заднього мозку, що свідчить про те, що середній мозок також бере участь у PCH. Один із плодів мав пов'язану мікроцефалію. Грем і співавт. (2010) не вдалося діагностувати PCH типу 2 у близнюків, які проходили послідовні УЗД між 20 і 30 тижнями гестації. Автори дійшли висновку, що пренатальна візуалізація була ненадійною при діагностиці цього розладу внутрішньоутробно.
Первинні та вторинні дерматологічні розлади молочної залози
Райан Дж. Карр,. Сара Б. Петерс, у грудях (п’яте видання), 2018
Гіпоплазія та супутні захворювання
Рудиментарні (відсутні або погано розвинені) соски можуть бути присутніми як ізольований вроджений дефект або як компонент синдромів, таких як синдром шкіри голови-вуха (SEN), комплекс ектодермальної дисплазії або фокомелія Аль-Аваді/Рас-Ротшильда/Шінцеля синдроми. 13–16 Шкірні прояви можуть включати вроджену аплазію кутиса волосистої частини голови, випуклі чашеподібні або складені зовнішні вуха та рідкісні пахвові волосся; проте варіативні прояви є загальними.
Дегенеративні розлади новонародженого
Понтоцеребелярна гіпоплазія 2 типу
Чоловіча репродуктивна система1
Гіпоплазія яєчок.
Гіпоплазія яєчок є загальним станом і порушенням статевого розвитку. Яєчко менше за норму для віку тварини, і воно часто присутнє при таких розладах, як крипторхізм та інші DSD. Гіпоплазія яєчка та придатків яєчка у звичайного чоловіка є основним завданням.
За допомогою морфологічних ознак важко відрізнити гіпоплазію від атрофії яєчок. І гіпоплазія яєчок, і атрофія можуть виникати поодинці, без видимих факторів, що сприяють чи впливають; або вони також можуть бути пов'язані з вторинним ураженням або частиною якогось іншого ураження. Гіпоплазія яєчок та епідидиму (рис. 19-14, A та B) причинно пов’язана з поганим загальним харчуванням, дефіцитом цинку, специфічними генами шведської червоно-білої породи великої рогатої худоби, а також ендокринними та цитогенетичними аномаліями. Ендокринні порушення, що викликають гіпоплазію яєчок, - це такі, що знижують вироблення гіпофізом або лютеїнізуючого гормону, що, в свою чергу, впливає на вироблення тестостерону клітинами інтерстиціальних ендокринних (Лейдіга), або ФСГ гіпофізом, що стимулює живильну функцію клітин Сертолі.
Широкий спектр цитогенетичних відхилень, від транслокацій та мозаїк до недиз'юнкцій, що спричиняють полісоми статевих хромосом, призводить до гіпоплазії яєчок. Найвідоміший приклад полісомії - XXY каріотип синдрому Клайнфельтера, який спостерігається у жеребців, биків, кнурів, собак та триколірних котів. У котів синдром розпізнається у самців із триколірним, черепаховим панциром або ситцевою шерстю. Ці коти можуть бути XXY, XX/XXY або більш складними химерами або мозаїками з двома або більше Х-хромосомами та однією або декількома Y-хромосомами. Ген чорного та ген помаранчевого переносяться по одному на Х-хромосому, тому у звичайного кота-самця не повинно бути волосся обох кольорів.
Гіпоплазія яєчка теоретично може виникнути, коли кількість або довжина насіннєвих канальців зменшена або коли статевих клітин немає або їх недостатньо. Зазвичай до статевого дозрівання насіннєві канальці мають лише клітини Сертолі та сперматогонії (див. Рис. 19-14, Б). У період статевого дозрівання канальці гіпопластичних яєчок зазнають нерегулярного прогресуючого склерозу і стають колагеновими, імовірно, внаслідок одночасної дегенерації. Інтерстиціальні ендокринні клітини виявляються більш численними та скупченими.
Гіпоплазія яєчок виявляється лише після статевого дозрівання. Одностороння гіпоплазія зустрічається частіше, ніж двостороння гіпоплазія, але ця різниця у поширеності може бути відображенням відносної легкості розпізнавання різниці в розмірах, коли нормальний контралатеральний яєчко доступний для повного порівняння. Односторонню гіпоплазію важко пояснити, оскільки більшість причин, як видається, діють системно і тому повинні мати двосторонній ефект.
Археологічне дослідження
Тім Д. Уайт,. Пітер А. Фолкенс, в Остеологія людини (третє видання), 2012
25.8 Фізіологічний стрес
Зубні гіпоплазії - це неспецифічні маркери зупинки росту в зубах, що свідчать про періодичність та інтенсивність стресу (глава 19). Дві третини досліджуваних виявили принаймні одну гіпоплазію, зосереджену у віці 3-4 років. Загалом, серія Стілвотер показала відносно низький рівень поширеності гіпоплазії порівняно з іншими популяціями. Лише 16% осіб виявляли запалення надкістя, переважно великогомілкової кістки. Це також було низьким рівнем щодо більшості інших північноамериканських фуражних серій. Хоча стрес не був серйозним, він був присутній на помітному рівні. Дослідники припускають, що вузькі гіпоплазії та дані про кісткову масу свідчать про те, що популяції Стілвотер страждали від епізодичного харчового стресу.
Гепатобіліарна система та екзокринна підшлункова залоза1
Гіпоплазія підшлункової залози
Гіпоплазія екзокринної підшлункової залози у телят виникає епізодично. Ендокринна тканина підшлункової залози в нормі. Грубо кажучи, орган невеликий, блідий і може виглядати лише у вигляді невеликих стержків біло-кремової тканини в брижі. Мікроскопічно ацинарна тканина присутня, але дефіцитна, організована в невеликі скупчення клітин. Багато клітин погано диференційовані і не мають гранул зимогену. У уражених телят є клінічні ознаки екзокринної недостатності підшлункової залози.
Розрізнення між атрофією та гіпоплазією може бути важко визначити, оскільки обидва процеси призводять до аномально малого органу зі зниженою функцією. Клітини гіпопластичної екзокринної підшлункової залози зазвичай не містять ліпофусцину, який можна побачити в атрофічних клітинах.
Нервово-м’язові розлади у новонароджених
Ніранджана Натараджан, Крістіан Іоніта, у хворобах Евері у новонародженого (десяте видання), 2018
Понтоцеребелярна гіпоплазія плюс спінальна м’язова атрофія
Понтоцеребелярна гіпоплазія (PCH) - гетерогенна група спадкових розладів, що розділяють гіпоплазію або атрофію мозочка та мозку. Інші аномалії ЦНС є загальними. PCH типу 1 має як відмінні риси м’язову слабкість та гіпотонію, спричинену хворобою рухового нейрона. Наразі визначено, що мутації у трьох генах спричиняють PCH типу 1: VRK1, EXOSC3 та EXOSC8 (Renbaum et al., 2009; Wan et al., 2012; Boczonadi et al., 2014). Всі успадковуються за аутосомно-рецесивним малюнком. Хоча ступінь тяжкості та вік початку захворювання різняться, у багатьох з цих пацієнтів у неонатальному періоді спостерігається гіпотонія, слабкість, контрактури та дихальний дистрес, а також енцефалопатія. Виживання коливається від кількох місяців до декількох років. Менеджмент підтримує. Генетичний діагноз важливий для планування сім'ї.
Статеве дозрівання
Гіпоплазія надниркових залоз Congenita
AHC, що характеризується первинною наднирковою недостатністю та HH, є Х-зчепленим рецесивним розладом через мутації DAX-1 (дозочутливий реверс статі, AHC-критична область Х-хромосоми, ген 1, який також відомий як NROB1 ) ген, розташований у Xp21.1. При AHC розвиток плодової зони кори надниркових залоз під час внутрішньоутробного розвитку та її регрес протягом першого року постнатального життя відбуваються нормально. З іншого боку, доросла зона кори надниркових залоз не розвивається. Таким чином, симптоми недостатності надниркових залоз при AHC, як правило, проявляються лише після віку 6-8 тижнів, і уражені особи чоловічої статі можуть проявлятись у грудному або дитячому віці з первинною недостатністю надниркових залоз. Може виникнути затримка адренархе.
Крім того, може виникнути повна або часткова ГХ. HH відображає поєднання непослідовної секреції гіпоталамусу GnRH та/або аномальної реакції гіпофіза на GnRH. 595 Ізольований НГ через мутації NROB1 може рідко виникати за відсутності надниркової недостатності або сімейного анамнезу гіпогонадизму. У гетерозиготних самок може бути затримка статевого дозрівання, але вони мають нормальну фертильність. 595
Ген NROB1 кодує рецепторний білок, що експресується в гіпоталамусі, гіпофізі, надниркових залозах і статевих залозах. Оскільки досі для рецептора не ідентифіковано жодного ліганду, він класифікується як ядерний рецептор-сирота. Завдяки своєму домену репресії транскрипції С-кінця білок пригнічує транскрипцію багатьох генів, що беруть участь у метаболізмі стероїдних гормонів. Більшість мутацій виявлені у пацієнтів з кластером AHC в області, що кодує С-кінцевий білок. 596 Мутації в цій області Х-хромосоми можуть бути частиною сусіднього синдрому делеції гена, який включає дефіцит гліцеролкінази та м'язову дистрофію Дюшенна.
Розлади надниркової залози
Гіпоплазія надниркових залоз Congenita
AHC, рідкісне сімейне захворювання, при якому кора надниркових залоз зупинила розвиток, зустрічається приблизно у 1 із 12500 пологів (Jones et al, 1995; Laverty et al, 1973). Розлад може проявлятися як чотири клінічні форми первинної надниркової недостатності: (1) спорадична форма, пов’язана з гіпоплазією гіпофіза; (2) аутосомно-рецесивна форма з чітко вираженою мініатюрною морфологією надниркових залоз у дорослих, що характеризується невеликими залозами з постійною зоною кори, але зменшеною зоною плода (генетична основа рецесивної форми AHC невідома); (3) X-пов'язана цитомегалічна форма, асоційована з гіпогонадотропним гіпогонадизмом; та (4) Х-пов'язана форма, пов'язана з дефіцитом гліцеролкінази та м'язовою дистрофією Дюшенна (Bartley et al, 1982). Мутації в DAX1 відповідають за обидві X-пов'язані форми.
- Сільське господарство комах - огляд тем ScienceDirect
- MacConkey Agar - огляд тем ScienceDirect
- Мальтодекстрин - огляд тем ScienceDirect
- Lactobacillus - огляд тем ScienceDirect
- Герпетичний стоматит - огляд тем ScienceDirect