Гіперамонемія: що потрібно знати сечовину: повідомлення про тяжку важку нециротичну гіперамоніємічну енцефалопатію та огляд літератури
Рубі Упадхяй
1 Відділ неврологічних наук, Медичний центр Університету Раша, 1725 West Harrison Street, POB Suite 1121, Чикаго, IL 60612, США
Томас П. Блек
2 Медичний коледж Rush, Медичний центр Університету Раша, 600 S. Paulina Street, Чикаго, штат Іллінойс, 60612, США
Катаріна М. Бусл
3 Департамент неврології, Відділ нейрокритичної допомоги, Університет Флориди, Інститут мозку Мак Найт, кімната L3-100, 1149 Ньюелл-Драйв, Гейнсвілль, Флорида 32611, США
Анотація
Призначення. У 66-річного чоловіка, який страждав комою, було виявлено важку важку гіперамонемію та діагностовано пізній розлад циклу сечовини. Лікувався успішно і повністю вилікувався. Методи. Ми повідомляємо про новий випадок нециротичної гіперамонемії та оглядаємо літературу на цю тему. Вибрана література для огляду включала англомовні статті про гіперамонемію з використанням пошукових термінів „гіперамонемічна енцефалопатія”, „нециротична енцефалопатія”, „печінкова енцефалопатія”, „розлади циклу сечовини”, „дефіцит орнітин-транскарбамілази (OTC)” та „ фульмінантна печінкова недостатність ”. Результати. Представлено унікальний випадок ізольованої гіперамонемії, діагностованої як пізній дефіцит безрецептурних препаратів. Наявні дані про гіперамонемію організовані для вирішення питань патофізіології, клінічної картини, діагностики та лікування. Звіт про справу обговорюється в контексті оглядової літератури. Висновок. Пізній дефіцит безрецептурних препаратів із серйозною гіперамоніємічною енцефалопатією та обширним корелятивним зображенням може бути повністю зворотним, якщо його негайно визнати та агресивно лікувати.
1. Передумови
Аміак - це високопотужний нейротоксин, добре відомий своїм впливом на печінкову енцефалопатію [1]. Будь-який випадок гострого зміненого психічного стану повинен викликати розгляд гіперамонемії як потенційної причини. При виявленні гіперамонемії необхідно визначити етіологію її накопичення для керівництва лікуванням. Хоча гіперамонемія у дорослих у 90% випадків пов’язана з важкими, часто циротичними, захворюваннями печінки [2], збільшення виробництва аміаку або зменшення виведення аміаку є однією з альтернативних етіологій гіперамонемії [1]. Усвідомлення гіперамонемії при відсутності важких захворювань печінки може призвести до швидкого діагностування та лікування.
Ми представляємо випадок гострої важкої нециротичної гіперамонемії та розглядаємо її патофізіологічні, діагностичні та лікувальні міркування.
2. Презентація справи
66-річний керівник бізнесу чоловіка з анамнезом гіпертонії, цукрового діабету та переривчастого синуситу був переведений до нашого центру вищої медичної допомоги для прогресуючої енцефалопатії та занепокоєння з приводу несудомного епілептичного статусу.
За три тижні до прийому йому призначили 10-денний курс левофлоксацину при гаданому синуситі. Оскільки кашель і післяносові крапельниці не покращувались, його лікували двома курсами метилпреднізолону на додаток до левофлоксацину і згодом кларитроміцину. За два дні до виступу у нього з’явилися головні болі та тиск у пазухах, він скаржився на „відчуття відчуття”, біль у епігастрії та сухість. Вночі перед презентацією він часто прокидався протягом ночі з прогресуючою розгубленістю. У пацієнта не було лихоманки, ознобу та поту. Його сім'я повідомляла про історію тривоги, панічних нападів, клаустрофобії та спалахів гніву, причому останній помітний спалах стався приблизно 6 місяців тому. Слід зазначити, що колеги знайшли на столі пацієнта колекцію різних безрецептурних вітамінів та харчових добавок.
З огляду на дедалі більшу плутанину та хвилювання, пацієнта доставили до іншої лікарні, де він поступово ставав більш обтяженим, що вимагало інтубації для захисту дихальних шляхів. Він емпірично розпочав лікування ванкоміцином, цефтріаксоном та ацикловіром з приводу інфекційного менінгоенцефаліту. Аналіз ліквору виявив підвищений вміст загального білка в дозі 53 мг/дл, глюкозу 160 мг/дл (глюкоза в сироватці крові: 240 мг/дл), відсутність плеоцитозу (1 лейкоцити/мм 3), негативний показник VDRL ліквору, негативний вірус IgM та IgG західного нілу, негативний антиген криптококів, а також негативні культури грибів та бактерій. Внаслідок розвитку зубного шліфування та занепокоєння субклінічною судомною активністю була проведена рутинна електроенцефалограма (ЕЕГ), яка не виявила ніякої судомної активності, однак результати виявилися відповідними глобальній мозковій дисфункції. Його розпочали з фенітоїну, а згодом - з леветирацетаму. МРТ головного мозку показала хронічну легку гіперінтенсивність перивентрикулярної білої речовини, але гострих результатів не виявлено. Він був переведений до нашого центру вищої медичної допомоги 3-го дня лікарні через стурбованість несудомним епілептичним статусом.
Під час огляду йому було проведено інтубацію та механічну вентиляцію без будь-яких ненормальних загальних фізичних висновків. Під час неврологічного обстеження він був у коматозному стані, з неушкодженими рефлексами стовбура мозку та розгиначем, що поставив на всіх кінцівках центральну стимуляцію. Початкові лабораторні роботи були помітними для нормальної функції печінки, аміаку в сироватці крові 120 мкг/дл (контрольний діапазон 65–107 мкг/дл) та негативної панелі гепатиту, а також респіраторного алкалозу. Повторний аналіз ліквору показав 3 лейкоцити/мм 3 (76% нейтрофілів), 1 еритроцити/мм 3, молочна кислота 2,6 мекв/л, загальний білок 28,5 мг/дл та негативна ПЛР вірусу простого герпесу, а також негативна ентеровірусна панель та ацикловір було припинено. Лікування лактулозою було розпочато, але сироватковий аміак швидко піднявся до 494 мкг/дл протягом декількох годин після прибуття до нашої лікарні. Були додані рифаксимін та L-карнітин, і було розпочато новий гемодіаліз.
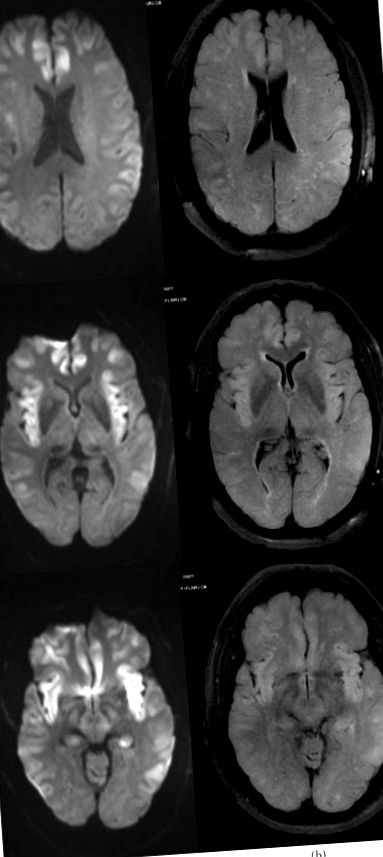
МРТ головного мозку в день передачі показала великі ділянки обмеженої дифузії з асоційованою гіперінтенсивністю FLAIR, що включає двосторонні скроневі частки та двосторонні островні, двосторонні лобові та тім’яні області в кортикальних та підкіркових областях, а також дифузне легке відшарування мозкових борозен (Рисунок 1), не посилюючи ураження. Безперервна електроенцефалограма (cEEG) протягом 96 годин демонструвала безперервне, нерегулярне, загальне уповільнення низької напруги (рис. 2); однак періодично спостерігаються посмикування обличчя та губ не мали електрографічного кореляту на cEEG. Результати МРТ щодо симетричної участі сірої речовини у вищезазначених областях, а також за відсутності гіпоксично-ішемічної інсультної та судомної активності, були визнані найбільш відповідними гіперамоніємічній енцефалопатії.
МРТ головного мозку ((а) послідовність DWI, (б) послідовність FLAIR) на 3-й день після презентації, показуючи великі ділянки обмеженої дифузії з асоційованою гіперінтенсивністю FLAIR, що включає двосторонні скроневі частки, двосторонні островні, двосторонні лобові та тім’яні області в кортикальній та підкіркових областях і дифузному слабкому відшаруванні мозкових борозен.
- Кето-дієта 10 речей, які ви дійсно повинні знати (і, мабуть, не знайте; t)
- Періодичне голодування, ВСАА та нарощування м’язів - що потрібно знати, що порушує м’язи
- Переривчастий піст, що потрібно знати; доктор
- Переривчасте голодування Що потрібно знати онкологічному центру доктора медицини Андерсона
- Дієта макросів - все, про що потрібно знати