Чи менше їжі змушує вас жити довше і краще? Оновлення щодо обмеження калорій
Анна Пікка
1 Кафедра геріатрії, неврології та ортопедії, Католицький університет Медичної школи Святого Серця, Рим
Віто Пеше
2 Кафедра біологічних наук, біотехнологій та біофармацевтики Університету Барі, Барі, Італія
Анжела Марія Серена Лецца
2 Кафедра біологічних наук, біотехнологій та біофармацевтики Університету Барі, Барі, Італія
Анотація
Складність старіння важко вловити. Однак, крім специфічних для тканин особливостей, загальний процес старіння характеризує структурно-функціональне прогресивне занепад цілого організму, що призводить до смерті, якому часто передує фаза хронічної захворюваності. Отже, мета досліджень вчених у цій галузі перейшла від пошуку стратегій, здатних продовжити тривалість життя, до тих, що забезпечують здорове старіння, пов’язаних із більш тривалим терміном життя, який називають „тривалістю здоров’я”. Процес старіння є пластичним і може регулюватися різними механізмами, включаючи дієтичні та генетичні втручання. На сьогоднішній день найнадійнішим підходом, ефективним для запобігання клітинним маркерам старіння, є обмеження калорій (CR). Тут, після попередньої презентації основної дискусії, яка виникла у CR, ми коротко оглянули останні результати лікування CR на людях. Ми також надали оновлення про молекулярні механізми, задіяні CR, та вплив на деякі вікові клітинні маркери. Нарешті ми розглянули низку перевірених CR-міметиків і завершили оцінку майбутніх застосувань такого дієтичного підходу.
Вступ
Природний і багатофакторний процес старіння впливає на всі організми. Хоча вони мають специфічні для тканини особливості, ознака прогресуючого структурного та функціонального занепаду з настанням віку, що в кінцевому підсумку призводить до смерті, одностайно поділяється. Часто досвід життя людей похилого віку робить їх безцінним резервуаром мудрості для молодих людей. Однак негативні корелятивні фактори старіння (наприклад, фізичний та когнітивний спад) роблять таких людей похилого віку поступово менш незалежними в самоокупності та більше потребують підтримки з боку суспільства.
Постійне «посивіння» західних країн вже призвело до великого економічного соціального тягаря, оскільки продовження тривалості життя, досягнуте в останні десятиліття, часто супроводжувалось хронічністю вікових захворювань. Це вказувало на необхідність переформулювати мету збільшення тривалості життя на здорове старіння, пов'язане з більш тривалим терміном життя, що називається "тривалість здоров'я" .1 Багато досліджень показали, що старіння не є унікальною причиною, тоді як безліч механізмів налаштовують цілий процес старіння.2. Завдяки новаторській роботі, проведеній над моделлю Caenorhabditis elegans від Kenyon та співавт., стало ясно, що процес старіння є пластичним і здатний прискорити або послабити за допомогою ряду дієтичних та генетичних втручань. шлях до втручання у спосіб життя, спрямований на сприяння здоровому старінню шляхом запобігання або затримки вікових дисфункцій.
На думку кількох авторів, 2,4–6 успішний підхід до здорового старіння повинен мати можливість протидіяти наступним дев’яти клітинним маркерам старіння: 1) ерозія теломер, 2) епігенетичні зміни, 3) виснаження стовбурових клітин, 4) клітинне старіння, 5) дисфункція мітохондрій, 6) нестабільність геному, 7) дисбаланс протеостазу, 8) порушення чутливості до поживних речовин та 9) аномальна міжклітинна комунікація. На сьогоднішній день найефективнішим втручанням, спрямованим на запобігання згаданим клітинним маркерам старіння, є обмеження калорій (CR), яке передбачає введення збалансованої, збагаченої поживними речовинами дієти, що зменшує споживання калорій на 20–40% без недоїдання. 7 CR має суттєвий ефект (у два-три рази), подовжуючи як середню, так і максимальну тривалість життя у гризунів, і запобігає або затримує початок різних вікових захворювань, таких як ожиріння, діабет типу 2, нейродегенерація, кардіоміопатія та рак .8
Тут, після попередньої презентації основної дискусії, яка виникла у CR, ми коротко оглянули останні результати лікування CR на людях. Ми також надали оновлення про молекулярні механізми, задіяні CR, та вплив на деякі вікові клітинні маркери. Нарешті ми розглянули низку перевірених CR-міметиків і завершили оцінку майбутніх застосувань такого дієтичного підходу.
CR: питання про справжню причину
Результати лікування CR у людини
Результати трьох тривалих довготривалих досліджень на приматів вказують на збільшення тривалості здоров'я у тварин, які отримували CR.33–36. Вплив, що опосередковується CR, на профілактику захворювань та тривалість життя ще не з’ясований, але корисні наслідки CR на метаболічні та молекулярні процеси у людини адаптації вже широко проаналізовані. Найбільш ретельним і розширеним оглядом результатів, отриманих від різних видів схем CR, застосованих до людей, є нещодавній аналіз Моста та співавт.
Короткотермінові втручання в CR у людей
Довготермінові втручання в організм людини
В даний час лише збір даних, записаних від членів Товариства обмеження калорійності, які наклали на себе режим важкого ХР з оптимальним харчуванням (КРОН), вважаючи продовженням цього способу здорового життя, дає прямі докази того, що ХР може вплинути на процес старіння у людини. Ці дуже худорляві чоловіки та жінки (індекс маси тіла 19,7 ± 1,8 кг/м 2) добровільно обмежували споживання калорій (1800 ккал/добу) в середньому протягом 15 років і споживали
CR: ефекти та механізми
CR має плейотропну дію, і, покращуючи різні метаболічні шляхи, він приносить користь для всього організму. Зокрема, деякі вказівки, що випливають із ретельного розслідування дії протидії CR, стосовно вищезазначених клітинних маркерів старіння, будуть коротко викладені в цьому параграфі, тоді як більш детальне обговорення конкретних механізмів, що беруть участь, буде розроблено в наступні параграфи.
Геномна нестабільність та епігенетичні зміни
Типовими віковими змінами є укорочення теломерів та високий рівень пошкодження ДНК (як на ядерному, так і на мітохондріальному рівні), включаючи мутації, розриви ДНК та хромосомні перебудови. Зі старінням здатність до відновлення ДНК зменшується, спричинюючи нестабільність геному.57 CR позитивно впливає на механізми репарації ДНК та теломер, сприяючи тим самим геномній стабільності та здоровому довголіття.58 Однак геном не є унікальним у формуванні клітинного гомеостазу, здоров’я та старіння, оскільки “епігенетика” розкрила механізми, що регулюють експресію генів і безпосередньо впливають на захворювання/фенотипи, не змінюючи послідовності ДНК. Епігенетичні мітки можна додавати/видаляти на гістонах або самій ДНК, модулюючи ремоделювання хроматину та експресію генів відповідно до різних екологічних сигналів.59 Існують деякі клітинні шляхи, які здатні відчувати поживні та/або енергетичні рівні, а також впливати на процеси, такі як епігеном ремоделювання, експресія генів, активність білка та цілісність органел.2 Такі шляхи глибоко залучені до модуляції старіння та вікових захворювань та до опосередкування корисних ефектів CR, що сприяють балансу протеостазу, стабільності геному та виживанню стовбурових клітин.60 Однак усі CR механізми ще не з’ясовані.
Дисбаланс протеостазу
Ще одна ознака клітинного старіння пов’язана з вирішальною функціональною роллю, яку виконують білки всередині клітин, де ці молекули інтегрують усі фізіологічні шляхи. Отже, стабільність білків (протеостаз) вказує на захист структури та функції білка від навколишнього середовища та внутрішніх стресових факторів, що діють клітиною. Вразливість у протеостазі корелює з віковими змінами та рівнем довголіття серед видів.61 Складна мережа протеостазу, що включає синтез білків, активність шаперонів, аутофагію, реакцію розгорнутого білка та шлях убіквітин-протеасома, протидіє всередині клітин та мітохондрій, білок неправильне згортання та розгортання, таким чином, забезпечуючи регулярний білковий оборот.62 Фактично, CR, здається, пов’язаний із збільшенням відповідних шаперонів та аутофагічних медіаторів, активних у контролі якості білка та видаленні дисфункціональних білків та органел.
Дисфункція мітохондрій, окисне пошкодження та порушення зондування поживних речовин
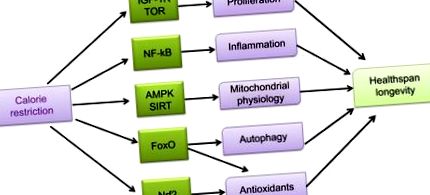
Обмеження калорій впливає на різні клітинні шляхи та індукує реакції всього організму, що призводить до більш ефективного метаболізму, більш високого захисту від клітинних пошкоджень та активації механізмів ремоделювання, тоді як менш ефективні метаболізм та синтетичні шляхи блокуються. CR інгібує процеси, пов'язані з проліферацією клітин та гліколізом, блокуючи рецептор-залежні шляхи IGF-1 та TOR-залежну діяльність. CR проявляє протизапальну дію, пригнічуючи активність ядерного фактора-kB (NF-kB). CR також зменшує вироблення АФК та збільшує біогенез мітохондрій через різні шляхи (AMPK, сиртуїни та eNOS), що призводить до поліпшення міохондріальної фізіології. CR-індукована активація FoxOs передбачає відновлення аутофагії та мітофагії та підвищену експресію антиоксидантів. CR також викликає активацію ядерного фактора (одержуваного еритроїдами 2), як 2 (Nrf2), що збільшує експресію мітохондріальних та клітинних антиоксидантних ферментів. Будь-який із цих процесів бере участь у зростанні, пов’язаному з CR, для покращення тривалості здоров’я та довголіття.
Скорочення: IGF-1, інсуліноподібний фактор росту-1; TOR, мішень рапаміцину; AMPK, AMP-залежна кіназа; FoxOs, білки форчхеда; eNOS, ендотеліальна синтаза оксиду азоту; АФК, активні форми кисню.
Управління активними видами кисню (АФК), перекисним окисленням ліпідів та мітохондріальною придатністю
CR: внесок генетики та епігенетики довголіття
Сіртуїни
Шляхи IGF/TOR/FoxO та APMK
Молекулярні маркери старіння, що беруть участь у плейотропних ефектах обмеження калорій. Кілька маркерів, що характеризують старі клітини, позначаються ураженими молекулами або функціями. У ядрі старіння передбачає наступне: ерозія теломер, геномна нестабільність та епігенетичні зміни (про що свідчить метилювання [m] гістонів H [Hm] та ДНК [DNAm] або ацетилювання [ac] гістонів [Hac]) із залученням сиртуїни та інші модифікуючі ферменти. У мітохондріях вікова дисфункція мітохондрій призводить до зменшення продукції АТФ та збільшення присутності АФК. У цитоплазмі віковий дисбаланс протеостазу викликає аномальний обмін білка з функціональними наслідками. У цитоплазмі старіння також впливає на інші шляхи (наприклад, mTOR, IIS, AMPK, сиртуїни, FoxOs) з подвійним впливом, а саме на метаболізм, а також на ремоделювання хроматину та регуляцію експресії генів, спричинюючи порушення чутливості поживних речовин/енергії, що призводить до різних зміни, також через взаємні взаємозв'язки.
Скорочення: SIRT, sirtuin; FoxOs, білки форчхеда; АТФ, аденозинтрифосфат; АФК, активні форми кисню; AMPK, AMP-активована протеїнкіназа; IIS, інсулін/інсуліноподібний фактор росту-1 сигналізація; mTOR, мішень для ссавців рапаміцину.
Запалення та CR
Старіння також характеризується станом відповідного запалення, продемонстрованим віковим зростанням кількох прозапальних факторів, включаючи TNF-α, інтерферон-γ, IL-1β та IL-18.141–143. Крім того, індукція такого хронічного запалення під час старіння може сприяти вікове підвищення окисного стресу, що також, як видається, збільшує частоту вікових захворювань.144,145 Ще однією особливістю старіння з патологічними наслідками є збільшення виробництва молекулярних моделей, пов'язаних з небезпекою, що виникли через накопичені пошкодження з віком розпізнаються імунними рецепторами та індукують активацію запалення, 146147, що призводить до хронічного запалення, що часто супроводжує різні вікові захворювання.148 Таке хронічне запалення, пов'язане зі старінням, було визначено новою ідеєю "запалення" .149 CR-позитивні ефекти на запалення були продемонстровані зменшенням запалення та резистентності до інсуліну, отриманими на моделі щурів o f пов'язане з віком запалення150, а також шляхом регуляції окислювально-відновного статусу GSH та експресії NF-κB, SIRT1, активованих проліфератором пероксисом рецепторів та FoxOs.151
CR-міметики
Майбутні додатки
Подяка
Це дослідження було підтримано грантами AMSL (Університет Барі-Прогетті ді Атенео, 2012) та грантом AMSL (Istituto Banco di Napoli-Fondazione, 2015). Ми дякуємо Флавіо Фракассо, штат МС, за допомогу з даними.
- Вживання в їжу лободи та цільних зерен щодня може допомогти вам жити довше The Independent The Independent
- Чи допомагає трохи зайвої ваги вам жити довше Новини Гарвард Т.
- Їжте менше живіть, довше цифровий Outlook
- Вживання найбільшої їжі за обідом ускладнює схуднення The Washington Post
- Дієтичне волокно змушує вас набирати вагу здоровим харчуванням SF Gate