Антиоксидантне лікування запобігає пошкодженню нирок та дисфункції та знижує артеріальний тиск при гіперчутливості, чутливій до солі
З кафедри фізіології та біофізики Медичного центру Університету Міссісіпі, Джексон.
З кафедри фізіології та біофізики Медичного центру Університету Міссісіпі, Джексон.
З кафедри фізіології та біофізики Медичного центру Університету Міссісіпі, Джексон.
З кафедри фізіології та біофізики Медичного центру Університету Міссісіпі, Джексон.
З кафедри фізіології та біофізики Медичного центру Університету Міссісіпі, Джексон.
Ви переглядаєте останню версію цієї статті. Попередні версії:
Анотація
Гіпертонія продовжує залишатись основним фактором серцево-судинного ризику та головним фактором, що сприяє кінцевій стадії ниркової хвороби. Зокрема, пацієнти з гіперчутливістю до солі набагато частіше страждають від ШОЕ порівняно з гіперчутливими до солі нечутливими. 1 Недавні дослідження на людях та на тваринних моделях гіперчутливості, чутливої до солі, вказують на те, що збільшення окисного стресу пов'язане з прогресивним підвищенням артеріального тиску та зниженням функції нирок. Однак механізми, що лежать в основі прогресування гіпертонії та ШОЕ при гіперчутливі до солі гіпертонії, не ясні.
Модель, яка точно імітує есенціальну гіпертензію, чутливу до солі людини, - щур Даля. Загальні риси, які поділяють чутливі до солі люди та щур S, включають прогресивне підвищення артеріального тиску та пошкодження нирок, 2,3 збільшення викиду O2 · - 4 та дисфункцію ендотелію. 5 Нещодавно ми показали, що окислювальний стрес, що виникає у щурів Dahl S при вживанні з високим вмістом натрію протягом 3 тижнів, сприяє підвищенню артеріального тиску, але ниркова гемодинаміка не змінювалася у щурів з високим вмістом натрію та пошкодження нирок було незначним. 6 На відміну від цього, пошкодження нирок набагато важче у щурів S на дієті з високим вмістом натрію протягом 5 тижнів, з поступовим зниженням швидкості клубочкової фільтрації (ШКФ) та ниркового плазмового потоку, але роль окисного стресу в гіпертонії зменшується в нирковій гемодинаміці а пов’язане з цим ураження нирок незрозуміле.
Нашою метою було перевірити гіпотезу, згідно з якою окислювальний стрес у щурів Dahl S при вживанні з високим вмістом натрію протягом 5 тижнів сприяє прогресуванню пошкодження нирок, зменшенню ШКФ та потоку ниркової плазми та розвитку гіпертонії. Ми спеціально вивчили, чи може антиоксидантна терапія, використовуючи вітаміни С та Е, допомогти запобігти пошкодженню нирок та зниженню ниркової гемодинаміки та послабити підвищення артеріального тиску.
Методи
Підготовка тварин, експериментальні вимірювання та приладобудування
Через 3 тижні на різних дієтах через стегнову артерію і вену імплантували хронічні артеріальні та венозні катетери за допомогою асептичних методик та ізофлуранової анестезії (1%). Пульсуючі сигнали артеріального тиску надсилалися на цифровий комп'ютер при частоті 500 Гц протягом 4 секунд кожної хвилини протягом усього 24-годинного періоду і використовувались для визначення артеріального тиску та частоти серцевих скорочень. Всім щурам дозволили відновитись протягом 4 днів до того, як розпочався 10-денний (дні з 26 по 35) збір артеріального тиску та функціональних даних нирок.
ШКФ та ефективний нирковий плазмовий потік визначали в кінці 5-тижневого періоду у свідомих щурів, як ми вже робили раніше, 6,7 шляхом вимірювання концентрації йоталамата та аміногіпурата в 4-годинному зразку плазми натще через 12 годин. період внутрішньовенної інфузії 125 I-йоталамату та аміногіпурата натрію. Наприкінці 5-тижневого періоду щурів знеболювали ізофлураном, а нирки видаляли для різних аналізів. Ниркову кору та мозкову тканину гомогенізували відповідними буферами та інгібіторами протеази, і хемілюмінесценцію вимірювали, використовуючи 5 мкмоль/л люцигеніну, як ми це робили раніше. 8 Кількість білка в ниркових тканинах визначали кількісно за допомогою аналізу Лоурі, а білок у сечі вимірювали за допомогою аналізу Бредфорда.
Аналіз гломерулярного некрозу, клубочкового склерозу та тубулоінтерстиціальної травми
Зріз PAS – гематоксилін у кожної щури досліджували на предмет некротичних та склеротичних клубочків при збільшенні 200 ×. Зрізи сканували в мікроскопічних полях, що не перекриваються, за допомогою монітора комп’ютера, а некротичні та склеротичні клубочки підраховували як частку всіх послідовно досліджуваних гломерулярних профілів будь-якого діаметра.
Пошкодження тубулоінтерстиціалу аналізували, використовуючи зріз, забарвлений трихромом Массона, від кожного щура. При збільшенні 100 × були зроблені зображення послідовних, неперекриваючих полів субкапсулярної до юкстамедулярної кори нирки над послідовними, неперекриваючими ділянками, що рухаються латерально вздовж субкапсулярної поверхні. За допомогою Adobe Photoshop 5.5 зображення було імпортовано на комп’ютер із 88-крапковою сіткою для підрахунку за допомогою програми для аналітичних зображень Image Pro Plus 4.5. Тубулоінтерстиціальне пошкодження вимірювали як частку кількості точок, що перекривають збільшену кількість пофарбованої синіми тканини міжклітинної тканини, розширеного гіпсу, що містить канальці, або канальців, що демонструють гостру травму, розділену на кількість точок на сітці, що перекриває негломерулярну та несудинну кору.
Статистичний аналіз
Порівняння даних тварин на дієтах з низьким вмістом солі та високим вмістом солі з вітамінами С та Е або без них спочатку було проведено з використанням двостороннього дисперсійного аналізу для повторних вимірювань або повністю рандомізованого дисперсійного аналізу з подальшим одностороннім дисперсійним аналізом для кожної групи та тест на найменшу значущу різницю для пост-hoc аналізу. Відмінності вважалися статистично значущими, якщо P · - Вивільнення відповідей на вітаміни С та Е
Малюнок 1 показує, що лікування вітамінами С та Е суттєво зменшило вивільнення O2 · - кортикальної та медулярної тканин нирок у щурів на дієті з високим вмістом натрію. У корі нирок та довгастому мозку лікування вітамінами зменшило вивільнення O2 · - у групах із високим вмістом натрію до рівнів, що не суттєво відрізняються від рівня групи з низьким вмістом натрію. 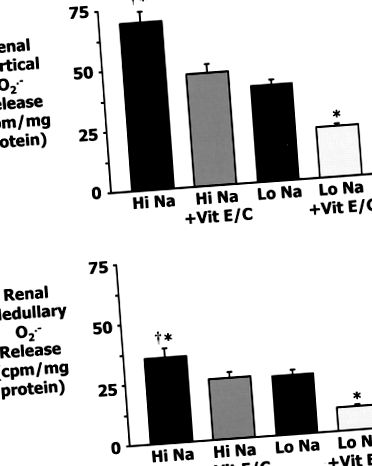
Фігура 1. Викид супероксиду в нирковій кортикальній та медулярній тканині щурів, чутливих до солі Даля (S), що мають лише дієту з високим вмістом натрію (n = 9), дієту з високим вмістом натрію та вітаміни Е та С (n = 7), лише дієту з низьким вмістом натрію (n = 8), а також дієта з низьким вмістом натрію плюс вітаміни Е і С (n = 9). †P
Середній артеріальний тиск, частота серцевих скорочень та реакція виведення білка з сечею на вітаміни С та Е
Малюнок 2 показує, що лікування вітамінами С та Е значно знижувало артеріальний тиск у щурів Dahl S на дієті з високим вмістом натрію. Тиск показано протягом останніх 10 днів 5-тижневого експерименту. На 35 день середній артеріальний тиск становив 180 ± 3 мм рт.P
Малюнок 2. Середній артеріальний тиск, частота серцевих скорочень та реакція виведення білка з сечею у щурів, чутливих до солі (S) Даль, які мають лише дієту з високим вмістом натрію (n = 9), дієту з високим вмістом натрію та вітаміни Е та С (n = 7), низьку концентрацію натрієва дієта (n = 8) та дієта з низьким вмістом натрію з вітамінами Е і С (n = 9). †P
Малюнок 2 також показує, що до 25-го дня екскреція білка з сечею, показник пошкодження нирок, значно зменшилась у групі з високим вмістом натрію та вітаміну порівняно з групою з високим вмістом натрію. На 35 день екскреція білка з сечею становила в середньому 285 ± 20 мг/добу у групі з високим вмістом натрію та 178 ± 36 мг/добу у групі з високим вмістом натрію та вітамінами С та Е (P
Малюнок 3. Швидкість клубочкової фільтрації (ШКФ) та відповідь ефективного потоку ниркової плазми (ERPF) у щурів, чутливих до солі (S) Даля, що мають лише дієту з високим вмістом натрію (n = 9), дієту з високим вмістом натрію та вітаміни Е та С (n = 7), дієта з низьким вмістом натрію (n = 8) та дієта з низьким вмістом натрію з вітамінами Е і С (n = 9). †P
Гістологічний аналіз нирок
На фіг.4 показані репрезентативні зрізи нирок для кожної групи щурів. У групі з низьким вмістом натрію (Малюнок 4А) та групою вітамінів С та Е з низьким вмістом натрію (Малюнок 4В) нирки мали нормальний вигляд, лише в окремих невеликих склеротичних клубочках у субокапсулярній корі.
Малюнок 4. Репрезентативні зміни патології в нирках щурів, чутливих до солі (S) Даля, що мають лише дієту з високим вмістом натрію, дієту з високим вмістом натрію та вітамінами Е та С, лише дієту з низьким вмістом натрію та дієту з низьким вмістом натрію з групами вітамінів Е та С. Нирки видаляли через 5 тижнів дієти натрієм. Застосовували трихромну пляму масонів. A, З низьким вмістом натрію. Нормальні клубочки, артеріоли та канальці, × 100. B, низький вміст натрію плюс вітаміни E і C. Нормальні клубочки, судини та канальці, × 100. С, високий натрій. Тромбонекроз артеріол (маленькі стрілки) та гострий клубочковий (велика стрілка) та пошкодження тубулоінтерстицію, × 100. D, високий вміст натрію та вітаміни E та C. Хронічне ураження клубочків та тубуло-інтерстиціальних тканин. Сегментарний гломерулосклероз (стрілка) та інтерстиціальний фіброз, × 100.
У щурів на дієті з високим вмістом натрію (рис. 4С) у нирках виявлено фібриноїдний артеріальний та артеріолярний некроз та фібриноїдний клубочковий некроз. Фібриноїдний клубочковий некроз часто зустрічався при безперервності некрозу аферентних артеріол. Час від часу клубочки на всіх рівнях кори демонстрували глобальний або сегментарний клубочковий склероз. Канальці містили вироджені клітини, залишки клітин та еритроцити з інтерстиціальним крововиливом, прилеглим до некротичних артеріол та клубочків.
У щурів на дієті з високим вмістом натрію та вітамінами С та Е (рис. 4D) нирки мали лише поодинокі клубочки, які виявляли фібриноїдний клубочковий та артеріолярний некроз. На додаток до невеликих склеротичних гломерулів у підкапсулярній корі, які були виявлені у щурів на дієті з низьким вмістом натрію, клубочки були виявлені на всіх рівнях кори, що продемонструвало сегментарний та глобальний склероз клубочків. Тубулоінтерстиціальне пошкодження, яке було набагато рідше, ніж у щурів на дієті з високим вмістом натрію, складалося з скупчень розширених канальців з потовщеними базальними мембранами, оточених підвищеною кількістю інтерстиціальної сполучної тканини.
Середня реакція на пошкодження клубочків та тубуло-інтерстиціальних клітин на вітаміни С та Е
Малюнок 5 показує, що середній клубочковий некроз значно збільшився у щурів Dahl S на дієті з високим вмістом натрію в порівнянні з групою з високим вмістом натрію та вітаміну або групою з низьким вмістом натрію. Лікування вітамінами С та Е суттєво зменшило рівень некрозу клубочків у щурів Dahl S при високому споживанні натрію. Клубочковий склероз, хоча і спостерігався певною мірою у всіх щурів, суттєво не відрізнявся в жодній групі. Сегментарний склероз був присутнім у групі з високим вмістом натрію та групами з високим вмістом натрію та вітамінів С та Е, але не в тій мірі, яка викликала статистичну значимість для загального склерозу. На малюнку 5 також видно, що середнє пошкодження тубулоінтерстиціалу в середньому становило 0,19 ± 0,03 (площа фракції) у групі з високим вмістом натрію, і ця площа зменшилася до 0,11 ± 0,02 у щурів з високим вмістом натрію, які отримували вітаміни С та Е. споживання їжі та води, а також вага тіла та нирок можна знайти в Інтернет-додатку (http://hyper.ahajournals.org).
Малюнок 5. Середній клубочковий некроз та склероз (фракція клубочків) та нирково-тубулоінтерстиціальне пошкодження в нирках щурів, чутливих до солі Даля (S), що мають лише дієту з високим вмістом натрію (n = 8), дієту з високим вмістом натрію та вітаміни Е та С (n = 6), дієта з низьким вмістом натрію (n = 7) та дієта з низьким вмістом натрію з вітамінами Е і С (n = 7). †P
Обговорення
Обробка щурів, чутливих до солі Даля, вітамінами С та Е значно зменшила нирковий окислювальний стрес. Лікування вітамінами ефективно підвищувало ШКФ та нирковий плазмовий потік, помітно зменшувало пошкодження нирок та знижувало артеріальний тиск. Ці дані свідчать про те, що окислювальний стрес є одним із основних факторів, що сприяють порушенню функції нирок та пошкодженню солевочутливої гіпертензії. Дані також вказують на те, що механізмами, що сприяють виникненню чутливої до солі гіпертонії Даля, є зниження ШКФ та ниркового потоку плазми.
Кілька факторів могли сприяти зменшенню ШКФ та ниркового потоку плазми. По-перше, на малюнку 4 видно, що дієта з високим вмістом натрію призводить до некрозу клубочків та судин. Це може безпосередньо спричинити зменшення кількості функціонуючих нефронів із пов'язаною з ними судинною системою, що зменшує ШКФ та нирковий кровотік. По-друге, чутлива до солі гіпертонія асоціюється із збільшенням судинозвужувальних засобів. У попередньому дослідженні в нашій лабораторії підвищена дієта натрію у щурів Dahl S протягом 3 тижнів спричиняла збільшення рівня F2-ізосопростанов у сечі та плазмі, що може спричинити звуження судин. 8 Інші дослідження показали, що дієта з високим вмістом натрію пов’язана зі збільшенням внутрішньониркової ангіотензину II, 10 що також може призвести до звуження нирок. По-третє, збільшення ниркового O2 · - вивільнення інактивує оксид азоту, що зменшить ниркову вазодилатацію, що призводить до посилення звуження судин.
Тварини з високим вмістом натрію та високим вмістом натрію та вітамінами Е та С виявили контрастні патологічні зміни. У щурів з високим вмістом натрію були ниркові зміни флоридної злоякісної гіпертензії з гострим пошкодженням канальців, при якому пошкодження канальців, здавалося, головним чином відбувалося поруч з некротичними клубочками у судинному забезпеченні некротичних та тромбованих артерій та артеріол. Нирки щурів на дієті з високим вмістом натрію та вітамінами С та Е показали деякі ознаки злоякісної гіпертензії, але на набагато менш інтенсивному рівні, ніж тварини, які приймали лише натрій. У групі з високим вмістом натрію та вітамінами С та Е гістопатологія була зміщена в бік гломерулосклерозу та артеріальної гіперплазії інтими, а не гломерулярного та артеріального некрозу, і пошкодження тубулоінтерстицію виявилося більш безладно, ніж у тварин, які приймали високий вміст натрію.
Основними клітинними джерелами активних форм кисню є оксидази NADH/NADPH, ксантиноксидаза, оксид азоту синтаза, циклооксигеназа, ліпоксигеназа та ферменти дихального ланцюга мітохондрій. Судинна активність NADPH-оксидази зростала у спонтанних гіпертонічних щурів, схильних до інсульту, 14 та активність NADPH-оксидази знижувались після обробки цих щурів вітаміном Е або вітаміном C. Ниркова ксантиноксидаза у щурів Dahl S збільшувалась під час прийому з високим вмістом натрію 18 та інгібування ксантину оксидазна активність з вольфрамом знижує артеріальний тиск. 19
Підводячи підсумок, добавки вітамінів С та Е до щурів Dahl S на дієті з високим вмістом натрію помірно знижували артеріальний тиск, знижували окислювальний стрес та пошкодження нирок та збільшували ниркову гемодинаміку. Пошкодження нирок у щурів Dahl S з високим вмістом натрію включало значне ураження інтерстиціальної нирки та клубочковий та артеріальний некроз із тромбованими артеріями та артеріолами. Гістопатологічні зміни у щурів Dahl S з високим вмістом натрію з добавками вітамінів С та Е продемонстрували значне зменшення пошкоджень інтерстиціальних, клубочкових та судинних систем та перехід від клубочкового некрозу до більш стабільного гломерулосклерозу. Зниження ШКФ та ниркового потоку плазми запобігали за допомогою добавок вітамінів С та Е. Нирковий окислювальний стрес при чутливій до солі гіпертензії відіграє важливу роль у загостренні нефропатії та зменшенні ниркової гемодинаміки.
Перспективи
Було проведено кілька клінічних випробувань, щоб визначити, чи може лікування вітамінами покращити серцево-судинні захворювання. Хоча були знайдені різні результати, деякі дослідження показали, що лікування пацієнтів з гіпертонічною хворобою вітаміном С знижує артеріальний тиск. 20 У більшості клінічних досліджень вітаміну Е використовували дози ≤400 МО/добу, і зменшення серцево-судинного ризику не зафіксовано 21; однак, коли було використано 800 МО/день вітаміну Е, відбулося 22,23 значне зниження серцево-судинного ризику. В недавньому 16-тижневому дослідженні у пацієнтів з гіперхолестеринемією 400 МО/день вітаміну Е не знижували рівні F2-ізопростанов у сироватці крові, але дози від 800 МО/день до 3200 МО/день спричиняли значне зниження рівня F2-ізопростану. 17 Другою причиною того, чому вітамін Е був неефективним у деяких клінічних дослідженнях, є те, що вітамін Е може стати вільним радикалом в організмі, 24 але вітамін С може перетворити прооксидантний вітамін Е радикал назад у вітамін Е, 24 саме тому ми використовували вітамін С у нашому дослідженні. Третя причина, чому вітамінна терапія є неефективною в клінічних дослідженнях, полягає в тому, що у пацієнтів були вже існуючі стани, коли вони вступили в дослідження. 21–23
Цей документ було надіслано Фрідріху К. Луфту, заступнику редактора, для ознайомлення з експертними рецензіями, редакційного рішення та остаточного рішення.
Це дослідження було підтримано грантом HL-51971 від Національного інституту серця, легенів та крові.
- Дієта з високим вмістом калорій посилює дисфункцію мітохондрій та викликає серйозні пошкодження печінки у Вільсона
- Дієта з низьким вмістом вуглеводів з високим вмістом жиру знижує артеріальний тиск у щурів, які спонтанно страждають гіпертонією
- Антиоксидант захищає від пошкодження легенів при силікозі - ScienceDaily
- Нервова анорексія - види, причини і лікування
- 1,25-дигідроксихолекальциферол запобігає та пом'якшує симптоми експериментального запалення мишей