Вплив інкапсульованої суміші поживних речовин на споживання їжі та ситність: подвійний сліпий рандомізований перехресний доказ концептуального дослідження
Еннік М. Е. Аллелейн
2 Відділ гастроентерології-гепатології, кафедра внутрішніх хвороб, Школа харчування та поступальних досліджень у метаболізмі, Медичний центр Університету Маастрихта +, П.О. Box 5800, 6202 AZ Маастрихт, Нідерланди; [email protected] (Д.К.); [email protected] (E.W.)
Марк ван Авесаат
2 Відділ гастроентерології-гепатології, кафедра внутрішніх хвороб, Школа харчування та поступальних досліджень у метаболізмі, Медичний центр Університету Маастрихта +, П.О. Box 5800, 6202 AZ Маастрихт, Нідерланди; [email protected] (Д.К.); [email protected] (E.W.)
Діна Ріпкен
3 Нідерландська організація прикладних наукових досліджень, TNO, P.O. Box 360, 3700 AJ Zeist, Нідерланди
4 Відділ харчування людини, Університет Вагенінгена, П.О. Box 17, 6700 AA Wageningen, Нідерланди
Синеад Б. Блейель
5 AnaBio Technologies LTD., Інноваційний центр, Carrigtwohill, T45 RW24 Корк, Ірландія; [email protected]
Даніель Кестхелі
2 Відділ гастроентерології-гепатології, кафедра внутрішніх хвороб, Школа харчування та поступальних досліджень у метаболізмі, Медичний центр Університету Маастрихта +, П.О. Box 5800, 6202 AZ Маастрихт, Нідерланди; [email protected] (Д.К.); [email protected] (E.W.)
Елен Вілмс
2 Відділ гастроентерології-гепатології, кафедра внутрішніх хвороб, Школа харчування та поступальних досліджень у метаболізмі, Медичний центр Університету Маастрихта +, П.О. Box 5800, 6202 AZ Маастрихт, Нідерланди; [email protected] (Д.К.); [email protected] (E.W.)
Фредді Дж. Троост
2 Відділ гастроентерології-гепатології, кафедра внутрішніх хвороб, Школа харчування та поступальних досліджень у метаболізмі, Медичний центр Університету Маастрихта +, П.О. Box 5800, 6202 AZ Маастрихт, Нідерланди; [email protected] (Д.К.); [email protected] (E.W.)
6 Харчові інновації та здоров'я, Центр здорового харчування та інновацій у харчовій промисловості, Маастрихтський університет, 5911 AA Venlo, Нідерланди
Хенк Ф. Дж. Хендрікс
Адріан А. М. Масклі
2 Відділ гастроентерології-гепатології, кафедра внутрішніх хвороб, Школа харчування та поступальних досліджень у метаболізмі, Медичний центр Університету Маастрихта +, П.О. Box 5800, 6202 AZ Маастрихт, Нідерланди; [email protected] (Д.К.); [email protected] (E.W.)
Анотація
Активація кишкового гальма шляхом введення поживних речовин у дистальний відділ тонкої кишки за допомогою катетерів перешкоджає надходженню їжі та посилює насичення. Капсуляція макроелементів, яка захищає від травлення в проксимальному відділі шлунково-кишкового тракту, може бути неінвазивною альтернативою активації цього гальма. У цьому дослідженні ми досліджуємо ефект перорального прийому всередину інкапсульованої суміші казеїну та сахарози (активної), спрямованої на дистальний відділ тонкої кишки, порівняно з контрольним продуктом, призначеним для вивільнення у шлунку, на споживання їжі, насичення та концентрацію глюкози в плазмі. П'ятдесят дев'ять добровольців отримали активний і контрольний продукт протягом двох окремих тестових днів. Споживання їжі визначали під час прийому їжі ad libitum через 90 хв після прийому досліджуваного продукту. Візуальні аналогові шкали оцінок ситості та зразки крові для аналізу глюкози збирали через рівні проміжки часу. Проковтування активного продукту зменшило споживання їжі порівняно з контрольним продуктом (655 ккал порівняно з 699 ккал, відповідно, p Ключові слова: ситість, інкапсульована поживна суміш, дистальне вивільнення, вуглеводи, білки, надмірна вага, регулювання ваги
1. Вступ
Кишкове гальмо складається з механізму негативного зворотного зв’язку від дистальних до більш проксимальних відділів шлунково-кишкового тракту (ШКТ) і активується внутрішньопросвітними макроелементами та продуктами їх травлення. Це гальмо контролює не тільки рухливість та секрецію шлунково-кишкового тракту, але також споживання їжі та почуття ситості [1,2,3]. Раніше було показано, що всі типи макроелементів здатні активувати це кишкове гальмо і тим самим впливати на харчову поведінку [4]. Хоча всі відділи тонкої кишки (дванадцятипала кишка, тонка кишка та клубова кишка) здатні активувати це «кишкове гальмо», то, як вважається, клубове гальмо індукує найпотужніші сигнали зворотного зв’язку при контролі над їжею та насиченням [5,6]. Тому активація клубового гальма виявилася потенційною метою зменшення споживання калорій і, в довгостроковій перспективі, для регулювання ваги [7].
Дотепер активація кишкового гальмування у людей в основному вивчалася за допомогою інтубації кишечника, тобто шляхом встановлення носо-кишкових катетерів для введення, щоб вводити поживні речовини безпосередньо в тонкий кишечник [4,5]. Ці дослідження дали чіткі докази того, що вливання невеликої кількості або жиру, або білка, або вуглеводів у дистальний відділ тонкої кишки зменшує споживання їжі та підвищує насичення. Для клінічного застосування слід розробити інші менш інвазивні стратегії доставки макроелементів у тонку кишку.
Schellekens et al. і Varum та співавт., обидва успішно розробили системи для цілеспрямованої та специфічної доставки лікарських засобів у ШКТ [8,9]. Подібний підхід може бути використаний для цільової доставки поживних речовин. Капсулювання поживних речовин харчовим покриттям створює бар’єр проти травлення в проксимальному відділі шлунково-кишкового тракту і вважається неінвазивною альтернативою цілеспрямованої доставки поживних речовин. Попередні дослідження використовували олійно-емульсійний продукт (Fabuless ®, Olibra ®), спрямований на більш дистальну доставку жиру. Ці продукти базувались на специфічних фізико-хімічних властивостях емульгатора [10,11,12]. Запропонованим механізмом Fabuless є активація клубового гальма; емульговані олії затримують ліполіз і поглинання жиру з проксимального відділу шлунково-кишкового тракту і, отже, піддають дистальний тракт шлунково-кишкового тракту високому вмісту внутрішньосвітлового жиру. Було показано, що Fabuless зменшує споживання їжі та підвищує ситість у дослідженнях Бернса та співавт. [7,8,9], хоча це не було підтверджено іншими [13,14,15,16]. Було висловлено гіпотезу, що переробка їжі, можливо, зменшила здатність Fabuless доставляти неперетравлений жир у дистальний відділ тонкої кишки [16].
Цей доказ концептуального дослідження мав на меті дослідити гострий ефект інкапсульованої поживної суміші, що вводиться перорально, орієнтуючись на більш дистальний викид кишечника, на споживання їжі та насичення порівняно з контрольним продуктом, який розпадається в шлунку у здорових осіб із надмірною вагою. Ми висунули гіпотезу, що інкапсульована поживна суміш потужніше індукує насичення та зменшує споживання їжі під час прийому їжі ad libitum порівняно з контрольним станом. Ми ввели два макроелементи: білок (казеїн) та вуглевод (сахароза). Ми вирішили не вводити жир, оскільки введення значної кількості жиру в дистальну частину клубової кишки може призвести до дискомфорту в ШКТ [17,18]. Крім того, жир вимагає іншої методики капсулювання порівняно з вуглеводами та білками [19].
2. Матеріали та методи
Дослідження було схвалено Комітетом з медичної етики Медичного центру Університету Маастрихта + та проводилось у повній відповідності з принципами Гельсінської декларації 1975 року зі змінами, внесеними у 2013 році, та Голландським положенням про медичні дослідження за участю людей (1998). Усі учасники давали письмову інформовану згоду перед участю. Це випробування було зареєстровано за адресою www.clinicaltrials.gov як> NCT02635659.
2.1. Предмети
Випробовуваних набирали у період з грудня 2015 року по червень 2016 року. Здорові добровольці мали право брати участь, якщо вони були у віці від 18 до 65 років та мали індекс маси тіла (ІМТ) від 25 до 30 кг/м 2. Добровольців набирали за місцевими оголошеннями. Критеріями виключення були споживання більше 20 алкогольних напоїв на тиждень, специфічне вживання ліків або історія хвороби будь-якого відповідного розладу чи хірургічного втручання, що може впливати на результати дослідження (за оцінкою лікаря), відомі симптоми ШКТ та дієта. Усі суб’єкти повідомляли про стабільність ваги протягом щонайменше 6 місяців перед скринінгом та нестримну їжу (оцінювану голландським опитувальником щодо харчової поведінки [20]) та повідомили, що вони не сиділи на дієті протягом періоду дослідження. Після надання первинної інформації усно або електронною поштою, на випадок зацікавленості суб’єктів була надана детальна письмова інформація про дослідження. Усі суб'єкти повинні були розуміти процедури навчання до того, як було підписано інформовану згоду. Письмова інформована згода була отримана через інтервал не менше 7 днів.
Розрахунок потужності базувався на зменшенні споживання їжі на 136 ккал, виявленому в дослідженні інфузії клубової вуглеводи, проведеному нашою групою [4]. Ми очікували виявити зниження на 50%, що відповідає 68 ккал. При стандартному відхиленні 175 ккал, потужності 80% і альфа 0,05, потрібно було загальної кількості 54 суб'єктів. Передбачаючи 10–15% відсіву, ми включили 62 здорових суб’єктів.
2.2. Вивчати дизайн
Це подвійне сліпе, рандомізоване, контрольоване перехресне дослідження порівнювало ефект інкапсульованої поживної суміші, спрямованої на дистальний відділ тонкої кишки, з ефектом ідентичного контрольного продукту (поживна суміш з альгінатною інкапсуляцією, яка розпадається в шлунку). Продукт, який досліджували, вживали через 180 хв після стандартного сніданку, щоб забезпечити спорожнення шлунка перед проковтуванням тестових напоїв. Планувались дні тестування з періодом вимивання 1 тиждень між ними, щоб уникнути можливих наслідків перенесення. Випробувальні дні були призначені випадковим чином (за допомогою Research Randomizer, www.randomizer.org). Суб'єкти були рандомізовані на лікування у рандомізованих блокових конструкціях. Основними факторами рандомізації були стать та вік.
2.3. Вивчення продуктів
Активним продуктом була інкапсульована поживна суміш, що містила 16 г сахарози (4 ккал г -1, ван Гільзе Автоматизатор, Оуд Гастель, Нідерланди), 10 г казеїну (щільність енергії: 3,45 ккал г -1, Нідерландська білкова служба, Тіль, Нідерланди) та 2 г сироваткового білка, який був використаний для виготовлення мікрокапсуляту (AnaBio Technologies, щільність енергії 112 ккал). Контрольний продукт містив 16 г сахарози та 10 г казеїну (AnaBio Technologies, щільність енергії 107 ккал). Макроелементи контрольного продукту інкапсулювали системою інкапсуляції альгінату натрію, що характеризується екструзією відповідного мікроелемента з використанням 1,8% (мас./Об.) Альгінату натрію з подальшим висушуванням. Зразки розчиняли у загальному обсязі 80 мл води перед споживанням. Напої готував незалежний дослідник і пропонував у чорній непрозорій пляшці, щоб засліпити і слідчого, і учасника.
2.4. Процедура мікроінкапсуляції
Процедура приготування мікрокапсул описана в патенті WO 2016/096931 A1 [21]. Всі матеріали були виготовлені відповідно до рекомендацій належної виробничої практики (GMP). Система мікроінкапсуляції використовує джерела сахарози та казеїну, що містять харчові продукти, для генерування мікрономних капсул для контрольованої доставки природного казеїну та сахарози до дистальної частини тонкої кишки для стимулювання гальмівного механізму кишечника. Гастростійкі мікрокапсули отримували, коли форму сахарози та казеїну екструдували через апарат, що складається із зовнішнього сопла, концентрично розташованого навколо внутрішнього сопла, і в якому денатурований білковий розчин екструдується через зовнішнє сопло та серцевинний казеїн —Розчин сахарози видавлюється через внутрішню форсунку. Мікрокраплі миттєво полімеризувались у кислому розчині і партії витримували при кімнатній температурі протягом максимум. 1 год в асептичних умовах. Цей процес дозволяє уникнути (1) закупорки розчину сахарози - казеїну в концентричній форсунці та (2) розбіжностей потоку під час процесу інкапсуляції, що може вплинути на ефективність інкапсуляції мікрокапсул сахарози-казеїну.
2.5. Характеристика мікро-капсулятів
2.5.1. Розподіл за розмірами та ефекти висушування
За даними світлової мікроскопії, мікрошарики продемонстрували діаметр приблизно 200 мкм з вузьким розподілом за розміром (± 1,2 мкм). Також була включена лазерна дифрактометрія, яка підтвердила значення D (ν, 0,9) для мікрокапсулятів, виявивши діаметр 201,7 ± 0,90 мкм та 183,42 ± 0,90 мкм, до і після висихання відповідно.
2.5.2. Інкубація шлунка та сила мікроінкапсулятів
Міцність мікрогранул аналізували як функцію часу інкубації шлунка in vivo (рН 1,2–1,4; 37 ° C). Не повідомлялося про різницю в міцності мікрошарочок для інкубації шлунка, а активовані ферментами умови шлунку не суттєво змінювали силу мікрогранул. Міцність на розтяг мікрогранул залишалася незмінною, не спостерігалося витоку або втрати інкапсульованого казеїну, білка гороху або сахарози. Після 180 хв шлункової інкубації мікрокапсуляти інкапсульованих казеїну, білка гороху та сахарози підтримували високу міцність на розрив 52,03 ± 1,27 нН, 60,31 ± 0,27 нН та 58,23 ± 0,12 нН, відповідно, для підтримки надійної та високопродуктивної системи інкапсуляції макроелементів.
2.5.3. Інкубація та деградація кишечника
Час транзиту мікрокапсулятів досліджували під час випробувань in vivo, і вони спостерігали, що через 35 хв після перорального прийому не відбулося деградації мікрокапсулятів у дванадцятипалій кишці. Було перевірено підтримання цілісності мікроінкапсуляту в рідинах тонкої кишки, і деградація не була очевидною. З плином часу капсулярна мембрана поступово деградує, виділяючись до одноядерного матеріалу серцевини [21].
2.6. Протокол
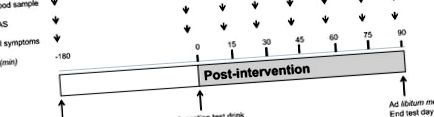
Графік тестового дня. Пробний напій (інкапсульована поживна суміш або контрольний препарат) вживали через 180 хв після закінчення сніданку. Зразки крові, оцінки VAS щодо насичення та оцінки симптомів шлунково-кишкового тракту збирали через рівні проміжки часу, як зазначено.
2.7. Оцінки VAS за ситість, повноту, бажання їсти, голод та оцінку симптомів шлунково-кишкового тракту
Ситість, голод, повноту та бажання їсти вимірювали за допомогою оцінок VAS (0–100 мм), закріплених у нижній частині з найбільш негативними почуттями найменшої інтенсивності (вкрай неприємними, зовсім не) та з протилежними умовами у верхній частині (надзвичайно приємний, дуже високий, екстремальний) [22]. Симптоми шлунково-кишкового тракту оцінювали за допомогою опитувальника, який відповідав на такі скарги, як нудота, здуття живота, головний біль та інші симптоми. Симптоми були оцінені за 4-бальною шкалою, оцінка 0 означала "не присутній" до 3 "сильно присутній". Випробовуваних попросили позначити оцінки симптомів VAS та GI перед вживанням сніданку. Це вважалося t = -180 хв. Суб'єкти також відзначали оцінки VAS та GI перед вживанням тестового напою. Після прийому досліджуваного напою (між t = 0 хв та t = 90 хв) симптоми VAS та GI оцінювали з інтервалом у 15 хв до початку обіду ad libitum.
2.8. Збір проб крові
Зразки венозної крові брали перед сніданком (натщесерце) та перед прийомом досліджуваного напою (t = 0 хв). Після прийому досліджуваного напою зразки крові відбирали кожні 15 хв до початку прийому їжі ad libitum (t = 90 хв) для аналізу глюкози. Концентрації глюкози аналізували як непрямий показник місця доставки поживних речовин та подальшого поглинання поживних речовин. Флуоридні пробірки натрію (Becton & Dickinson, NJ, США) використовували для збору зразків крові для концентрації глюкози в плазмі. Вимірювання глюкози проводили за допомогою аналізатора Roche Cobas C701 (GLUC3, Roche, Мангейм, Німеччина) з варіацією між тестами 0,02 ммоль/л при концентрації глюкози 3,27 ммоль/л.
2.9. Статистичний аналіз
- Використання твердження про низький вміст поживних речовин Рекомендації FDA Виробники продуктів харчування повинні знати
- Вплив підвищення ціни на їжу на споживання калорій у Китаї
- Вплив освіти з питань харчування на знання, ставлення та результати щодо нездорової їжі
- Вплив харчування та виховання гігієни харчування на знання жіночої початкової школи
- Втрачена їжа, втрачені поживні речовини Втрата поживних речовин від відходів харчування у Сполучених Штатах та порівняння з