Успішне лікування алергічного бронхолегеневого аспергільозу ісавуконазолом: звіт про випадки та огляд літератури
Саманта Е. Джейкобс
1 відділ інфекційних хвороб, медицина Weill Cornell, Нью-Йорк, Нью-Йорк
Дебора Саез-Лейсі
2 Акушерство та гінекологія Бріель, Манаскван
Вальтер Вінкуп
3 Ocean Pulmonary Associates, Brick, New Jersey
Томас Дж. Уолш
1 відділ інфекційних хвороб, медицина Weill Cornell, Нью-Йорк, Нью-Йорк
Анотація
Ісавуконазол - новий триазол, який схвалений для первинної терапії інвазивного аспергільозу. Ми надаємо перший звіт про пацієнта з алергічним бронхолегеневим аспергільозом (ABPA), який успішно лікувався ізавуконазолом із помітним поліпшенням та мінімальними побічними ефектами. Далі ми розглядаємо літературу щодо протигрибкового лікування ABPA.
Алергічний бронхолегеневий аспергільоз (ABPA) є результатом аномальної перебільшеної місцевої та системної імунної відповіді на конідії та гіфи, що колонізують синопульмональний тракт. Алергічний бронхолегеневий аспергільоз ускладнює астму та муковісцидоз у 1% –2% та 5% –15% пацієнтів відповідно [1]. У хворих на астму ABPA представляється як погано контрольована астма з хрипами, кашлем, виділенням мокроти, субфебрильною температурою, втратою ваги та нездужанням.
Лікування алергічного бронхолегеневого аспергільозу включає кортикостероїди для контролю імунної відповіді господаря та протигрибкові засоби для зменшення навантаження на організм. В даний час ітраконазол є препаратом першої лінії для симптоматичних хворих на ABPA на основі рандомізованих, контрольованих клінічних випробувань [2, 3]. Вориконазол є альтернативою, заснованою на даних спостережень [4]. Однак і ітраконазол, і вориконазол пов'язані зі значними несприятливими ефектами.
Ісавуконазол - це протигрибковий триазол широкого спектру дії, що має потужну активність щодо видів Aspergillus. Рекомендується як альтернативна первинна терапія інвазивних синдромів аспергільозу в Інструкціях Американського товариства інфекційних хвороб 2016 року [5]. Ми надаємо перший звіт про пацієнта з ABPA, який успішно лікувався ізавуконазолом після стійких симптомів та значних побічних ефектів з ітраконазолом та вориконазолом.
МЕТОДИ
Ми спершу прагнули зрозуміти вплив системного протигрибкового лікування на ABPA. Тому ми систематично шукали в базі даних PubMed англомовну літературу протигрибкової терапії АБПА у пацієнтів з основною астмою. Були використані такі пошукові терміни: “ітраконазол”, “вориконазол”, “позаконазол”, “ізавуконазол”, “небулайзований амфотерицин В” та “алергічний бронхолегеневий аспергільоз”. Потім ми детально повідомляємо про наш індекс.
ЗВІТ ПРО СПРАВУ
56-річна жінка-лікар з астмою була звернена до консультацій у травні 2015 року щодо управління ABPA. Її симптоми почалися у вересні 2009 року, коли у неї розвинулася грипоподібна хвороба з лихоманкою, нездужанням, непродуктивним кашлем та зниженням толерантності до фізичних навантажень. Вона регулярно відвідувала заняття аеробними вправами, але виявила, що будь-яка активність, що збільшує частоту дихання, призводить до "нападу" кашлю, що виключає подальші фізичні вправи.
Навесні 2010 року кашель та хрипи посилились, і у неї з’явилося нове виділення мокроти. Рівень імуноглобуліну (Ig) в сироватці крові становив 813 МО/мл, виявляли осаджуючі сироваткові антитіла IgG до Aspergillus fumigatus, тести на шкіру Aspergillus були позитивними, а посіви мокроти вирощували A fumigatus. Комп’ютерна томографія з високою роздільною здатністю (КТ) грудної клітки продемонструвала м’яку гіперінфляцію легенів двобічно та мінімальні запальні зміни в лівому середині легені. Тести легеневої функції (ПФТ) виявили обструктивну хворобу дихальних шляхів (обсяг форсованого видиху [ОФВ] 1 2,08 л, вимушена життєва ємність [ФВК] 3,02 л, ОФВ1/ФВК 69%), яка не покращилася після бронходилататорної терапії. У пацієнта діагностовано ABPA. У жовтні 2010 року їй призначили преднізон по 0,5 мг/кг перорально щодня протягом 1 тижня з подальшим зменшенням протягом 3 місяців. Її респіраторні симптоми покращились настільки, що вона могла брати участь у заняттях аеробною гімнастикою. IgE в сироватці крові знизився до 326 МО/мл. Однак вона не змогла повністю припинити прийом кортикостероїдів. Культури мокроти продовжували вирощувати види Aspergillus до липня 2011 р. Тести легеневої функції показали стабільну легку обструкцію.
Протягом наступного року хронічне утворення кашлю та мокроти тривало, і вона ненавмисно схудла на 15 кілограмів. У жовтні 2011 р. Вона відновила рівень преднізону приблизно до 1 мг/кг. У грудні 2011 р. Вона почала застосовувати ітраконазол; однак у неї розвинулася вулик, і препарат припинили. Потім її лікували вориконазолом по 200 мг перорально двічі на день, і виділення кашлю та мокроти значно покращилося. Потім преднізон скорочувався та припинявся. IgE в сироватці крові знизився з 663 МО/мл до 384 МО/мл. У березні 2012 року вона зупинила вориконазол через безсимптомне підвищення рівня аланінамінотрансферази (АЛТ) до 247 МО/л.
Восени 2012 року та взимку 2013 року у неї повторювався бронхіт та пневмонія через синьогнійну паличку. КТ грудної клітки високої роздільної здатності показало циліндричні бронхоектатичні захворювання як нижніх часток, так і двосторонні, множинні крихітні вузлики легенів. В межах заднього базального сегмента лівої нижньої частки спостерігалася непрозорість 5,1 × 4,5 × 2,0 см. Під час бронхоскопії в дихальних шляхах спостерігалася густа біла мокрота. Культура рідини бронхоальвеолярного промивання вирощувала види Aspergillus, Cladosporium та мальтофілію Stenotrophomonas. Дані про протигрибкову сприйнятливість були недоступні. Пацієнт відновив вориконазол у вересні 2014 року і знову відзначив клінічне покращення. Рівень IgE знизився з 1583 МО/мл до 787 МО/мл. Тести легеневої функції показали помірну обструкцію (ОФВ1 1,61L, ОФВ1/FVC 68%). Однак вона пережила фотопсію, і рівень АЛТ у сироватці крові збільшився більш ніж удвічі вище верхньої межі норми. Вориконазол було припинено в березні 2015 року. З огляду на те, що пацієнт не міг переносити вориконазол і був стурбований несприятливими ефектами кортикостероїдів, вона подала до пресбітеріанської лікарні Нью-Йорка/Медицини Weill Cornell для подальшого управління.
Додаткова минула історія хвороби включала індукований кортикостероїдами діабет (контрольований дієтою), остеопенія та сезонна алергія. Ліки включали небулайзери N-ацетилцистеїну, інгалятор альбутеролсульфату, назальний спрей азеластин-флутиказон, інгалятор беклометазону, інгалятор будесонід-формотерол, фексофенадин та монтелукаст.
Під час фізичного огляду життєві показники були нічим не примітними. Насичення киснем становило 96% під час дихання навколишнім повітрям. Індекс маси тіла становив 17,4 кг/м 2. Хрипи середнього вдиху та видиху були вислухані по легеневих полях. Решта іспиту була нормальною. Рівень IgE в сироватці крові становив 676 МО/мл. Швидкість осідання еритроцитів становила 20 мм/годину (норма 0–40 мм/годину), а С-реактивний білок - 0,5 мг/л (норма 0,0–4,9 мг/л).
З огляду на погану переносимість пацієнтом кортикостероїдів (остеопенія та гіперглікемія), вориконазолу (фотопсія та підвищений рівень аспартатамінотрансферази [AST] та ALT) та ітраконазолу (реакція гіперчутливості), їй призначили пероральний ісавуконазол у дозі 200 мг кожні 8 годин × 2 дні, після чого 200 мг один раз на день. Їй було наказано приймати ізавуконазол 4-місячними «імпульсами», щоб полегшити симптоми під час загострення АБРА, одночасно зменшуючи ризик появи резистентності. Протягом кількох тижнів вона відзначила помітне поліпшення вироблення мокротиння та хрипів, і навіть у липні 2015 року вона змогла здійснити рюкзак на 16 миль. Вона припинила приймати беклометазон і продовжувала застосовувати лише будесонід-формотерол. Рівень IgE у сироватці крові залишався підвищеним на рівні 732 МО/мл. У серпні 2015 року, після 10 тижнів терапії, вона припинила застосування ізавуконазолу, зазначивши, що її толерантність до фізичних навантажень була найкращою за останні роки. Як правило, вона добре переносила ізавуконазол, за винятком водянистої діареї, яку вона приписувала препарату і яка затримувалася на кілька тижнів після припинення терапії. АСТ та АЛТ у сироватці крові залишались у межах норми.
Пацієнт продовжував почувати себе добре протягом усієї осені 2015 року та підтримував прийом будесоніду-формотеролу. На повторних PFT FEV1 покращився до 2,42 л, а FEV1/FVC становив 68%. У січні 2016 року збільшилося виділення мокроти та хрипи відповідно до загострення ABPA. Пацієнт відновив застосування ізавуконазолу в березні 2016 року з тією ж навантажувальною дозою. Знову вона відзначила симптоматичне поліпшення, і вона взяла участь у 5 пішохідних поїздках навесні та влітку. У травні 2016 р. Вона припинила застосування ізавуконазолу. Тести легеневої функції були повторені в липні 2016 р. І знаходились у межах норми (ОФВ 1,43 л, ОФК 3,39 л, ОФВ 1/ФВК 72%) (рис. 1). Починаючи з січня 2017 року, у неї продовжують спостерігатися мінімальні респіраторні симптоми, і вона залишається поза системними кортикостероїдами та відлучає інгаляційні кортикостероїди до 1 затяжки будесоніду/формотеролу щодня.
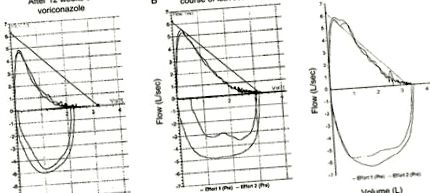
Криві обсягу потоку. (А) Помірна обструкція дихальних шляхів під час прийому вориконазолу в грудні 2014 року (об’єм форсованого видиху [ОФВ] 1 1,61 л, примусова життєва ємність [ФВК] 2,38 л, ОФВ1/ФВК 68%). (Б) Легка обструкція дихальних шляхів після першого курсу прийому ісавуконазолу в липні 2015 року (ОФВ 1 2,12 л, ОФК 3,09 л, ОФВ 1/ОФК 69%). (C) Крива нормального обсягу потоку після другого курсу прийому ісавуконазолу в липні 2016 року (ОФВ1 2,43 л, FVC 3,39 л, ОФВ 1/FVC 72%).
ОГЛЯД ЛІТЕРАТУРИ
Ми виявили 3 рандомізовані клінічні випробування та 16 спостережних досліджень (7 обсертаційних когортних досліджень, 1 серія випадків та 8 повідомлень про випадки) ітраконазолу, вориконазолу, позаконазолу та небулайзованого амфотерицину В для лікування АБРА у пацієнтів з астмою (табл.
Таблиця 1.
Вибірковий огляд літератури протигрибкової терапії для лікування ABPA у пацієнтів з астмою
| Якобс та ін | Поточний звіт про справу | N = 1 | Ісавуконазол 200 мг 3 ×/день × 2 дні, потім 200 мг щодня | Симптоми ПФТ Біомаркери Кортикостероїди | o Симптоматичне поліпшення o Покращення рівня ОФВ1 та ПВК o Зниження загального IgE o Зниження кількості інгаляційних кортикостероїдів | Діарея |
| Де Боле та ін. [11] | Перспективне спостережне когортне дослідження | N = 5 (із 137 пацієнтів з різними формами аспергільозу) | Ітраконазол | Симптоми Мікробіологія | o Симптоматичне поліпшення у 4 з 5 пацієнтів o Стерилізація посівів мокротиння у 3 з 4 пацієнтів із зростанням видів Aspergillus на вихідному рівні | Серед загальної когорти (N = 137) 18% мали несприятливі наслідки. Найчастіше спостерігалися диспепсія, біль у животі, нудота, діарея, запаморочення. |
| Деннінг та ін. [12] | Серія корпусів | N = 6 (N = 3 при астмі) | Ітраконазол по 200 мг двічі на день | Симптоми Біомаркери Кортикостероїди | o Симптоматичне поліпшення у 3 з 3 пацієнтів o Зниження рівня IgE у сироватці крові на ≥50% у 2 з 3 пацієнтів o Зниження потреби в кортикостероїдах у 1 з 3 пацієнтів | Зниження лібідо |
| Пачеко та ін. [13] | Звіт про справу | N = 1 | Ітраконазол 200 мг/добу | Біомаркери ПФТ Кортикостероїди | o Зниження рівня IgG в сироватці крові, специфічного для Aspergillus o Покращення показника ОФВ1 на 19% та показника ОФК на 28% o Зниження потреби в кортикостероїдах | Не вказано |
| Жермо і Туше [14] | Наглядове когортне дослідження | N = 12 (N = 9 при астмі) | Ітраконазол 200 мг/добу | Симптоми Біомаркери Кортикостероїди | o Загальна відповідь (клінічна, лабораторна, рентгенологічна) у 11 пацієнтів o Зниження середньої еозинофілії |
50%
o Зниження середнього рівня IgE в сироватці крові
Абревіатури: ABPA, алергічний бронхолегеневий аспергільоз; FEF, примусовий потік видиху; ОФВ1, об’єм форсованого видиху; FVC, примусова життєва ємність; Ig, імуноглобін; NAB, небулайзований амфотерицин В; NEB, небулайзований будесонід; PEF, піковий потік видиху; ПФТ, тести легеневої функції; RCT, рандомізоване клінічне випробування; SAFS, важка астма з грибковою сенсибілізацією.
a Протигрибкові засоби включають ітраконазол, вориконазол, позаконазол, ісавуконазол, NAB.
b Результати включають лише 20 пацієнтів з ABPA.
ОБГОВОРЕННЯ
Наскільки нам відомо, це перший звіт про використання ісавуконазолу для лікування АБРА. На основі сприятливої клінічної та фізіологічної відповіді цього пацієнта на ісавуконазол, ми вважаємо, що ісавуконазол є життєздатним варіантом лікування для пацієнтів з АБРА.
Ісавуконазоній сульфат є проліком активної триазольної частини, ісавуконазолом. Подібно до інших триазолів, ізавуконазол запобігає синтезу мембрани клітин грибка шляхом інгібування ланостерол-14α-деметилази. Ісавуконазол має активність in vitro щодо багатьох дріжджів і цвілі, включаючи види Aspergillus, Mucorales, Fusarium та демісіозні цвілі.
Ісавуконазол зменшує грибкове навантаження та покращує клінічні результати на експериментальних моделях дисемінованого кандидозу та аспергільозу [6, 7]. У людях рандомізоване контрольоване клінічне випробування пацієнтів з інвазивним аспергільозом та іншими ниткоподібними грибковими інфекціями (дослідження SECURE) продемонструвало, що ізавуконазол мав порівнянні показники виживання з вориконазолом, був безпечнішим і краще переносився [8]. Це дослідження, в поєднанні з доклінічними даними, призвело до затвердження ізавуконазолу для первинної терапії інвазивного аспергільозу в США та Європі в 2015 році.
Пацієнтка, про яку повідомляється в цьому документі, добре переносила ізавуконазол, мала помітне симптоматичне поліпшення та продемонструвала вражаючу фізіологічну реакцію, оскільки її співвідношення FEV1/FVC нормалізувалось вперше за 7 років після діагностики ABPA. Цей вплив на ПФТ після прийому ісавуконазолу свідчить про те, що він був ефективнішим, ніж вориконазол, хоча ми не можемо виключити можливість того, що попередні курси вориконазолу або поліпшення лікування симптомів астми також сприяли різниці. Варто зазначити, що ізавуконазол також мав кортикостероїднозберігаючий ефект для пацієнта, зменшуючи тим самим ризик короткочасних та довгострокових побічних ефектів.
Потенційним поясненням відносно більшої реакції на лікування ізавуконазолом у порівнянні з вориконазолом є те, що ізавуконазол досяг вищої експозиції лікарського засобу та більш швидкого кліренсу організму в порівнянні з вориконазолом, для якого терапевтичний моніторинг лікарських засобів не проводився. Альтернативним поясненням субтерапевтичних концентрацій вориконазолу може бути явище аутоіндукції [9]. Перевагою ісавуконазолу є його передбачувана лінійна фармакокінетика.
Лікування ізавуконазолом, як правило, безпечне та добре переноситься, що є ключовою відмінною рисою препарату порівняно з іншими методами лікування ABPA. Унікальні побічні реакції серед пацієнтів, які отримують вориконазол, включають тимчасові зміни зору, зорові галюцинації та світлочутливість [4]. Серед пацієнтів, які перебувають на тривалій терапії, викликають занепокоєння періостит та плоскоклітинний рак. Ітраконазол асоціюється з розладами шлунково-кишкового тракту, застійною серцевою недостатністю, висипом та підвищенням рівня печінкових ферментів. Позаконазол пов’язаний із розладом шлунково-кишкового тракту залежно від рецептури, і є рідкісні дані, що підтверджують його застосування для АБРА. Небулізований амфотерицин В викликає кашель та бронхоспазм під час інгаляції [10].
ВИСНОВКИ
Підводячи підсумок, ми представляємо перший звіт про пацієнта з основною астмою та АБРА, який успішно лікується ізавуконазолом з мінімальними побічними ефектами. На основі цього звіту про випадки ми пропонуємо розглянути відкрите або рандомізоване дослідження ізавуконазолу проти вориконазолу для лікування АБРА у пацієнтів з основною астмою.
Подяка
Т. Дж. В. - науковий співробітник Фонду «Врятуй наших хворих дітей» та науковий співробітник Фонду гострих сімей у галузі дитячих інфекційних захворювань.
Фінансова підтримка. Цю роботу частково фінансував Фонд "Врятуй наших хворих дітей" (Т. Дж. В.).
Потенційні конфлікти інтересів. Т. Дж. В. отримав гранти на наукові дослідження з експериментальної та клінічної антимікробної фармакотерапії від Astellas, Cubist, Novartis, Merck, Pfizer, Allergan та Theravance. Він також працював консультантом Astellas, ContraFect, Cubist, Drais, iCo, Novartis, Pfizer, Methylgene, SigmaTau та Trius. Усі автори подали форму ICMJE для розкриття потенційних конфліктів інтересів. Розкрито конфлікти, які редактори вважають відповідними до змісту рукопису.
- Успішне лікування у дитини з артритом, пов’язаним з ентезитом, що зачіпає грудино-ключичний
- Програма NIOSH FACE, Мічиган, звіт про справу 01MI006 CDCNIOSH
- Оптичний неврит як ізольоване прояв лептоменінгеального карциноматозу
- Тіосульфат натрію - нове лікування кальцифілаксії у хворих на діаліз - FullText - Випадок
- ОСТЕОХОНДРИТС ДИСКАНСИ РАДІАЛЬНОЇ ГОЛОВИ У МОЛОДОГО СПОРТСМОНА