Тривожна поведінка та гіпокампальний nNOS у відповідь на ожиріння, спричинене дієтою, у поєднанні з фізичними вправами
Анотація
Дієта з високим вмістом жиру (HFD) і стан із зайвою вагою можуть спричинити дисфункцію гіпокампа, що призводить до депресії та тривоги. Вправи сприятливо впливають на емоційну поведінку. Раніше ми повідомляли, що тренувальні вправи рятують від надмірної експресії гіпокампа нейрональної оксиду азоту синтази (nNOS), яка є ключовим регулятором тривожності. Тут ми досліджували поведінку, подібну до тривожності, та експресію nNOS у гіпокампалі у відповідь на HFD у поєднанні з фізичними вправами. Мишей призначали до стандартної дієти, HFD або HFD з групами фізичних вправ протягом 12 тижнів. Ми виявили, що фізичні вправи протягом останніх 6 тижнів режиму HFD покращили 12 тижнів індукованої HFD дефекації, супроводжуваної врятуванням надлишкової експресії nNOS. Однак показники тривожності в підвищеному плюс-лабіринті не змінились. Ці ефекти не були очевидними лише через 1 тиждень фізичних вправ. На закінчення, 6 тижнів фізичних вправ зменшили тривожність, пов’язану з ВЧС, згідно з одним із наших заходів (дефекація), і змінили зміни в шляху nNOS/NO в гіпокампах.
Вступ
Світова поширеність ожиріння, яке є важливим фактором тягаря хвороб, швидко зростає. Надмірне споживання жиру збільшує ризик надмірної ваги та ожиріння, які були пов’язані з психічними розладами [1, 2]. Епідеміологічні дослідження показали, що споживання західної дієти та стан надмірної ваги пов’язані з меншим об’ємом гіпокампа [3, 4] та психічними розладами, такими як тривога [2, 5]. Однак, як стверджують Eyres та співавт., Відсутні вагомі докази сприятливого впливу втрати ваги, спричиненого дієтою, на тривожність у осіб із ожирінням [6]. Тому, схоже, необхідні додаткові втручання не тільки для поліпшення ожиріння, але й симптомів тривоги у людей із ожирінням.
Матеріали і методи
Тварини
Вісімдесят самців мишей C57BL/6 J (віком 4 тижні; Японія SLC, Сідзуока, Японія) утримувались при температурі (23,5 ± 0,7 ° C), вологості (34,0 ± 5,7%) та світлі (12-годинний цикл світло-темрява ) контрольований об'єкт. Тварини отримували стандартну чау та воду за бажанням. Усі експерименти були схвалені Комітетом з догляду та використання тварин Університету Фукуока.
HFD та тренування
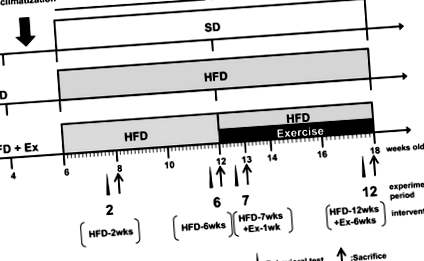
Протокол HFD та тренувань щодо фізичних вправ відповідав попереднім описанням [21]. Коротко кажучи, через 2 тижні акліматизації мишей розділили на три групи: група зі стандартною дієтою (SD) (n = 24) годували стандартною дієтою (CE-7, CLEA Японія, Токіо, Японія; 62% вуглеводів, 14% жирів і 25% білка), група HFD (n = 28) годували HFD (HFD-32, CLEA Японія, Токіо, Японія; 23% вуглеводів, 57% жиру та 20% білка) та HFD + Ex (n = 28) групу годували HFD-32 протягом 12-тижневого експериментального періоду, і їй дозволяли добровільно займатися на робочому колесі протягом останніх 6 тижнів експерименту. Як групи HFD, так і HFD + Ex вирощувались у клітках з робочим колесом, але лише група HFD + Ex мала право вільного доступу до робочого колеса протягом останніх 6 тижнів експерименту. Вага тіла та кількість обертань колеса вимірювали кожну другу добу. Загальна відстань пробігу розраховувалася на основі підрахунку обертання колеса. Ми провели поведінкові тести 2 (n = 6/група), 6 (n = 6–7/група), 7 (1 тиждень фізичних вправ, n = 6–7/група) та 12 тижнів (6 тижнів фізичних вправ, n = 6–7/група) в експериментальну сесію, а потім жертвували мишами шляхом обезголовлення (рис. 1).
Схематичний вигляд експерименту. Цей дизайн дослідження був змінений на основі попереднього дослідження [21]. Мишей з HFD годували дієтою з високим вмістом жиру протягом 12-тижневого експериментального періоду. Мишей HFD + Ex годували дієтою з високим вмістом жиру протягом 12-тижневого експериментального періоду і надавали добровільний доступ до бігового колеса з 12-тижневого віку до кінця експерименту. Миші проводили поведінкові тести через 2, 6, 7 та 12 тижнів. Через три дні після поведінкових тестів мишей вбивали шляхом обезголовлення
Тестування поведінки
Ми оцінили поведінку, схожу на тривогу, за допомогою підвищеного плюсового лабіринту (EPM), за 3 дні до жертви (рис. 1). Всі випробування проводили між 13:00 та 16:00 під час світлового періоду (80–100 lx). Перед кожним випробуванням випробувальний прилад ретельно очищали 70% (об./Об.) Етанолом і сушили для зменшення присутності нюхових сигналів.
Ми провели тест EPM відповідно до протоколу Nishijima et al. [22]. Коротко кажучи, лабіринт складався з чотирьох рук (кожна 30 см завдовжки і 5 см завширшки) на 40 см над підлогою. Дві раки містили бічні та торцеві стінки висотою 15 см (закриті рамена), а інші дві рами не мали стін (розкриті рамена). Ми зафіксували поведінку миші за допомогою відеокамери. Мишей розміщували в центрі лабіринту таким чином, що вони стикалися з розкритою рукою, і дозволяли їм досліджувати протягом 5 хв. Наступні параметри вимірювались вручну: (1) кількість входів у відкрите плече; (2) загальна кількість входів у руки (загальна кількість входів у руку = входи у відкриту руку + записи у закриту руку, раз); (3) відсоток входів з відкритим озброєнням (вхід з відкритим озброєнням/загальний об'єм входів × 100); (4) дефекація (разів).
Підготовка тканин
Через три дні після ЕРМ мишей забивали декапітацією після 6 год голодування. Гіпокампу швидко збирали та гомогенізували за допомогою пінцета, щоб уникнути специфічності регіону. Потім частини тканини гіпокампа заморожували в рідкому азоті для аналізу білка. Для аналізу експресії генів частину тканини гіпокампа швидко занурювали у розчин для стабілізації РНК (Ambion, Austin, TX). Всі зразки зберігали при - 80 ° C для подальшого біохімічного аналізу.
Вестерн-блот-аналіз
Експресія гена
Рівні експресії гена nNOS визначали, як описано раніше [21]. Тканину гіпокампа мишей SD, HFD та HFD + Ex гомогенізували за допомогою гомогенізатора Polytron. Загальну РНК витягували з усіх зразків за допомогою системи Maxwell ® 16 LEV (Promega, Токіо, Японія). Ми провели RT-PCR-аналіз у реальному часі за допомогою системи ПЛР Step One у реальному часі (Applied Biosystems), використовуючи зонди для аналізу експресії генів TaqMan для аналізу рівня мРНК nNOS (No1-Mm00435175_m1; Прикладні біосистеми, Фостер-Сіті, Каліфорнія). Рівні мРНК nNOS були нормалізовані до рівнів мРНК GAPDH (Gapdh-Mm99999915_g1; Applied Biosystems) та кількісно визначені за допомогою методу ΔΔCt.
Статистика
Дані відображаються як середнє значення ± значення SE. Всі статистичні аналізи проводились із використанням призми версії 7.0 (GraphPad Software, Сан-Дієго, Каліфорнія). Ми використовували Student's т-тести для оцінки поведінкових параметрів, рівня білка та експресії генів на 2 та 6 тижні (SD та HFD). Непараметричні дані оцінювали за допомогою Манна – Уітні U тест. Ми використовували односторонню ANOVA, а потім постхок-тест Бонферроні, щоб провести групові порівняння параметрів поведінки, рівня білка та експресії генів на 7 та 12 тижнях (SD, HFD та HFD + Ex). Непараметричні дані оцінювали за допомогою критерію Крускала – Уолліса. Кореляції обчислювались за допомогою кореляційних характеристик продукту і моменту Пірсона. A P значення
Результати
Вплив HFD та фізичних вправ на масу тіла та жирову масу через 2, 6, 7 та 12 тижнів
Споживання HFD призвело до швидкого збільшення маси тіла та маси вісцерального жиру на 2 тижні (рис. 2а, б). Це збільшення маси тіла та маси жирової прокладки у мишей HFD продовжувалося через 6, 7 та 12 тижнів порівняно з мишами SD (P Рис.2
Вплив HFD на поведінку, схожу на тривогу, та шлях nNOS/NO через 2 тижні
Через 2 тижні споживання HFD ми спостерігали зміни у поведінці, подібній до тривоги, у EPM (рис. 3). Ми виявили значні відмінності в кількості відкритих входів (P Рис.3
Білок nNOS у гіпокампалі, експресія генів та рівень фосфорилювання не змінювались при споживанні HFD через 2 тижні (рис. 3e – i). Рівні pAkt Ser473 значно зросли, а рівні CREB та pCREB ser133 зменшились у мишей HFD (рис. 3j, l, m).
Вплив HFD на поведінку, схожу на тривогу, та шлях nNOS/NO через 6 тижнів
Через 6 тижнів ми не виявили суттєвих відмінностей у будь-яких тестованих параметрах, включаючи вхід у відкриту руку (рис. 4а), загальну кількість входів у руки (рис. 4б), відсоток входів у відкриту руку в загальній кількості входів у руки (рис. 4в) та дефекація (рис. 4г) між мишами SD та HFD. Хоча 6 тижнів споживання HFD не впливали на експресію білка nNOS у гіпокампах та інші молекули, пов’язані з nNOS/NO, рівні експресії гена nNOS значно збільшились (рис. 4e – m).
Вплив HFD та 1 тиждень фізичних вправ на поведінку, подібну до тривоги, та шлях nNOS/NO через 7 тижнів
Хоча це не було статистично значущим, порівняно з групою SD, загальна кількість випадків введення групи зменшилась у групі HFD через 7 тижнів (P = 0,07, рис. 5б). Відсоток відкритих груп входів у загальну кількість входів у групи значно зменшився у мишей HFD + Ex (рис. 5в). Ми спостерігали дефекацію в групах SD та HFD, але не в групі HFD + Ex. Однак ми не виявили значущих відмінностей між групами (рис. 5г). Ці результати свідчать про те, що на виміряні поведінкові параметри частково впливав споживання ВЧЧ, але не фізичні вправи. Через 7 тижнів рівень експресії nNOS в гіпокампах значно збільшився у мишей з HFD (P Рівні Ser1412/GAPDH та pAkt Ser473 зростали із споживанням HFD та зменшувались під час фізичних вправ (рис. 5g, j). Рівні pCREB Ser133 були незмінними у всіх групах (рис. 5л).
Вплив HFD та 6 тижнів фізичних вправ на поведінку, схожу на тривогу, та шлях nNOS/NO через 12 тижнів
У кінцевий момент часу (рис. 6, 12 тижнів споживання HFD з 6-тижневим тренуванням) входи у відкриту руку та відсоток входів у відкриту руку в загальній кількості входів у руки були однаковими у групах HFD та SD (рис. 6а, в). Однак відсоток відкритих груп входів у загальній кількості входів (P Ser1412 та AktSer473 виявилися незмінними внаслідок споживання HFD та фізичних вправ (рис. 6g, h, j). Фосфорилювання CREB Ser133 у мишей HFD + Ex було значно вищим, ніж у мишей HFD (рис. 6l). Ці результати вказують на те, що 6 тижнів фізичних вправ під час споживання HFD покращують поведінку, схожу на тривогу, модулюючи шлях nNOS/NO в гіпокампалі.
Взаємозв'язок між рівнем експресії білка nNOS у гіпокампалі та масою тіла або масою вісцерального жиру
Далі ми дослідили можливі фактори, що сприяють спостережуваним змінам рівня експресії білка nNOS в гіпокампалі. Через 2 і 6 тижнів рівні експресії nNOS не асоціювались з масою тіла або масою вісцерального жиру (рис. 7а, б, е, е). Однак через 7 тижнів рівні експресії nNOS суттєво корелювали з вагою тіла (р = 0,59, P Рис.7
Кореляція між рівнем експресії білка nNOS в гіпокампалі та масою тіла (a, b, c, і d), а також відносна вісцеральна маса жиру (e, f, g, h) через 2 тижні (a, e), 6 тижнів (b, f), 7 тижнів (c, g), і 12 тижнів (d, h). Відкриті кола, група SD; світло-сірі кола, група HFD; темно-сірі кола, HFD + Ex група. Лінії на діаграмах розсіювання демонструють суттєві кореляційні зв’язки (за тестом кореляції між продуктом і моментом Пірсона)
Обговорення
Основними висновками цього дослідження були: (1) споживання HFD збільшило рівень експресії білка nNOS гіпокампа; (2) тренування з фізичними вправами змінила експресію nNOS в гіпокампах та зменшила тривожність, пов’язану з ВЧЧ, згідно з одним із наших двох заходів; та (3) експресія nNOS в гіпокампах корелювала з вагою жиру/масою тіла через 7 та 12 тижнів.
Два тижні споживання HFD суттєво зменшили вхід у відкриту руку та відсоток відкритих/загальних входів у руку. Однак рівні експресії nNOS у гіпокампах не змінювались протягом 2 тижнів споживання HFD. Крім того, 6 тижнів споживання HFD, схоже, не змінювали виміряні поведінкові параметри або рівні експресії nNOS в гіпокампалі. Відповідно до наших результатів, Gainey et al. [23] повідомляв, що HFD асоціюється із підвищеною поведінкою, подібною до тривожності, через 3 тижні споживання HFD, але не через 1 або 6 тижнів. Інше дослідження показало, що споживання HFD було пов’язано зі зменшенням часу, проведеного у відкритих обіймах тесту EPM на 1 тиждень, але не на 3 тижні [24]. Отже, виявляється, що минуща тривога була спричинена на початкових стадіях споживання HFD, хоча механізми, що лежать в основі цього явища, досі незрозумілі. Наші висновки про те, що експресія nNOS в гіпокампалі збільшувалась з часом експерименту, вказують на те, що механізми регулювання настрою, спричиненого ожирінням, шляхом nNOS/NO відрізняються між ранніми та пізніми стадіями ожиріння.
На закінчення, наші результати демонструють, що 7 і 12 тижнів споживання HFD збільшували рівень експресії nNOS в гіпокампалі. Крім того, 6 тижнів фізичних вправ відновлювали експресію nNOS у гіпокампалі та покращували тривалість тривоги, пов’язаної з HFD, через 12 тижнів відповідно до відновлення рівня дефекації. Однак ми не виявили відмінностей у тривожності, виміряних EPM. Крім того, рівні експресії nNOS в гіпокампах були пов'язані з масою тіла та масою вісцерального жиру при ожирінні, спричиненому HFD.
Список літератури
Такасе К, Цунеока Ю, Ода С та співавт. (2016) Харчування з високим вмістом жиру змінює нюхові, соціальні та винагородні поведінки мишей, незалежно від ожиріння. Ожиріння 24: 886–894
Jacka FN, Pasco JA, Mykletun A et al (2010) Асоціація західних та традиційних дієт з депресією та тривогою у жінок. Am J Psychiatry 167: 305–311
- 135 ЕФЕКТИ ОЖИРІННЯ ТА ВІТАМІНУ Д В ОТВІТІ ТІЛА НА ВАКЦИНУ проти гепатиту В BMJ Відкрити
- Бетулінова кислота пригнічує ожиріння, спричинене дієтами, і покращує енергетичний баланс, активуючи
- Дані про рівень ожиріння серед дорослих для Парафії Вознесіння, штат Лос-Анджелес, і округу Комаль, штат Техас - поведінка здоров’я
- Байкалін послаблює ожиріння, спричинене дієтою, ожиріння та дисфункцію печінки, реакцію на дозу та потенціал
- Дані про рівень ожиріння серед дорослих для округу Олбані, штат Нью-Йорк, та округу Нью-Лондон, штат Коннектикут - Здоров'я