Погляньте на останні статті
Споживання йоду з їжею, захворювання щитовидної залози та поширеність папілярної карциноми (ПТК)
Інститут онкології Джорджа Чжу, 422407, Пекін, Китай
Анотація
Йод - мікроелемент, який необхідний для синтезу гормону щитовидної залози. Як хронічний дефіцит йоду, так і надлишок йоду пов’язані з гіпертрофією та гіперплазією фолікулярних клітин та впливом тиреоїдного гормону (Т3, Т4) та тиреотропіну (ТТГ). Частота збільшення раку щитовидної залози зростає після опромінення 131I у дітей або альдолесцентів. Відповідно, надлишковий зоб йоду в їжі, індукований йодом гіпертиреоз (IIH) та ІІТ, споживання йоду та поширеність папілярної карциноми (PTC), а також дослідження випадків та когортні дослідження раку щитовидної залози та споживання морепродуктів та молочних продуктів, були переглянуті. Більше того, наявні докази онкогенних мутантів рецепторів гормонів щитовидної залози в експериментах на тваринах та клінічних дослідженнях були зміщенням в бік онкогенної функції раку щитовидної залози людини, а також її цільової терапії.
Ключові слова
Надлишковий зоб йоду, IIH та IIT, картина папілярної карциноми (PTC), мутанти онкогенних рецепторів гормонів щитовидної залози
Вступ
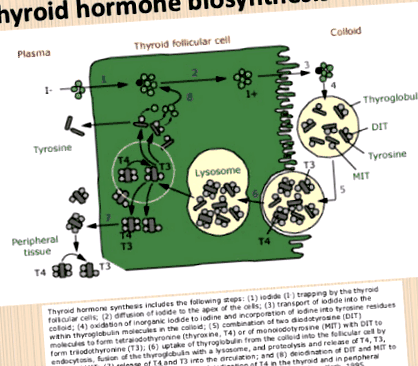
Основна функція щитовидної залози - виробляти гормони (рис. 1) [1]. Т4 і Т3, які є важливими для регуляції метаболічних ефектів, наприклад, посилений ліпогенез, кетогенез, клітинна проліферація та диференціація, такі як швидкий розвиток жаб з тиректомізованих пуголовків, індукція гормону росту в гіпофізі та розвиток мозку. у новонароджених шляхом сприяння дендриту форматиїну та мієлінізації.
Фігура 1. Біосинтез гормону щитовидної залози.
Малюнок 2. Йодування Т4 за залишком 5 в ланцюзі Tg.
Індукція новоутворення щитовидної залози у щурів
У щурів розвиток новоутворень щитовидної залози після радіоактивного йоду було добре встановлено в попередніх порівняльних експериментах у 1950-1964 рр. Минулого століття [5-8]. Недавні ефекти, що сприяють пухлині щитовидної залози, спричинені дефіцитом та надлишком йоду, також досліджувались на двоступеневих моделях у щурам, яким давали канцерогени, такі як N-біс (2-гідроксипропіл) -нітрозамін (BHPN) або N-нітрозометилуреа (NMU). У щурів вплив N-нітрозобісу (2-гідроксипропіл) аміну (BHP) та надмірна йодна дієта [9 ], захворюваність на рак щитовидної залози становила 29% у тих, хто харчувався надмірною йодною дієтою, проти 33% у тих, хто харчувався достатньою кількістю йоду. Kanno та ін. [10] вивчав потенційні наслідки дефіциту та надлишку йоду, що стимулюють пухлину щитовидної залози, протягом 26 тижнів у щурів, яким давали фізіологічний розчин або BHPN. У щурів, які отримували фізіологічний розчин, поодинокий дефіцит або надлишок йоду не був канцерогенним, але у щурів, оброблених BHPN, і йодом дефіцит і надлишок збільшених фолікулярних пухлин щитовидної залози, дефіцит йоду має помітно сильніший ефект (рис. 3а). Частота щурів з доброякісними вузликами становила 100% в обох групах. Boltze [11] годував щурів понад пероїдом висотою 110 тижнів (
В 10 разів нормальний), нормальний і низький (
0,1 рази від нормального) щоденного споживання йоду і піддавали їх одноразовому зовнішньому опроміненню 4 сірими (Гр) або фіктивними випромінюваннями Поодинці як дефіцит йоду, так і надлишок збільшували швидкість проліферації тироцитів та індукували аденоми щитовидної залози, але не викликали карцином щитовидної залози. У поєднанні з радіацією дефіцит йоду та надлишок йоду індукують карциноми щитовидної залози (PTC та фолікулярні карциноми щитовидної залози, FTC) у 50-80% тварин, тоді як у тварин, що мають достатню кількість йоду, карциноми щитовидної залози не розвиваються (рис. 3b). Ці дані свідчать про те, що як тривалого дефіциту йоду, так і його надлишку недостатньо для стимулювання канцерогенезу щитовидної залози, проте обидва сприяють канцерогенезу щитовидної залози, викликаному радіацією. Ці менш переконливі дані свідчать про те, що надлишок йоду може бути слабким промотором раку щитовидної залози.
Малюнок 3. Поширеність пухлин у тварин проти споживання йоду. a Поширеність тварин з аденомою щитовидної залози та карциномою щитовидної залози на 26 тижні після одноразової дози 2,8 мг/кг DHPN на 2 тижні та під час однієї із семи довготривалих, недостатніх або надмірних дієт йоду (дефіцит споживання: 0,25, 0,4, 0,55, 0,84 мкг/добу; нормальне споживання: 2,6 мкг/добу; надмірне споживання: 760, 3000 мкг/добу). b Поширеність тварин з аденомою щитовидної залози та карциномою щитовидної залози на 110 тижні після одноразового впливу зовнішнього випромінювання 4 Гр на 6 тижні та під час однієї з трьох довготривалих недостатніх, достатніх або надмірних дієт йоду (недостатнє споживання: 0,42 мкг/100 г маса тіла/добу; нормальне споживання: 7 мкг/100 г маси тіла/добу; надмірне споживання: 72 мкг/100 г маси тіла/добу). Затінена область: діапазон нормального споживання йоду.
Радіаційне опромінення та ризик раку щитовидної залози у людини
Зовнішня радіація щитовидної залози збільшує ризик раку щитовидної залози, особливо коли радіація відбувається у дітей або підлітків [12-20]. Ядерна аварія на ЧАЕС у 1986 році піддала населення Білорусі, України та Російської Федерації внутрішньому опроміненню радіоактивними йодами в щитовидній залозі, що призводить до різкого збільшення раку щитовидної залози у дітей та підлітків [18]. Близько 60% білоруського раку щитовидної залози та 30% українських випадків, переважно ПТК, були виявлені приблизно через 20 років після аварії [21]. Історично склалося так, що райони, що зазнали наслідків Чорнобильської катастрофи, зазнавали різного ступеня минулого дефіциту йоду [22]. Хронічний дефіцит йоду збільшує тиреоїдний кліренс йоду в плазмі, збільшує кровотік і проліферацію тироцитів у щитовидній залозі та збільшує розмір щитовидної залози. поглинання радіойодів, що потрапили всередину, також збільшуючи вразливість щитовидної залози до накопичених радіойодів [15,23]. Зоб в анамнезі був пов'язаний з ризиком раку щитовидної залози (АБО 2.19), але дослідження було обмеженим через невелику кількість раку справи (n = 45) [17,20].
Йод із надлишком зоба - різноманітний етіологічний підтип зоба
У 7-9 років середнє значення об’єму щитовидної залози становило 4,7 мл (нормальні діти 4,0–4,8 мл) [24]. Основний висновок про тісну кореляцію між збільшенням об’єму щитовидної залози та великим споживанням йоду у дітей заснований головним чином на дані з узбережжя Хоккайдо у 1962-69 рр. Частота ендемічного зобного зобу серед студентів становила від 6,8% до 8,9%, але ніколи не було задокументовано, що вона була б> 25% [25,26]. Niepominszoze [27] досліджував епідеміологію пальпируемого зоба серед населення столичного району Великого Буенас-Айреса (11 мільйонів жителів), що має достатню кількість йоду. У випадковій групі поширеність зоба становила 8,7%, тоді як у індукованій групі, яка робить висновок серед родичів пацієнтів із розладами щитовидної залози та іншими скаргами, вона заявляла 14,4%. Обидві групи в основному складалися з жінок (87,2%). Дані представлені першими, що виникли в результаті скринінгового обстеження, проведеного серед великої кількості йоду, достатньої для населення Південної Американського континенту.
Для вивчення впливу надлишку йоду та надлишку тирозину на зоб у мишей [28], корм з високим вмістом йоду (високий вміст йоду та адекватний тирозин, HIAT) може призвести до типового колоїдного зобу у мишей, а рівень зобу становить 89,5%, тоді як 35% зоб спостерігався як при надлишку йоду, так і при тирозині (HIHT), а лише при високому тирозині (AIHT) (рис. 4) не спостерігався зоб, що означає, що йод і тирозин відігравали важливу роль у зобі, а надлишок йоду мав помітно сильніший ефект ефект, який характеризується великими фолікулами з плоским епітелієм та рясним колоїдом, змішаним з нормальними або більшими за розміром фолікулами, вистеленими епітелієм підвищеної маси щитовидної залози. Більше того, існувала позитивна взаємозв'язок між дозою зобів мишей та дозою йоду (KI) [29]. Диференціальна швидкість зоба 10%, 50% та 90% може бути індукована питною водою, що містить різні дози йоду відповідно 250, 1500 та 3000 мкг/Л відповідно. Доза йоду 250 мкг/л змогла викликати колоїдний зоб у мишей. Висновки були сумісні з епідеміологічними результатами авторів у людині. Вміст йоду у питній воді становив 244,63, 533,83, 963,75 та 1570,0 мкг/л проти 6,4%, 32,4%, 37,14% та 43,71% зоба відповідно [29].
Малюнок 4. Зоб з високим вмістом йоду в золі щурів.
Накопичені дані, за останні десятиліття було зареєстровано щонайменше 46 випадків зобу у людини, пов’язаного з йодом (KI, Na I, розчин Lu gol та антиаритмічний засіб аміодарон). Згідно з епідеміологією, в Китаї частота йодового зоба на дієті з клубком солі була 16% (вміст йоду 1089,2 мкг/кг); та 28,36% (загалом 4344 аналізи) частота випадків йодного зоба у вищих поїлок йоду з глибокої криниці (вміст йоду 661,2 мкг/л) порівняно з 8,37% (4158) зоба у поїлок з низьким вмістом йоду (вміст йоду 27,2 мкг/л ) [30]. У Китаї рівень готела у дітей в районах із надмірною йодною вмістом йодованої солі був вищим, ніж у йодованої солі, 12,1% проти 8,6% [31]. У Цзінані серед 725 мешканців розслідування показник зобів щитовидної залози становив 4,8% (35/725) .МІК (концентрація йоду в сечі) у 725 суб'єктів з 29 сільських районів становила 327,0 мкг/л (діапазон 35-2938,5 г/л), а вміст йоду у воді в 376 пробах питної води в середньому становив 112,1 ± 91,3 мкг/л, 90,3 мкг/л (діапазон 0,5-605,2 мкг/л у середовищі) [32]. У таблиці 1 частково представлена частота зустрічальності берегового зоба, як показано нижче.
Таблиця 1. Ендемічний зоб з надлишком йоду в узбережжі, Китай (Дані Yu ZH, etal, 2001 [30]).
Рік
Провінція
Сільські райони
Йод води (мкг/л)
Йод сечі (мкг/л)
Захворюваність на зоб (%)
28,36 (всього 4344 аналізи)
Індукований йодом гіпертиреоз (ІІТ) та тиреотоксикоз (ІІТ)
Згідно з вищезазначеними ВООЗ у 1994 р. [33] та Корейськими центрами контролю та профілактики захворювань (KCDC) у 2012 р. [34]] харчові продукти, такі як перероблені, сільськогосподарські, м’ясні та морські продукти, контролювались для вимірювання дієтичного йоду. Рекомендована добова доза йоду 70-150 мкг [35]. Надлишок йоду через дієтичне вживання їжі, ліків або інших йодовмісних сполук може призвести до зобу [36-37], гіпертиреозу [38-45], тиреоїдиту Гашимото [46]. ] та тиреотоксикоз [47-54] через посилення синтезу гормонів щитовидної залози за наявності основного захворювання щитовидної залози, особливо багатовузлових зобів, що містять раніше існуючу область автономної функції. У 1958 р., Запровадивши йодид калію (KI) з метою профілактики зобу французькою мовою, багато студентів розробили йодний зоб з пероральним високим дозуванням 1% KI або 10 мг KI на день. До цього часу в літературі було принаймні 22 повідомлення про випадки IIH або IIT. Йодид потасуму (KI) при концентрації 10-4-10-7 моль/л стимулює проліферацію клітин ДГПЖ від раку щитовидної залози 10-3, підвищення рівня Т3 і Т4 у сироватці крові, підвищення рівня мРНК і білка D1 цикліну. У щурів сироватковий тироксин (TT4, FT4, rT3) був вищим у вищому йоді, ніж результат у нижчому йоді [55-57].
Таблиця I. Йодовмісні сполуки, потенційно пов'язані з ІІТ
Радіологічні контрастні речовини: Діатрізоат, іпанова кислота, іподат, йоталамат, метризамід, йопромід, йопамідол, йотролан.
Місцевий препарат йоду: Йодна настоянка, повідон йод (Бетадин), йодоформна марля.
Рішення: насичений йодид калію, розчин Люголя, йодований гліцерин (органідин), йодид ехотіопату, сироп гідродієвої кислоти.
Наркотики: Аміодарон, вітаміни, що містять йод, йодид калію, йодид ізопропаміду.
Харчові компоненти: ламінарія, комбу та інші морські водорості, сполуки йоду в хлібі, тиреоїдит гамбургера.
Аміодарон є найпоширенішим джерелом йоду в США. Індукований аміодароном тиреотоксикоз (АІТ) I типу є результатом збільшення йоду в синтезі тироксину (200 мг аміодарону, що містить 75 мг йоду). У пацієнтів, у яких розвивається АІТ I типу, зазвичай буває вузловий зоб, що передує. AIT II типу спричинений цитотоксичною дією ліків, що призводить до вивільнення попередньо утвореного тироксину [48]. AIT виникає пізно після відміни аміодарону [59].
Ламінарія - це великі морські водорості, що належать до бурих водоростей і класифікуються в порядку Laminariales, і є важливим джерелом їжі в багатьох азіатських культурах [60]. Вимірювали середній вміст йоду в ламінарії від 1500 до 2000 мкг/г [61-62]. Фітопрепарати, включаючи ламінарію та харчові добавки, що містять ламінарію, також використовуються все більшою кількістю пацієнтів [63]. Сузукі [23] першим повідомив про випадок ендемічного зобу на морському узбережжі після морських водоростей. В даний час зареєстровано щонайменше 8 пацієнтів з ІІГ або ІІТ після прийому ламінарії [60,64-69]. Ще 12 тиреотоксикозів, спричинених фітотерапією, що зменшує вагу [63]. У 2001 р. Чжу [70] повідомив про випадок новоутворення щитовидної залози після морських водоростей при раку молочної залози. З епідеміологічних досліджень серед корейського населення велике споживання йоду з морських продуктів може збільшити ризик раку щитовидної залози, особливо у жінок [71,72]. За накопиченими даними, морські водорості становлять близько 80% споживання йоду людьми Джапанази, споживання морських водоростей було чітко пов'язано з підвищений ризик розвитку папілярної карциноми (ПТК) у жінок у постменопаузі [73].
Споживання йоду в їжі та поширеність папілярної карциноми (ПТК)
Більше того, за даними Циммеранна в нещодавньому огляді [11] та Вільямса в попередньому огляді [22], існували повідомлення, що у країнах із високим споживанням йоду (США, Ісландія) співвідношення PTC: FTC коливалося від 3,4 до 6,5, тоді як у країнах із помірним споживанням йоду (Великобританія та північна Німеччина) це співвідношення становило від 1,6 до 3,7, а в країнах із низьким споживанням йоду (Аргентина, Колумбія, Фінляндія, Південна Німеччина, Австрія та Швейцарія) з 0,19 до 1,7. Захворюваність на ПТК у Нідерландах зростала на 2,1% на рік між 1989 і 2003 роками, що частково пояснювалося стабільним та достатнім споживанням йоду населенням Нідерландів протягом останніх 4 десятиліть, а також іншими низькими показниками радіаційного опромінення та випадково виявлених вузлів щитовидної залози [84]. На північному заході Іспанії йодована сіль була введена в 1985 р., Захворюваність на рак щитовидної залози зросла у жінок з 1,56/100 000 протягом 1978-1985 рр. До 8,23/100 000 у період з 1984 по 2001 рр. PTF: FTC збільшився з 2,3 до 11,5 [85]. Італія мала один із найвищих показників захворюваності на рак щитовидної залози, майже 20/100 000 жінок у 2007 році, частота раку щитовидної залози у жінок із холодними вузликами становила 5,3% в достатній кількості йоду (середня UIC 114 мкг/л) та 2,7% у область з дефіцитом йоду (середня інформація про редакцію UIC
Головний редактор
Чіро Рінальді
Університет імені Федеріко II Неаполь
Тип статті
Історія публікацій
Дата надходження: 02 грудня 2017 року
Дата прийняття: 14 лютого 2018 року
Дата публікації: 17 лютого 2018 р
- Харчова кислотна навантаження та споживання калію пов'язані з артеріальним тиском та поширеністю гіпертонії у
- Чи впливає споживання дієтичних напоїв на схему дієтичного споживання Результати від вибору здорового
- Порівняння дієтичного споживання та клінічних характеристик дорослих із ожирінням та нормальною вагою
- Женьшень Дієтична добавка як імуномодулятор при різних захворюваннях - ScienceDirect
- Приблизне споживання радіонуклідів у раціоні та ризики для здоров’я для жителів міста Фукусіма,