Порівняльний антиліпідемічний ефект введення N-ацетилцистеїну та кунжутного масла у мишей з гіперхолестеринемією, індукованих дієтою
Анотація
Передумови
Збільшується кількість нових антиліпідемічних методів лікування, що розглядаються. Передбачуваний гіполіпідемічний ефект N-ацетилцистеїну (NAC) та кунжутного масла вивчали на мишачій моделі гіперхолестеринемії, спричиненої дієтою.
Методи
Самці мишей C57bl/6 були віднесені до наступних груп: (NC) контрольна група, (HC) група, яка отримувала тестову дієту з доповненням 2% холестерину та 0,5% холінової кислоти протягом 8 тижнів, (HCN) група, яка отримувала тестову дієту з добавкою NAC (230 мг/кг перорально) та (HCS) групу годували тестовою дієтою, збагаченою 10% кунжутним маслом. Загальний рівень холестерину в сироватці крові, ЛПНЩ-холестерин, ЛПВЩ-холестерин та тригліцериди аналізували на початку та в кінці експерименту. Наприкінці експерименту в сироватці крові вимірювали загальний рівень пероксидів та оксиду азоту (NO). Ураження печінки та аорти оцінювали шляхом фарбування гематоксилін-еозином.
Результати
Вищі рівні загального та холестерину ЛПНЩ у сироватці крові були зареєстровані у всіх групах, які харчувались дієтою з високим рівнем холестерину. Група HCN показала знижений рівень ліпідів порівняно з групами HC і HCS. Ніяких відмінностей між HCS та HC групами не спостерігалось. Вміст перекису в сироватці крові помітно збільшився у мишей, які споживали дієту з високим рівнем холестерину. Введення NAC та кунжутного масла призвело до значного зменшення перекисного окислення ліпідів у сироватці крові на рівнях контрольної групи, тоді як лише NAC відновив біодоступність NO. Що стосується гістології печінки, ураження, що спостерігались у групі HCN, були менш серйозними, ніж ті, що спостерігались в інших групах з високим рівнем холестерину.
Висновок
Одночасне введення NAC, але не кунжутної олії, відновлювало порушений ліпідний профіль та покращувало стеатоз печінки у досліджених мишей з гіперхолестеринемічною дієтою. Обидва агенти покращують антиоксидантний захист сироватки крові.
Передумови
Гіперхолестеринемія у поєднанні з підвищеною концентрацією ЛПНЩ-холестерину є основними факторами ризику розвитку та прогресування атеросклерозу, а отже і серцево-судинних захворювань [1]. На основі цих доказів наукові дослідження спрямовані на відкриття нових препаратів з гіпохолестеринемічним ефектом. Сьогодні для профілактики дисліпідемії пропонуються дієтичні терапії на рослинній основі та натуральні харчові компоненти. Антиоксидант N-ацетилцистеїн (NAC), сірка органо з Цибуля рослини та кунжутна олія з’являються як перспективні гіполіпідемічні засоби в останній літературі.
NAC - це гідрофільна цистеїнвмісна сполука, природно утворена в Цибуля такі рослини, як часник і цибуля. Встановлено, що споживання цієї сполуки ефективно зменшує індукований триацилгліцерином (TAG) високий рівень насичених жирів та накопичення холестерину в печінці мишей. Більше того, було показано, що він захищає печінку від окисного пошкодження, спричиненого високим вмістом жиру [2].
Кунжут належить до виду Sesamum indicum (Педаліеві сім'я). Він широко використовувався як традиційна їжа на сході, але також вважається, що він має важливі лікувальні властивості. Існує безліч даних різних досліджень, в основному щодо видів гризунів, що підтримують гіполіпідемічну дію багатьох компонентів насіння кунжуту та його олії [3, 4]. Satchithanandam та співавт. [4] дійшли висновку, що поглинання лімфатичного холестерину у щурів, яких годували дієтами, що містять кунжутну олію, було приблизно на 50% менше, ніж у щурів, які харчувалися контрольною дієтою. Крім того, введення порошку знежиреного кунжутного насіння у гіперхолестеринемічних щурів-альбіносів покращило їх антиоксидантний статус та суттєво зменшило ліпіди в плазмі [5]. Наскільки нам відомо, на основі літератури немає даних про потенційні гіполіпідемічні ефекти введення кунжутного масла без заміщення інших жирових харчових сполук.
Отже, дане дослідження було проведено для того, щоб визначити, чи матиме введення NAC та кунжутного масла сприятливий гіполіпідемічний та антиоксидантний ефект у мишачої моделі, яка споживає дієту чау, збагачену холестерином та холевою кислотою.
Методи
Тварини
12-тижневих мишей C57bl/6 самців (Mus musculus) були отримані в Інституті Олександра Флемінга (Варі, Греція) і були акліматизовані за тиждень до початку експерименту. Тварин утримували в умовах контрольованої температури (23 ± 2 ° C) та вологості (60%) з 12-годинним циклом світло/темрява. Експериментальний протокол був розглянутий та схвалений Ветеринарним управлінням префектури Афін та Комітетом з етики Медичної школи Національного університету і Афінського університету Каподістрія, відповідно до етичних рекомендацій Директиви Ради Європейських Співтовариств від 24 листопада 1986 р. (86/609/ЄЕС).
Експериментальний дизайн
Всього 25 мишей було розділено на наступні 4 експериментальні групи:
Миші мали вільний доступ до їжі та пиття протягом усього дослідження. Протягом 8-тижневого періоду споживання їжі контролювали щодня, тоді як кількість споживаної води щодня також реєстрували в групі HCN. Мишей зважували раз на тиждень.
Збір крові та вимірювання ліпідів у сироватці крові
Зразки крові мишей відбирали на початку та в кінці експериментального періоду (о 9:00 ранку, після 12-годинного періоду голодування), використовуючи капілярні трубки, введені в медіальне ретроорбітальне венозне сплетення під легкою ефірною анестезією. На початку експерименту від кожної миші відбирали кількість приблизно 150-200 мкл крові. В кінці експерименту та перед евтаназією мишей збирали більшу кількість крові (400 - 500 мкл). Сироватку відокремлювали центрифугуванням при 3000 об/хв протягом 10 хв і зберігали при -80 ° C до аналізу.
Концентрації загального холестерину та тригліцеридів у сироватці крові визначали, використовуючи комерційний набір ферментативних PAP («біоз» - Біотехнологічні програми, Афіни, GR), а холестерин ЛПВЩ визначали ферментативним фотометричним методом холестерину. LDL-холестерин визначали за математичною моделлю "LDL-холестерин = Загальний холестерин- (HDL-холестерин + тригліцериди/5)".
Всі зразки були проаналізовані в лабораторії експериментальної хірургії та досліджень Афінської медичної школи (Афіни, Греція).
Перекисне окислення ліпідів у сироватці крові - Визначення рівнів NO
Загальну концентрацію пероксиду у зібраній сироватці оцінювали фотометрично (набір PerOx, Immundiagnostic AG, Бенсхайм, Німеччина). Загальний вміст оксиду азоту в сироватці крові (NO) розраховували на основі ферментативного перетворення нітрату в нітрит за допомогою нітратредуктази, використовуючи комерційний набір (Загальний набір параметрів аналізу параметрів оксиду азоту та нітратів/нітритів, R&D SYSTEMS, Міннеаполіс, Міннесота, США).
Гістопатологічне фарбування
Наприкінці 8-тижневого періоду тварин піддавали евтаназії під ефірною анестезією з негайним розсіченням печінки та аорти для подальшого гістопатологічного аналізу. Частина печінки та аорти фіксували у 10% формаліні при кімнатній температурі. Потім тканини вкладали у парафін, розрізали та встановлювали на предметні стекла мікроскопа. Зрізи фарбували гематоксилін-еозином і досліджували наосліп двома незалежними дослідниками за допомогою світлової мікроскопії. Точніше, печінку оцінювали, як це було раніше описано Комітетом з патології безалкогольного стеатогепатиту [8]. Гістологічні ознаки були згруповані у 4 широкі категорії: стеатоз, балонізація, портальне запалення та часточна активність. Кожному параметру присвоювали оцінку від 0 (відсутність) до 3 (важке ураження).
Статистична оцінка
Всі аналізи проводились із використанням статистичного програмного забезпечення SPSS. Результати були виражені як середні значення ± стандартні помилки та проаналізовані на статистичну значимість за допомогою тесту ANOVA One Way. Ураження печінки було продемонстровано як середній бал ± стандартні помилки для стеатозу, балонізації, ворітного запалення та часточної активності. Статистичне значення було встановлене P
Результати
Маса тіла та споживання їжі та води
У цьому дослідженні початкова маса тіла для всіх груп була однаковою. Наприкінці 8-тижневого дослідження миші групи HC показали знижену масу тіла порівняно з тваринами в NC (P = 0,027), HCN (Р = 0,018) та HCS (Р = 0,002) групи (табл. 1). Статистично значуще збільшення споживання їжі в групі HCN відносно NC (P Таблиця 1 Маса тіла та споживання їжі
Ліпідний профіль сироватки
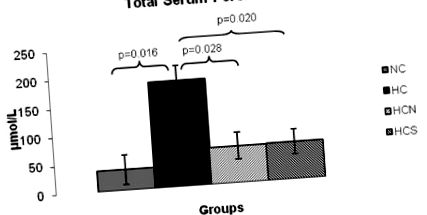
При первинному заборі крові різниці в рівнях ліпідів (крім ЛПНЩ-холестерину, таблиця 1) серед груп не зафіксовано. Харчування дієти з високим вмістом холестерину, що містить 2% холестерину та 0,5% холевої кислоти, протягом 8 тижнів призводило до розвитку гіперліпідемії в експериментальних групах мишей порівняно з контрольною групою. Рівень загального холестерину та ЛПНЩ-холестерину в сироватці крові (табл. 1) суттєво підвищений у трьох групах, які харчувались дієтою з високим рівнем холестерину, порівняно з групою, яка отримувала НСP Фігура 1
Гістопатологія печінки та аорти
Зразки печінки, пофарбовані гематоксилін-еозином, отримані з груп, що харчувалися дієтою з високим вмістом холестерину, виявляли ознаки стеатозу та запалення печінки (рисунок 3). Значне збільшення накопичення крапель жиру спостерігалося в печінці груп HC і HCS порівняно з групою NC [групи HC та HCS проти NC, (P = 0,001) та (P Малюнок 3
Фарбування гематоксиліном та еозином печінкової тканини (400 ×). Контрольні миші (A); миші, які харчуються дієтою з високим вмістом холестерину (В); мишей годували дієтою з високим рівнем холестерину та отримували NAC (C). Стрілка в B. вказує на включення ліпідів гепатоцитів (стеатоз). Зверніть увагу на темні перипортальні запальні інфільтрати у B. та C.
Оцінюючи загальні досліджувані параметри в печінковій тканині мишей, ми робимо висновок, що введення NAC покращило гістологію печінки, тоді як добавки до дієти кунжутною олією мали негативні ефекти.
У тканинах аорти всіх експериментальних мишей не зафіксовано жирових прожилок або бляшок (дані не наведені).
Обговорення
Гіперхолестеринемія є одним з основних факторів ризику розвитку атеросклерозу. Це дослідження було зосереджено на можливому антиліпідемічному ефекті введення NAC та кунжутного масла у мишей з гіперхолестеринемією. Наскільки нам відомо, це перше дослідження, яке досліджувало дію NAC та кунжутного масла на ліпідні профілі мишей, які споживають дієту чау, збагачену холестерином та холевою кислотою.
Харчування холестерино-холевою кислотою часто застосовувалося для підвищення рівня холестерину в плазмі та тканинах експериментальних тварин [9, 10]. Експериментальна дієта, якої дотримувались у цьому дослідженні, призвела до підвищеного рівня загального холестерину та холестерину ЛПНЩ у всіх мишей, які її отримували. Рівень тригліцеридів знижувався у всіх групах, які харчувались дієтою з високим рівнем холестерину та холевої кислоти. Цей висновок відповідає попереднім дослідженням на групах мишей та щурів, яких годували дієтами, що містять холеву кислоту або холат [11, 12]. Крім того, згідно з дослідженням Камісако та співавт. [13] спостерігалося незначне зниження рівня тригліцеридів щурів, які отримували раціон, що містив 1% холевої кислоти, порівняно з їхніми контрольними аналогами. Лі та ін. [11] припустив, що зниження рівня тригліцеридів у їх дослідженні може бути наслідком пригнічення активності 7а-гідроксилази внаслідок присутності холату в експериментальній атерогенній дієті, що не відповідає Beigneux et al. [14], який припустив, що пригнічення активності 7a-гідроксилази призводить до підвищення рівня тригліцеридів.
Гіперхолестеринемія різними способами підсилює утворення вільних радикалів [1] і, як правило, пов’язана з підвищеною продукцією радикалів кисню, таких як супероксидний аніонний радикал [15]. NAC у нашому дослідженні мав сприятливі ефекти щодо ліпідного профілю. Введення цього антиоксиданту в значній мірі запобігло збільшенню рівня ліпідів у сироватці крові (загального рівня холестерину та холестерину ЛПНЩ).
Показано, що NAC знижує рівень холестерину в плазмі та печінці у мишей Balb/cA, які споживають дієту з високим вмістом насичених жирів [2]. Крігер та ін. [16] згадували незначне зниження фракцій ліпідів у плазмі крові за допомогою доповнення NAC у мишей-нокаутів гіперхолестеринемічних рецепторів ЛПНЩ. Отже, інші дослідники вказують на сприятливий вплив NAC на дисліпідемічний профіль щурів, які харчуються дієтою з високим вмістом сахарози, або щурів, яким дають стандартну чау та 30% сахарози у питній воді [17, 18]. Напружувальні механізми, що враховують гіполіпідемічний ефект NAC, можуть бути пов'язані з його антиоксидантними властивостями. NAC у нашому дослідженні призвів до зниження вмісту пероксиду в сироватці крові. Підтримка нормальної структури ліпопротеїнових рецепторів є необхідною для їх функції, покращуючи клітинне засвоєння ліпідів сироватки крові. Реактивні форми кисню, що утворюються під час окисного стресу, реагують з ліпопротеїнами, утворюючи ступінь окиснення, зменшуючи клітинне поглинання ліпідів із крові [17, 19, 20]. Таким чином, антиоксидантна дія NAC може сприяти підвищеному поглинанню клітинних клітин, що призводить до зниження рівня холестерину в сироватці крові.
За словами Ліна та Іня [21], зниження ліпідів дії NAC у мишей, які споживають дієту з високим вмістом жиру, частково пов’язано з придушенням експресії мРНК трьох ферментів, пов’язаних з ліпогену (яблучний фермент, синтаза жирних кислот та 3-гідрокси-3 -метилглутарил-кофермент А-редуктаза).
NO розглядається як важлива вазоактивна речовина, яка захищає цілісність судин. Ху та ін. [22] дійшов висновку, що рівень NO у плазмі крові знижується у кроликів, які харчуються з високим вмістом жиру. Подібно до цього дослідження, ми спостерігали, що наша експериментальна дієта з високим вмістом холестерину та холевої кислоти пригнічувала рівень NO в сироватці крові, тоді як введення NAC підвищувало біодоступність NO та підтримувало його на нормальному рівні. Таким чином, NAC може виконувати важливу захисну роль для нормальної роботи артерій.
Наші результати щодо стеатозу та запалення печінки відповідають результатам попередніх досліджень [23]. Як описано раніше, введення NAC пригнічує печінкову інфільтрацію ліпідів у печінкових тканинах мишей, які харчуються дієтами з високим вмістом жиру [21]. Гепатопротекторна дія NAC може бути пов'язана з його антиоксидантною дією, як уже згадувалося вище.
Подібно до висновків Sener та співавт. [9], дієта з використанням холестерино-холевої кислоти, яка використовувалась у нашому дослідженні, не призвела до жирової смуги або утворення нальоту в тканинах аорти мишей. Цього висновку було частково передбачено, оскільки наша тестова дієта складалася зі звичайної дієти чау (3,5% жиру), збагаченої холестерином та холевою кислотою без додаткового жиру. Навпаки, дієти, що використовуються для ініціювання атеросклерозу у мишей дикого типу, такі як дієта Пайгена [24, 25], мають кінцевий жировий склад більше 15% (у вагових відсотках).
Добавки кунжутного масла на рівні 10% у досліджуваній дієті не змогли відновити порушений ліпідний профіль, спричинений дієтою з високим вмістом холестерину та холевої кислоти, незважаючи на зменшення перекисного окислення сироватки крові. Рівень загального холестерину та холестерину ЛПНЩ демонстрував зниження при введенні кунжутного масла. Однак цей профілактичний ефект не може бути статистично підтверджений, ймовірно, через обмежену кількість наявних спостережень або/та підвищену калорійність модифікованої кунжутною олією дієти. Крім того, ми спостерігали, що одночасне застосування кунжутної олії посилює стеатоз печінки та запалення.
Введення дієтичного знежиреного кунжутного борошна кроликам не захищало від індукованої холестерином гіперхолестеринемії, але знижувало сприйнятливість до окислювального стресу (нижче перекисне окислення ліпідів у сироватці та печінці), можливо, завдяки антиоксидантній активності сезамінолу [26]. Баскаран та ін. [27] повідомили про значне зниження рівня холестерину в плазмі крові, холестерину ЛПНЩ та тригліцеридів у мишей LDLR -/-, коли їх атерогенна дієта була перероблена з тим самим рівнем кунжутної олії. У нашому дослідженні кунжутне масло було додано до дослідної дієти без заміщення жиру. Додаткові калорії дієти з кунжутною олією можуть призвести до відсутності гіполіпідемічної реакції, як було зазначено вище.
У попередньому дослідженні було показано збільшення гіперліпідемічного статусу кроликів, які харчувались гіперхолестеринемічною дієтою, збагаченою оливковою олією [28], тоді як Acin et al. [29] дійшов висновку, що дієтичний холестерин пригнічує здатність оливкової олії затримувати розвиток атеросклеротичних уражень у мишей, негативно впливаючи на показники ліпідів у плазмі крові. Тому ми можемо припустити, що додавання холестерину, як у випадку з оливковою олією, частково пригнічує передбачувану гіполіпідемічну дію кунжутної олії.
Таким чином, незважаючи на те, що кунжутне масло мало антиоксидантні властивості, воно не виявляло значної гіполіпідемічної активності у мишей, які споживали дієту чау, збагачену холестерином та холевою кислотою. Адміністрація NAC змогла поліпшити ліпідемічний статус у сироватці крові, підтримати фізіологію печінки та зменшити кількість пероксидів у сироватці крові, ймовірно, покращивши ефективність системи антиоксидантного захисту експериментальних тварин. Більше того, NAC може здійснювати профілактичну антиатерогенну активність за допомогою підвищеного рівня NO в сироватці крові.
Висновки
Спільне введення NAC, але не кунжутної олії, відновило порушений ліпідний профіль та пошкодження печінки у дослідженій гіперхолестеринемічній мишачій моделі, хоча обидва агенти посилювали антиоксидантну здатність сироватки крові. Таким чином, NAC може бути корисною альтернативою зниженню рівня холестерину у людей під час клінічної практики.
- Вплив Enterococcus faecalis FK-23 на проти ожиріння у мишей із ожирінням, спричинених дієтою
- Вплив солі на гіпертонію та окислювальний стрес у американської моделі ожиріння, спричиненого дієтою, на щурах
- Порівняльна оцінка впливу нано- та мікрочастинок міді у курячому Oriental Journal of
- Філаріальна інфекція або введення антигену покращують толерантність до глюкози у мишей із ожирінням, індукованих дієтою
- Вплив антагоніста NPY5R MK-0557 на відновлення ваги після зниження ваги, спричиненої дуже низькою калорійністю