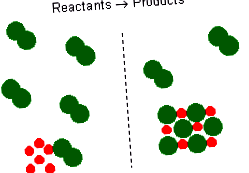
Надлишок та обмеження реагентів
- Стехіометрична суміш
- Надлишок реагенту
- Обмежувальний реагент
Навички для розвитку
- За допомогою стехіометричного розрахунку визначте надлишок та обмежувальні реагенти в хімічній реакції та поясніть, чому.
- Розрахувати теоретичний вихід продуктів, що утворюються в реакціях, що включають обмежувальні реагенти.
Рівняння хімічної реакції дають ідеальне стехіометричне співвідношення між реагентами та продуктами. Однак реагенти для реакції в експерименті не обов'язково є стехіометричною сумішшю. У хімічній реакції називаються реактиви, які не витрачаються після закінчення реакції надлишок реагентів. Реагент, який повністю витрачений або прореагував, називається обмежувальний реагент, оскільки його кількість обмежує кількість утвореної продукції.
Розглянемо реакцію твердого газу натрію та хлору. Реакцію можна представити рівнянням:
Він являє собою реакцію металу та двохатомного газового хлору. Це рівняння збалансованої реакції вказує на те, що два атоми \ (\ ce \) реагували б з двома атомами \ (\ ce \) або однією молекулою \ (\ ce \). Таким чином, якщо у вас 6 атомів \ (\ ce \), знадобиться 3 \ (\ ce \) молекули. Якщо є надмірна кількість молекул \ (\ ce \), вони залишаться без реакції. Ми також можемо стверджувати, що 6 моль натрію потребуватимуть 3 моль газу ((ce)). Якщо є більше 3 молей \ (\ ce \) газу, частина залишиться як надлишок реагенту, а натрій є обмежуючим реагентом. Це обмежує кількість продукту, який може утворитися.
Хімічні реакції зі стехіометричними кількостями реагентів відбуваються ні обмежувальні або надлишкові реагенти.
Обчисліть кількість молей \ (\ ce \), що утворюються при згорянні етану \ (\ ce \) в процесі, коли витрачається 35,0 моль \ (\ ce \).
ПІДКАЗКА
Реакція є
ОБГОВОРЕННЯ
Збалансоване рівняння реакції є основною вимогою для визначення граничного реагенту, навіть якщо відомі кількості реагентів.
Два молі \ (\ ce \) і п'ять молей \ (\ ce \) поміщають у реакційний посудину, а потім \ (\ ce \) підпалюють відповідно до реакції
Визначте граничний реагент у цьому експерименті.
ПІДКАЗКА
Перш ніж ідентифікувати обмежуючий реагент, реакція повинна бути збалансованою. Збалансована реакція є
Таким чином, для двох молей \ (\ ce \) потрібен лише ОДИН моль \ (\ ce \). Чотири родимки кисню залишаться непрореагованими. Отже, кисень є надлишком реагенту, а \ (\ ce \) - обмежуючим реагентом.
ОБГОВОРЕННЯ
Дайте відповіді на ці питання:
Скільки утворюється родимок \ (\ ce \)?
Яка вага утвореного \ (\ ce \)?
Навички, що розробляють проблеми
- При кімнатній температурі (25 ° C), яким є стан натрію: твердий, газовий або рідинний?
Підказка: металевий натрій
- Рівні ваги \ (\ ce
\) і \ (\ ce \) поміщають у повітряну кулю, а потім запалюють. Припускаючи, що реакція завершується, який газ є надлишком реагенту?
Підказка: оксид заліза
Обговорення -
Стехіометрична суміш має масове співвідношення 54: 160 (майже 1: 3) для \ (\ ce \).
Співавтори та атрибуції
Чунг (Пітер) К'є (заслужений професор, хімія @ Університет Ватерлоо)
- Надмірна вага, пов’язана з ще вісьма типами раку. Обмеження збільшення ваги може допомогти зменшити ризик розвитку
- Загальна теорія розділення - хімія LibreTexts
- Енергія в спринті на 100 м - Хімія LibreTexts
- Політ в Бразилії, де зайвий багаж не коштує додатково
- Харчова хімія - Чи має печений хліб таку ж кількість калорій, як і його інгредієнти Хімія