Мікробіом кишечника
На сьогоднішній день мікробіом кишечника є найбільш вивченою мікробною спільнотою здорової людини завдяки його відомій чи підозрілій ролі в широкому діапазоні гомеостатичних фізіологічних функцій та запальних захворювань кишечника та великій біомасі, що робить можливим надійне взяття проб.
Пов’язані терміни:
- Фірма
- Дисбіоз
- Серозит
- Обмін речовин
- Метаболіт
- Мікробіом
- Ожиріння
- Бактерія
Завантажити у форматі PDF
Про цю сторінку
Мікробіом кишечника
Гейл А.М. Креші PhD, RDN, CNSC, Kristin Izzo MS, RDN, CNSC, при синдромі короткого кишечника для дорослих, 2019
Вступ
Мікробіом кишечника, як визначив молекулярний біолог Джошуа Ледерберг, - це сукупність мікроорганізмів, бактерій, вірусів, найпростіших та грибів, а також їх колективний генетичний матеріал, присутній у шлунково-кишковому тракті (ШКТ). Мікробіота кишечника складається з усіх бактерій, коменсальних та патогенних, що мешкають у ШКТ. Протягом останнього десятиліття мікробіота кишечника була досліджена щодо можливих взаємодій кишків мікроб-господар, включаючи вплив на метаболізм, імунні та нейроендокринні реакції. Мікробіота кишечника відіграє важливу роль у поглинанні поживних речовин та мінералів, синтезі ферментів, вітамінів та амінокислот, а також у виробництві коротколанцюгових жирних кислот. Побічні продукти ферментації ацетат, пропіонат і бутират важливі для здоров'я кишечника і забезпечують енергією клітини епітелію, підвищують цілісність епітеліального бар'єру, забезпечують імуномодуляцію та захист від патогенних мікроорганізмів. Поточні дослідження досліджують функцію резидентних бактеріальних генів та потенційну відповідну роль у здоров’ї та метаболізмі людини. Крім того, триває дослідження того, чи можуть непатогенні штами бактерій стимулювати відновлення імунної відповіді на патогенні хвороби (Cresci and Bawden, 2015).
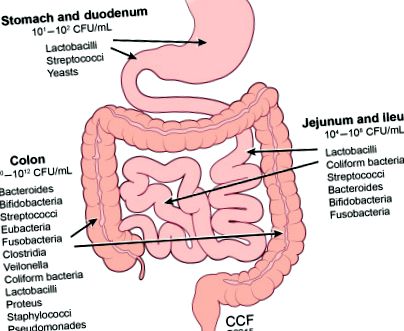
Мікробіота кишечника людини поділяється на багато груп, які називаються філами. Мікробіота кишечника складається в основному з чотирьох основних типів, які включають Firmicutes, Bacteriodetes, Actinobacteria і Proteobacteria (Belizario and Napolitano, 2015). Поки бактерії колонізують людський організм, включаючи порожнину рота, плаценту, піхву, шкіру та шлунково-кишковий тракт, більшість бактерій мешкає всередині ШКТ, а більшість переважно анаеробних бактерій розміщуються в товстій кишці (рис. 4.1). Щоб отримати перспективу величини присутності бактерій та потенційного впливу на господаря, людський організм експресує 20 000 генів еукаріотів, тоді як мікробіом кишечника експресує 3,3 мільйона генів прокаріотів (NIH, 2012).
Рисунок 4.1. Переважання мікробіоти кишечника.
На розвиток та зміни мікробіому кишечника впливають різні фактори, включаючи метод виношування та годування немовлят, вплив стресу, навколишнє середовище, дієта, ліки, стадія життєвого циклу та супутні захворювання (рис. 4.2). Дисбіоз описується як зміна мікробної спільноти, що призводить до зменшення різноманітності та кількості коменсальних бактерій. Дослідження свідчать про взаємозв'язок між дисбактеріозом кишечника та хронічними захворюваннями, такими як запальні захворювання кишечника, метаболічний синдром, серцево-судинні захворювання, ожиріння та рак (Carding et al., 2015).
Малюнок 4.2. Фактори, як відомо, впливають на мікробіом кишечника.
Хронічна хвороба нирок та шлунково-кишкові розлади
Сьюзі К. Лью, Джай Радхакрішнан, Хронічна хвороба нирок (друге видання), 2020
Мікробіом кишечника
Мікробіом кишечника відіграє важливу роль як у підтримці здоров’я, так і в патогенезі захворювання. У пацієнтів з ХХН існує дисбактеріоз кишкового мікробіому, що є наслідком зміни складу та функції мікробіома кишечника та порушення функції бар’єрного кишечника. Дисбіоз мікробіомів кишечника утворює надмірну кількість уремічних токсинів. Більшість із них отримані в результаті незбалансованого бродіння сполук азоту щодо неперетравних вуглеводів, таких як p-крезилсульфат та індоксилсульфат, зокрема. Порушений кишковий бар’єр дозволяє переносити ці токсини в системний кровообіг. Ці уремічні токсини причетні до прогресування ХХН, розвитку серцево-судинних захворювань та ризику смерті у хворих на ХХН. 134,135 Докази свідчать про те, що мікробіом кишечника змінений у пацієнтів з ХХН. 136 Кілька факторів, що сприяють дисбіозу мікробіомів кишечника при ХХН, включають зменшення споживання харчових волокон, запор, порушення засвоєння білка, вживання антибіотиків та терапію залізом. 134
Вплив на метаболізм господаря
Висновки
Мікробіом кишечника широко досліджувався і було доведено, що він бере участь у різних механізмах захворювання. Нові технології в геномному та метабономічному полях, а також системні моделі, такі як миші, що не містять мікробів, вдосконалились за останнє десятиліття та розширили наші знання та розуміння щодо складної взаємодії мікробіоти кишечника з метаболізмом господаря. Однак здатність перекладати результати досліджень на гризунах та застосовувати їх до функцій людини залишається проблематичною, оскільки в обох організмах виявляються різні види мікробів та метаболітів, що мають подібні метаболічні функції. Аналітичні методи кидають виклик великій різноманітності метаболітів. Рівні метаболітів, що впливають на дисбактеріоз мікробіоти кишечника, такі як SCFA та BA, відіграють ключову роль у метаболізмі господаря. Очікується, що нещодавно розроблені методи дадуть нове розуміння функції мікробіоти кишечника шляхом моніторингу метаболітів, що впливають на функцію кишечника. Очевидно, що взаємодоповнюваність різних -омічних аналізів є активом максимізації діапазону виявлення метаболітів для розуміння осі мікробіоти господаря-кишечника та участі у патофізіології шлунково-кишкового тракту (табл. 28.1).
Таблиця 28.1. Короткий зміст метаболізму SCFA та BAs, пов’язаних з віссю кишечника-господаря
| SCFA | • |
PH шлунково-кишкового тракту
Вплив на АТФ, ТГ, холестерин та синтез БА
Активуйте шляхи через GPCR (GPR41, GPR43 та GPR109a)
Активація шляхів PPAR, ROS та TNFα
Синтез модульованих DG та TG
Емульгування та всмоктування харчового жиру
PH шлунково-кишкового тракту
Регулюють власний синтез за допомогою CYP7A1 за допомогою FXR, LXR
Захист від інсулінорезистентності за допомогою TGR5
Варіації середнього та вищого рівнів BA
Вплив дієтичних факторів на мікробіоти кишечника
Джемма Сіфра,. Хосе Мануель Фернандес-Реал, в “Молекулярне харчування та діабет”, 2016
5 мікрофлора кишечника та діабет 1 типу
Запропоновано мікробіому кишечника відігравати певну роль у патогенезі аутоімунних розладів, таких як діабет 1 типу (T1D). Недавні дослідження виявили важливу роль мікробіоти кишечника в регуляції системного метаболізму глюкози та модуляції імунологічних реакцій на мишачій моделі аутоімунного діабету. Відсутність мікробіоти кишечника у мишей без діабету (NOD) не вплинуло на загальну частоту захворювання, але призвело до збільшення інсуліту та рівня аутоантитіл до інсуліну та прозапальних цитокінів та погіршення метаболізму глюкози у мишей, які не прогресували до діабету. 64 Крім того, ці автори спостерігали різницю в профілі метаболоміки сироватки між беззародковими та звичайними мишами NOD, що нагадувало різницю між новонародженими немовлятами, які пізніше прогресували до T1D, та непрогресорами. 64 Таким чином, метаболічні зміни у немовлят, які пізніше переходять до T1D, можуть модулюватися мікробіотою кишечника.
Проспективне дослідження на людях з 35 новітньо діагностованими дітьми з T1D та 35 здоровими дітьми виявило зменшення кількості корисних анаеробних бактерій та супутнє збільшення кількості Enterobacteriaceae, крім колонізації E. coli, у пацієнтів з T1D порівняно з контрольною групою. 65 Порушення екологічного балансу кишкової флори може бути чинником, що викликає етіологію T1D. На підставі всіх цих результатів не можна виключити роль мікробіоти кишечника як регулятора діабетичного аутоімунітету.
Мікробіом кишечника
Сара Ашман, Харі Крішнамурті, у Вплив способу життя на здоров’я чоловіків, 2019
Анотація
Мікробіом кишечника обговорює роль мікробіоти кишечника у здоров’ї та захворюваннях людини як у широкому контексті імуномодуляції, так і у специфічному впливі запальних процесів. Виділено технологічні досягнення, включаючи різноманітні наукові методи оцінки складу мікробіому кишечника та сильних і слабких сторін кожного методу. Симбіотичні стосунки кишкового мікробіома та людського господаря є ключовими для розуміння того, як кожен із них впливає і залежить від іншого для взаємного виживання, від народження до дорослого віку та через механізми різноманітного впливу мікробів, впливу навколишнього середовища та режимів харчування. Також приділяється увага механізмам, що спричиняють хронічні захворювання, та втручанням, включаючи дієтичні та додаткові пробіотики, пребіотики та фенольні сполуки, а також додаткові додаткові поживні речовини, які заслуговують на вирішення проблеми дисбактеріозу кишечника.
Пребіотики та пробіотики в зміні мікробіоти
30.2.2.5 Імуномодуляція
Клінічні умови, пов’язані з переростанням бактерій
Ayesha Shah MBBS, FRACP, Gerald Holtmann MD, PHD, MBA, FRACP, FRCP, при шлунково-кишкових захворюваннях та асоційованих з ними інфекціях, 2019
Характеристика мікробіому кишечника
Мікробіом кишечника може характеризуватися складом бактерій, що колонізують слизову, щільністю колонізації бактерій та продуктами обміну, що виробляються бактеріями. Широко поширена думка, що методи культивування та кількісне визначення колонієутворюючих одиниць (КУО) або метаболічна характеристика продуктів метаболізму культивованих бактерій є найбільш доцільними для характеристики мікробіома. Таким чином, для оцінки кишкових мікробів використовували звичайні методи, засновані на культурі. Однак методи, засновані на культурі, виявились недостатніми для визначення справжнього мікробіологічного різноманіття кишкової мікробіоти, оскільки велика частка мікробіоти залишається необробленою. 40 Дослідження на людях, що використовують різноманітні незалежні від культури молекулярні аналізи, демонструють незрозумілу до цього часу складність мікробіоти людської кишки із сотнями філотипів, з яких 80% залишаються некультурними. 41 Наразі більшість досліджень зосереджувались на мікробіоти калу, частково тому, що зразки калу порівняно легко отримати; однак фекальний матеріал переважно складається з тих мікробів, які мешкають у просвіті кишечника, що не точно відображає склад МАМ. 42–45
Вищезазначені обмеження прямих тестів на основі культури спричинили розвиток непрямих тестів у клінічних умовах для виявлення пацієнтів зі зміненою (посиленою) бактеріальною колонізацією кишечника. Найбільш широко доступними непрямими тестами для діагностики SIBO є дихальні тести 37, засновані на бродінні вуглеводів бактеріями, для отримання кислот, води та газів. Субстрат вводять перорально, а рівень водню (Н2), метану (СН4) або вуглекислого газу (СО2) вимірюють на видиху. Субстратами можуть бути глюкоза лактулоза, ксилоза або жовчні кислоти. Залежно від протоколу виявлення, субстрати також можуть бути марковані радіоактивними або стабільними ізотопами, а альвеолярний видих, що видихається, вимірюється відповідними детекторами (наприклад, твердотільними електрохімічними детекторами [H2 і CH4], сцинтиляційними пристроями [14 C] або інфрачервоною спектроскопією [13 С]). Крім того, метаболічні продукти, такі як H2, CH4 та CO2, можуть бути виміряні за допомогою газової хроматографії або твердотільних датчиків. Речовини, що використовуються для тесту на водень та метан, включають глюкозу 46,47 або лактулозу. 48 Ці дихальні тести зараз широко використовуються в клінічних умовах для діагностики переростання бактерій.
Поліфеноли та здоров’я кишечника
Крістіна Б. Мартінес,. Майкл К. Макінтош, Харчування та функціональна їжа для здорового старіння, 2017
Анотація
Зміна мікробіому кишечника з пребіотиками може пом’якшити дисбіоз та покращити здоров’я кишечника та системи. Рослини багаті на три основні класи поліфенолів з пребіотичними властивостями: (1) фенольні кислоти, (2) флавоноїди та (3) інші феноли. Все це багате фруктами, овочами, спеціями та травами і має як антиоксидантні, так і протизапальні властивості. Оскільки дієтичні поліфеноли погано всмоктуються в тонкому кишечнику, вони залишаються в товстій кишці і метаболізуються в ароматичні метаболіти, які всмоктуються в портальну кров і направляються в печінку або виводяться з калом. Печінкові метаболіти поліфенолу потрапляють у (1) кров для поглинання тканинами-мішенями, (2) сечовий міхур для виведення з сечею або (3) пул жовчних кислот для реміксування з кишковим травленням. У товстій кишці поліфеноли змінюють популяції мікробів кишечника та продукують мікробні метаболіти та кишкові метаболіти, що походять від господаря, та пептидні гормони, які впливають на цілісність кишечника та системний метаболізм.
Слізовий мікробіом
Джонатан Джейкобс, Джонатан Браун, Імунологія слизової оболонки (четверте видання), 2015
Дієтичні впливи
Проведено два дослідження, в яких добровольці піддавались стандартизованій дієті з поздовжнім моніторингом мікробіоти. Один порівняв дієту з високим вмістом жиру/з низьким вмістом клітковини та дієтою з низьким вмістом жиру/з високим вмістом клітковини, тоді як інший вивчав дієту з дефіцитом холіну (Wu et al., 2011; Spencer et al., 2011). Обидва дослідження дійшли висновку, що модифікація дієти призвела до зміни складу кишкової мікробіоти. В одному дослідженні цей зсув спостерігався протягом одного дня (Wu et al., 2011). Сподіваємося, що подальше розуміння впливу дієти на мікробіоти призведе до майбутніх терапевтичних стратегій, які використовують дієтичні маніпуляції або пребіотики для просування мікробних спільнот зі сприятливими властивостями.
Кишкова мікробіота; Його значення в ожирінні
Araceli Muñoz-GarachIsabel M. Cornejo-Pareja Francisco J. Tinahones, в Encyclopedia of Endocrine Diseases (Second Edition), 2019
Анотація
Багато досліджень пов’язували мікробіом кишечника з розвитком метаболічних захворювань, таких як діабет 2 типу та ожиріння. Ожиріння саме по собі пов'язане зі зміною складу мікробіоти кишечника, з тенденцією до надмірного розростання мікроорганізмів, які ефективніше отримують енергію з раціону. Однак збільшення жирової маси відбувається не тільки за рахунок більш ефективного збору енергії, але й мікробіота бере участь у змінах гормонального середовища, експресії генів, що регулюють ліпогенез, інсулінорезистентності, змінах проникності кишечника, ендотоксемії, взаємодії з жовчними кислотами, зміни частки коричневої жирової тканини та наслідки, пов’язані із вживанням наркотиків.
В даний час використання профі і пребіотиків та інших нових методів, таких як трансплантація мікробіоти кишечника або антибіотикотерапія, вважається корисним інструментом для модуляції розвитку ожиріння та інсулінорезистентності за допомогою дієти.
- Фруктоза - огляд тем ScienceDirect
- Цитрулінемія - огляд тем ScienceDirect
- Вага плода - огляд тем ScienceDirect
- Ферментована їжа - огляд тем ScienceDirect
- Холодна кропив'янка - огляд тем ScienceDirect