Мелатонін, гормон темряви: від підвищення сну до лікування Еболи
Аліна Мастерс
1 відділ ендокринології, Медичний факультет, SUNY Downstate Medical Center, 11203 Бруклін, Нью-Йорк, США
Seithikurippu R Pandi-Perumal
2 Центр здорової зміни поведінки, Відділ охорони здоров'я та поведінки, Відділ охорони здоров'я, Медичний центр університету Нью-Йорка, Лангон, Медична школа Нью-Йоркського університету, 227 East 30th St, 10016 Нью-Йорк, Нью-Йорк, США
Азізі Сейшас
2 Центр здорової зміни поведінки, Відділ охорони здоров'я та поведінки, Відділ охорони здоров'я, Медичний центр університету Нью-Йорка, Лангон, Медична школа Нью-Йоркського університету, 227 East 30th St, 10016 Нью-Йорк, Нью-Йорк, США
Жан-Луї Жирарден
2 Центр здорової зміни поведінки, Відділ охорони здоров'я та поведінки, Відділ охорони здоров'я, Медичний центр університету Нью-Йорка, Лангон, Медична школа Нью-Йоркського університету, 227 East 30th St, 10016 Нью-Йорк, Нью-Йорк, США
Самі І. Макфарлейн
1 відділ ендокринології, Медичний факультет, SUNY Downstate Medical Center, 11203 Бруклін, Нью-Йорк, США
Анотація
Мелатонін - гормон, що виділяється загадковою епіфізом у відповідь на темряву, звідси і назва гормону темряви. Це викликало великий інтерес як терапевтичний спосіб лікування різних захворювань, особливо порушень сну. Ця плейотропна молекула має протизапальну, антиоксидантну та антикоагулопатичну властивості на додаток до ендотеліального захисного ефекту. У цій статті ми обговорюємо секрецію мелатоніну та механізми дії, а також терапевтичне обґрунтування. Ми також підкреслюємо потенційну корисність мелатоніну в смертельній сучасній епідемії Ебола.
Вступ
У формі соснової шишки, загадкова шишкоподібна залоза, яка глибоко сидить у мозку, запалила уяву вчених і філософів, а також духов різних культур протягом поколінь, і її охрестили "третім оком" і "оселею душі" Рене Декарта і був задуманий як "заспокійливий орган" [1,2]. Цікаво, що дослідники припустили, що епіфіз та його гормональний продукт мелатонін, можливо, пов’язані з довголіттям [3,4], а дисфункція епіфіза та можливий збій є тим, що ініціює процес старіння [5]. Перші докази того, що епіфіз виділяє біологічно активну сполуку, відому зараз як мелатонін, продемонстрували здатність екстрактів епіфізової тканини з бичачих джерел змінювати пігментацію меланіну у жаб, викликаючи агрегацію меланіну, що породжує назву мелатонін [6, 7]. Ці висновки призвели до спроб використання мелатоніну як лікування вітіліго, що виявилось в основному неефективним. Однак це дослідження призвело до випадкового виявлення ефектів мелатоніну, що сприяють сну. [8,9].
Синтез, зберігання та вивільнення мелатоніну
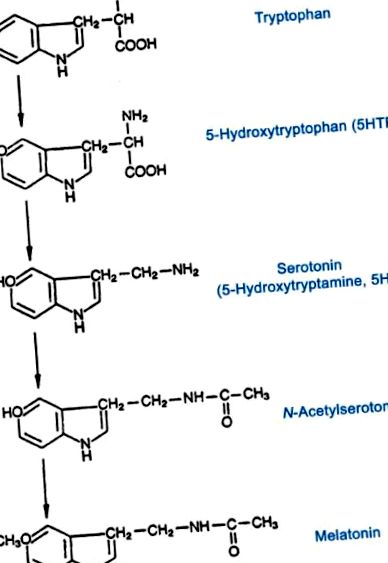
Мелатонін - єдиний відомий гормон, синтезований епіфізом, і виділяється у відповідь на темряву, звідси і назва, “гормон темряви” [10]. Мелатонін забезпечує циркадний та сезонний сигнал для організмів у хребетних. Мелатонін виробляється із серотоніну (виготовленого з триптофану) через каскад ферментативних реакцій (рис. 1). Останні два етапи на шляху включають перетворення серотоніну в N-ацетилсеротонін (NAS), каталізований ферментом арилалкіламін N ацетилтрансферазою (AANAT), з подальшим перетворенням N-ацетилсеротоніну в мелатонін, каталізований ферментом гідроксил-індол-O-метилтрансфераза (HIOMT) [8].
Біосинтез серотоніну та мелатоніну.
Епіфіз отримує надходження з постгангліонарних волокон, що призводить до вивільнення норадреналіну та збільшення продукції циклічного АМФ, таким чином, активуючи згаданий вище фермент AANAT, який є критично важливим для виробництва мелатоніну. Нейрогормона мелатонін не зберігається в епіфізі, а вивільняється в кров і може проникати в усі тканини організму [11]. Важливо відзначити, що «темрява» стимулює епіфіз виділяти мелатонін, тоді як вплив світла гальмує цей механізм [12].
Цікаво, що епіфіз, будучи ембріологічно частиною мозку, знаходиться поза гематоенцефалічним бар’єром і втрачає свої зв’язки з центральною нервовою системою, маючи головним джерелом симпатичну іннервацію [7]. Це, можливо, пояснює здатність епіфіза мати велике поглинання триптофану, що призводить до високого вироблення та секреції мелатоніну у відповідь на темряву. Цей процес також забезпечує відносний захист від передчасної ферментативної деградації, що призводить до 10-20-кратного збільшення рівня мелатоніну в плазмі крові, який легко дифундує через клітинні мембрани та перетинає гематоенцефалічний бар'єр (ВГВ) [7,13].
Механізми дії мелатоніну та терапевтичне обґрунтування
Зі збільшенням поширеності розладів сну, пов’язаних з епідемією ожиріння, спостерігається значний відновлення інтересу до мелатоніну, його механізму дії та терапевтичних ефектів. Порушення сну, незалежно від етіології, часто стикаються з лікарями та іншими медичними працівниками. За даними Центру контролю за хворобами (CDC), близько 70 мільйонів американців страждають хронічними проблемами сну [14], які, як правило, пов'язані з ожирінням, діабетом, гіпертонією та підвищеним серцево-судинним ризиком. Хоча дедалі частіші явища серед загальної популяції в поєднанні з ожирінням, розлади сну є непропорційно важкими та пов’язаними з підвищеним серцево-судинним ризиком серед меншинського населення [15,16]. Порушення сну також часто асоціюються з іншими супутніми захворюваннями, включаючи деменції, хронічний біль, психічні захворювання та шлунково-кишкові розлади [17]. На жаль, незалежно від високої поширеності та серйозних наслідків для здоров’я, порушення сну часто залишаються недіагностованими та в основному недолікованими [18]. Тому надзвичайно важливо правильно діагностувати та лікувати певні типи порушень сну з циркадним ритмом, такі як синдром прогресуючої фази сну (ASPS), розлад сну в змінній роботі та джетлаг [19,20].
Незважаючи на те, що мелатонін впливає на різні клітини людського організму [21], його дії, що сприяють сну, здебільшого зумовлені його зворотним зв'язком з супрахіазматичним ядром (SCN; головний годинник), зокрема на мелатонінові рецептори (MT1 та MT2) [22]. ]. Працюючи над SCN, мелатонін допомагає синхронізувати циркадний ритм, впливаючи як на фазу, так і на амплітуду ритму [23,24]. Запропоновано пригнічувати випалювання нейронів через рецептори МТ1, тоді як рецептори МТ2 відповідають за фазовий зсув [23]. Таким чином, терапія мелатоніном та спорідненими сполуками часто досліджувалась і є предметом інтересу для наукових досліджень.
Мелатонін іноді призначають пацієнтам із порушеннями сну, і він продемонстрував свою ефективність у лікуванні деяких порушень сну, таких як відставання струменя [19,20] та безсоння у людей похилого віку [25]. У дослідженні мета-аналізу, проведеному Бжезінським та ін. у 2005 р., що включав 15 досліджень пацієнтів із лише безсонням, було показано, що лікування мелатоніном значно зменшує затримку початку сну, підвищує ефективність сну та збільшує тривалість сну [26]. Крім того, в недавньому мета-аналізі, проведеному Ferracioli-Oda та співавт. (2013), було виявлено, що мелатонін значно зменшує затримку початку сну та збільшує загальний час сну порівняно з плацебо [27]. Були також клінічні випробування із залученням людей похилого віку безсоння та пацієнтів із хворобою Альцгеймера, які страждали на порушення сну та показали поліпшення стану із застосуванням екзогенного мелатоніну [8].
Адміністрація та профіль безпеки мелатоніну
Що стосується фактичного введення мелатоніну, було показано, що час введення мелатоніну, а не стільки фактична доза, є вирішальним для досягнення найкращих результатів; це вторинно до нормальної фізіологічної функції добового ритму [11]. Наприклад, було встановлено, що коли мелатонін вводили перед сном як «снодійне», він не був ефективним, якщо не використовували високі дози [11,28]; однак, коли невеликі дози мелатоніну вводили пацієнтам приблизно за 2-4 години до сну, було показано, що це ефективно для зменшення затримки сну [29].
Профіль побічних ефектів терапії мелатоніном є досить обнадійливим і в значній мірі перевершує інші засоби, що викликають сон. Наприклад, терапія мелатоніном не викликає симптомів відміни або залежності, на відміну від бензодіазепінів (BZD) та z-препаратів, таких як золпідем [23]. Деякі з потенційних шкідливих наслідків екзогенної терапії мелатоніном включають імуномодулюючі ефекти, що створює ризик погіршення певного ревматологічного стану, такого як ревматоїдний артрит [30]. Це також може призвести до аменореї при застосуванні у великих дозах, що, ймовірно, зумовлене пригніченням гонадотропін-рилізинг-гормону (GnRH) [31]. Однак цей ефект легко відновлюється із припиненням прийому ліків.
Роль рецептур, пов’язаних з мелатоніном
Починаючи з 2005 р. Було введено кілька сполук, пов’язаних з мелатоніном, включаючи Ramelteon, який є агоністом рецепторів МТ1 та МТ2 з більш тривалим періодом напіввиведення порівняно з мелатоніном [23]. Цей препарат був затверджений у США FDA у 2005 році як лікування безсоння [32]. Показано, що він має набагато більшу спорідненість до рецепторів МТ1 та МТ2 у порівнянні з самим мелатоніном [33]. Рандомізоване контрольоване дослідження, проведене Erman та співавт. встановили, що Рамелтеон ефективно зменшує латентний період до стійкого сну в різних дозуваннях [34]. Як і терапія мелатоніном, не було показано, що Рамелтеон асоціюється з ефектом похмілля або симптомами відміни [35].
Ще одним цікавим агентом, який нещодавно був затверджений FDA, є агомелатин. Окрім своєї дії як агоніста на рецептори МТ1 та МТ2, цей препарат має додаткову перевагу, оскільки є антагоністом на 5-НТ2с рецепторі серотоніну [36]. Окрім потужних антидепресивних ефектів, цей препарат сприяє сну - переваги, якої не вистачає більшості антидепресивних засобів. Насправді багато наявних в даний час антидепресантів можуть насправді погіршити сон, а не приносити йому користь [23,37].
Одне інтригуюче питання, яке виникало протягом багатьох років, полягає в тому, як сліпота впливає на циркадний ритм, оскільки надходження з сітківки ока порушено. Хоча дослідження, проведене Czeisler та ін. у 1995 р. показав, що деякі сліпі особи без свідомого сприйняття світла все ще могли пригнічувати секрецію мелатоніну під впливом світла [38], порушення циклу сну і неспання у сліпих людей залишається ціллю для дослідження. На щастя, за результатами двох опублікованих випробувань, новий засіб Tasimelteon був затверджений у 2014 році для лікування стану, відомого як "розлад сну, що не триває 24 години" у сліпих пацієнтів [39]. Цей препарат, ще один агоніст рецепторів МТ1 та МТ2, виявився кращим у порівнянні з плацебо у полегшенні захоплення циркадного ритму, а також у збільшенні нічного сну у досліджуваних "не 24-годинних" сліпих пацієнтів [40].
Мелатонін як можливий терапевтичний варіант для вірусу Ебола
Показано, що мелатонін, універсальна і плюрипотентна молекула, має кілька благотворних ефектів, що перевищують його відому властивість сприяти сну (Рисунок 2).
- Мелатонін - старий гормон з новими хитрощами - пізнання нейронів
- Гормональний дисбаланс у жінок - ознаки, симптоми та лікування GoodtoKnow
- Варіанти лікування легкого апное уві сні - апное сну
- Фонд мелатоніну та сну
- Ефективність, дозування та побічні ефекти препарату для допоміжного сну з мелатоніном