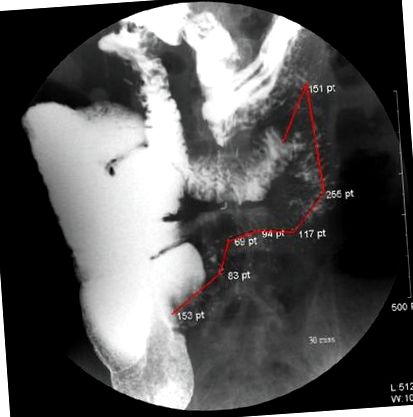
Короткий кишечник (тонкий кишечник = 40 см), відсутність ілеоцекального клапана та хворий на інерцію товстої кишки добре працює з пероральним прийомом самостійно без парентерального харчування
1 відділ харчування, лікарня Тайнань Сін-Лау, № 57, секція 1, дорога Дунмен, місто Тайнань 70142, Тайвань
2 відділення хірургії, лікарня Тайнань Сін-Лау, № 57, секція 1, Донгмен-роуд, місто Тайнань 70142, Тайвань
3 Відділ медсестер, лікарня Тайнань Сін-Лау, № 57, секція 1, дорога Дунмен, місто Тайнань 70142, Тайвань
4 Департамент наук про життя, Коледж біологічних наук та біотехнологій, Національний університет Ченг Кунг, № 1, Університетська дорога, місто Тайнань 701, Тайвань
Анотація
Ми представляємо 50-річного чоловіка, який страждав на ішемічну хворобу кишечника, перенісши масивну резекцію тонкої кишки та ілеоцекального клапана. Йому довелося впоратися із залишком товстої кишки 40 см та дистальною кишкою 70 см. У післяопераційному періоді парентеральне харчування (ПН) застосовувалось негайно для підтримки харчування та корекції електролітного дисбалансу. Ми дали йому домашню ПН як регулярну рекомендацію щодо стану короткої кишки після виписки з лікарні. Цей пацієнт терпів регулярний пероральний прийом через 2 місяці і не розвивав значного синдрому короткої кишки. Було кілька епізодів інфекції венозного доступу, які турбували цього пацієнта та приймали його на лікування під час домашньої ПН. Тому ми змінили домашній ПН на циклічне звуження. Пацієнт міг підтримувати своє харчування та зволоження лише оральним прийомом після звуження додому ПН через 15 місяців. Він вижив не один рік без підтримки ПН і все ще підтримував 80% ідеальної маси тіла із середнім вмістом альбуміну 3,5 ± 0,2 мг/дл. Хоча пацієнт госпіталізувався кожні два місяці для поповнення поживних речовин, проте це значно покращило якість життя.
1. Вступ
Резекція великої частини тонкої кишки може спричинити сильне порушення всмоктування, гіпотрофію та порушення електролітного балансу [1, 2]. Результати резекції залежать від кількості кишечника, що залишився, та конкретного резектованого відділу та збереження довжини товстої кишки або наявності ілеоцекального клапана [1]. Після негайної післяопераційної допомоги зазвичай використовували підтримку пацієнта за допомогою парентерального харчування (PN) та антисекреторних засобів [3] та сприяння адаптації кишечника шляхом перорального харчування [4]. Мінімальна абсорбційна площа тонкої кишки для підтримки життя варіюється від людини до людини.
2. Презентація справи
50-річний бездомний чоловік знепритомнів на станції і був переправлений перехожим у лікарню, зріст 153 см і звичайна маса тіла 54 кг (близько трьох місяців тому до прийому), і скаржився на спазми в животі, перервані з поганим апетитом протягом декількох днів. Вага тіла пацієнта під час прийому становив 40 кг. Він страждав на ішемічну хворобу кишечника, перенісши масивну резекцію тонкої кишки та ілеоцекального клапана. Йому довелося впоратися з проксимальною кишкою 40 см (рис. 1) і дистальною кишкою, що залишилася 70 см. Після операції маса його тіла становила 34 кг (день лікарні 3). За 4 місяці він схуд з 54 кг до 34 кг і розвинув важке недоїдання.
У післяопераційному періоді ПН негайно застосовували для підтримки харчування та корекції електролітного дисбалансу. Через 10 днів розпочали ентеральне харчування, а для лікування діареї застосовували протидіарейні препарати (лоперамід 2 мг два рази на день). Дієтичним прогресом стала чітка рідка дієта (продовжувати годувати 30 мл/год протягом 2 днів), розведена елементарна дієта (продовжувати годувати 700 ккал/день протягом 3 днів) та елементарна дієта з нормальною концентрацією (продовжувати годувати 1200 ккал/день протягом 20 днів) до дієта на основі полімерних сумішей (продовжуйте годувати 1200 ккал/день протягом 5 днів). Пацієнт переносив оральну м’яку дієту та добавки через 40 днів. Ми виписали йому домашню ПН як звичайну рекомендацію та лоперамід після виписки з лікарні.
Цей пацієнт дотримувався дієти з низьким вмістом оксалатів та мінімізував внутрішньопросвітній жир. Ці поживні речовини безпосередньо стимулюють адаптацію кишечника. Через 2 місяці він переносив регулярний пероральний прийом без протидіарейних препаратів. У нього не розвинувся значний синдром короткої кишки, такий як посилення дефекації, мальабсорбція, анемія, стеаторея та втрата м'язів. Через півроку вага тіла пацієнта підтримувалася на рівні 42 кг, а сироватковий альбумін становив 3,6 мг/дл. Було кілька епізодів інфекції венозного доступу, які турбували цього пацієнта та приймали його на лікування під час домашньої ПН. Ми оцінили стан харчування та забезпечили ефективне засвоєння білка, незважаючи на відносно короткий тонкий кишечник. Тому ми змінили домашній ПН на циклічне звуження та контролювали масу тіла, альбумін, електроліт та рівень гемоглобіну. На наш подив, пацієнт міг підтримувати своє харчування та зволоження лише оральним прийомом після звуження додому ПН через 15 місяців. Він вижив не один рік без парентеральної підтримки і все ще підтримував 80% ідеальної маси тіла (близько 41
42 кг) із середнім вмістом альбуміну 3,5 ± 0,2 мг/дл. Незважаючи на те, що пацієнт відвик від регулярної підтримки ПН, у нього почали розвиватися анемія та симптоми дефіциту вітаміну В1. Пацієнта госпіталізували протягом трьох днів кожні два місяці через периферичне парентеральне харчування для доповнення вітамінів та мікроелементів.
3. Обговорення
Залишкова довжина кишечника у цих пацієнтів, відлучених від TPN, становила від 27 до 75 см (середнє значення 57 см) у педіатричних пацієнтів [5] та від 57 до 150 см (середнє значення 96 см) у дорослих пацієнтів [6]. Жоден із дорослих пацієнтів із залишковою довжиною тонкої кишки менше 40 см не зміг досягти повної адаптації кишечника. Нашого пацієнта з тонкою кишкою 40 см і без ілеоцекального клапана успішно відлучили від ПН. Далі ми перевіряємо час кишкового транзиту та низку шлунково-кишкового тракту (шлунково-кишкового тракту) після орального прийому пацієнтом 16 місяців. Час транзиту товстої кишки розраховували за допомогою заповнених радіонуклідами капсул та рентгенографії черевної порожнини. Через 64 години радіонукліди майже не виділялися. Серія з низьким шлунково-кишковим трактом показала, що товста кишка стала товстою і довгою. Довжина від 70 см становила близько 120 см, а живіт повний товстої кишки (рис. 2). Пацієнт приймає перорально на волі, але він завжди скаржиться на розтягування, оскільки харчування сприяє адаптації тонкої кишки та товстої кишки та збільшує абсорбційну площу. Особливо велика, товста і інерційна товста кишка для подовження часу перебування продуктів, корисного для всмоктування.
Основним механізмом люмінальних білків є те, що вони перетравлюються на ди- та трипептиди для всмоктування. Транспортер олігопептидів PepT1 відповідає за транспорт ди- та трипептидів у кишечнику ссавців [7]. PepT1 поширений уздовж кордону кисті тонкої кишки у людей, але експресується на низькому рівні в поглинаючих клітинах товстої кишки. Циглер та співавт. [8] показали, що підвищення регуляції PepT1 в товстій кишці хворих на СРС свідчить про те, що товста кишка людини може збільшити просвіт ди- та трипептидів у кишечнику під час кишкової недостатності. Цей пацієнт підтримував середній рівень альбуміну 3,5 ± 0,2 мг/дл. Це означало, що підвищена експресія товстої кишки PepT1 є прикладом адаптації кишечника у цього пацієнта з короткою кишкою.
4. Висновки
Пацієнт із інерцією короткої кишки та товстої кишки, який протягом кількох місяців отримував ентеральну та парентеральну підтримку, збільшував абсорбційну область та функції тонкої кишки та товстої кишки. Цей пацієнт із короткою кишкою добре працює лише при пероральному прийомі без парентерального харчування. Хоча пацієнта госпіталізували кожні два місяці для доповнення поживних речовин, проте це значно покращило якість життя.
Конфлікт інтересів
Автори заявляють про відсутність конфлікту інтересів щодо публікації цієї статті.
Список літератури
- А. Сундарам, П. Куткія та К. М. Аповіан, “Харчове лікування синдрому короткої кишки у дорослих”, Журнал клінічної гастроентерології, вип. 34, ні. 3, с. 207–220, 2002. Переглянути на: Сайт видавця | Google Scholar
- C. L. Donohoe і J. V. Reynolds, "Синдром короткої кишки", Хірург, вип. 8, № 5, с. 270–279, 2010. Переглянути на: Сайт видавця | Google Scholar
- L. M. Nørholk, J. J. Holst та P. B. Jeppesen, "Лікування пацієнтів із синдромом короткої кишки з допомогою тедуглутиду", Думка експерта з питань фармакотерапії, вип. 13, № 2, с. 235–243, 2012. Переглянути на: Сайт видавця | Google Scholar
- А. Р. Віл, А. Г. Едвардс, М. Бейлі та П. А. Лір, “Кишкова адаптація після масивної резекції кишечника”, Медичний журнал післядипломної освіти, вип. 81, ні. 953, с. 178–184, 2005. Переглянути на: Сайт видавця | Google Scholar
- М. Васа, Ю. Такагі, К. Сандо, Т. Харада та А. Окада, “Кишкова адаптація у дитячих хворих із синдромом короткої кишки” Європейський журнал дитячої хірургії, вип. 9, № 4, с. 207–209, 1999. Перегляд за адресою: Google Scholar
- М. Васа, Ю. Такагі, К. Сандо, Т. Харада та А. Окада, “Віддалений результат синдрому короткої кишки у дорослих та педіатричних пацієнтів” Журнал парентерального та ентерального харчування, вип. 23, ні. 5, с. S110 – S112, 1999. Перегляд за адресою: Google Scholar
- Y.-J. Fei, Y. Kanai, S. Nussberger et al., "Експресійне клонування протонно-зв'язаного транспортера олігопептидів ссавців", Природа, вип. 368, ні. 6471, с. 563–566, 1994. Переглянути на: Сайт видавця | Google Scholar
- T. R. Ziegler, C. Fernández-Estívariz, L. H. Gu et al., “Розподіл H +/пептидного транспортера PepT1 в кишечнику людини: регульована експресія в слизовій оболонці товстої кишки пацієнтів із синдромом короткої кишки” Американський журнал клінічного харчування, вип. 75, ні. 5, с. 922–930, 2002 р. Перегляд за адресою: Google Scholar
- Аппалачська долина® Собачий рецепт дрібних порід з олениною; Боби Garbanzo Taste of the Wild®
- Примітка про невеликі кількості продуктів тваринного походження в продуктах харчування PETA
- Заміна аортального або мітрального клапана на Biocor та Biocor Supra - Повний текст
- Bfabulous Diets Sector 18, Noida - Досвід пацієнтів для Bfabulous Diets Noida
- Крім жирного і тонкого, короткий і високий балет для людей