Гігантська ліва аневризма коронарної артерії, що представляє собою множинні імплантовані дефібриляторні удари кардіовертера
Опубліковано: 12 квітня 2020 р. (Див. Історію)
DOI: 10.7759/cureus.7653
Цитуйте цю статтю як: Malyshev Y, Syed A, Castillo R, et al. (12 квітня 2020 р.) Гігантська ліва аневризма коронарної артерії, що представляється як багаторазові імплантовані дефібриляторні удари кардіовертера. Cureus 12 (4): e7653. doi: 10.7759/cureus.7653
Анотація
Гігантські аневризми лівої магістральної коронарної артерії є одними з найрідкісніших знахідок у кардіології, з якими стикаються менш ніж у 0,02% пацієнтів. Презентація зазвичай така ж, як ішемічна хвороба артерій, оскільки більшість коронарних аневризм у західному світі пов’язані з атеросклерозом. Тут ми повідомляємо про перший випадок гігантської аневризми лівої магістральної коронарної артерії, що проявляється як шлуночкова тахікардія з численними поштовхами дефібрилятора у 57-річного чоловіка з серцевою недостатністю. Ми також розглядаємо етіологію, патологію та лікування коронарних аневризм.
Вступ
Аневризми коронарних артерій (КАА) - дуже рідкісні клінічні утворення; серед них гігантські аневризми лівої магістральної коронарної артерії (LMCAA) надзвичайно рідкісні, що зустрічаються менш ніж у 0,02% пацієнтів [1]. Етіологія CAA варіюється залежно від віку, супутніх захворювань та навіть географічного району. Етіологія, як правило, визначає представлення та управління. У цьому документі ми повідомляємо про унікальний випадок гігантського LMCAA у 57-річного чоловіка із серцевою недостатністю зі зниженою фракцією викиду (HFrEF), який подав до нашого відділення невідкладної допомоги біль у грудях після того, як його імплантований кардіовертерний дефібрилятор (МКБ) спрацював 12 разів. Термінова діагностична катетеризація показала гігантський LMCAA без ознак ішемічної хвороби серця (ІХС). Пацієнту розпочато подвійну антитромбоцитарну терапію. Він залишався безсимптомним більше року. Ми також розглядаємо поточну літературу про різні методи діагностики та різні підходи управління CAA.
Презентація справи
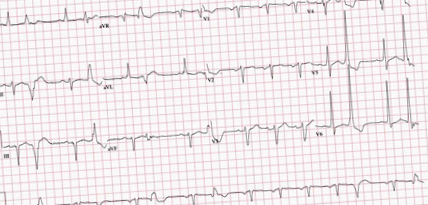
Напередодні у 57-річного чоловіка з артеріальною гіпертензією, діабетом, ожирінням та HFrEF спостерігався біль у грудях, серцебиття та синкопе. Його МКБ спрацював 12 разів. Його життєві показники були нічим не примітні. Фізичний огляд був значущим для нерегулярного пульсу. ЕКГ показав нормальний синусовий ритм з частими передчасними шлуночковими комплексами та лівою передньою фасцикулярною блокадою (рис. 1).
Рисунок 1: ЕКГ, що показує синусовий ритм із передчасними скороченнями шлуночків та лівою передньою фасцикулярною блокадою
Рентген грудної клітки був чітким. Аналіз крові показав підвищений рівень серцевих ферментів та аномалій електролітів, а скринінг препаратів був позитивним щодо канабіноїдів (табл. 1).
| Тест | Результат |
| Тропонін (нг/мл) | 2.14 |
| CPK (од./Л) | 537 |
| pBNP (пг/мл) | 1860 рік |
| Калій (мекв/л) | 2.8 |
| АНА | Негативні |
| Анти-dsDNA антитіло (МО/мл) | 1 |
| pANCA (AU/мл) | Таблиця 1: Значущі результати лабораторних досліджень |
CPK, креатинфосфокіназа; pBNP, про-мозковий натрійуретичний пептид; ANA, антинуклеарні антитіла; анти-dsDNA, анти-дволанцюжкове антитіло до ДНК; pANCA, перинуклеарні антинейтрофільні цитоплазматичні антитіла
Допит за МКБ показав, що два штурхи були проведені при шлуночкової тахікардії, а 10 поштовхів були невідповідними через електромагнітні перешкоди на відведенні. Ехокардіограма виявила фракцію викиду 10% -15% з дифузним гіпокінезом (Відео 1).
Відео 1: Ехокардіограма, що демонструє сильно знижену систолічну функцію лівого шлуночка, фракцію викиду 10% -15% та дифузний гіпокінез
Термінова катетеризація серця не показала ознак оклюзійної ІХС. Однак був великий мішкоподібний LMCAA, що включає усть лівого переднього низхідного (LAD), лівого циркумфлекса (LCX) та артерії ramus intermedius. Вимірювали розмір аневризми 37,4 мм х 20 мм (рис. 2, відео 2). Аутоімунна обробка була негативною (таблиця 1).
Рисунок 2: Гігантська аневризма лівої головної коронарної аневризми
A: праворуч передній косий черепний вигляд; B: праворуч передній косий каудальний вигляд
Відео 2: Ангіограма, що демонструє гігантську аневризму лівої головної коронарної артерії
Пацієнту розпочато подвійну антитромбоцитарну терапію аспірином та клопідогрелем. КТ-операція оцінила пацієнта, але не рекомендувала втручання. Пацієнту було успішно імплантовано кардіовертерний дефібрилятор під час того самого прийому. Через рік його побачили в ЕД із підозрою на легеневу емболію. КТ грудної ангіограми показала, що LMCAA має діаметр 1,5 см (рисунок 3).
Малюнок 3: КТ грудної клітки, що показує аневризму лівої головної коронарної артерії (біла стрілка)
A: поперечна площина; B: корональна площина
Через два місяці після відвідування ЕД його побачили в клініці без симптомів, а МКБ добре функціонував.
Обговорення
CAA - це сегмент артерії, ширина якого перевищує довжину, а діаметр перевищує діаметр нормального сусіднього сегмента або в 1,5 рази більший за найбільший коронарний посудину (рис. 4) [2,3].
Рисунок 4: Схематичне зображення справжньої коронарної аневризми
CAA класифікуються наступним чином. Склад стінки: справжні аневризми мають усі три шари стінки судини; псевдоаневризми втрачають одну-дві. Форма: поперечний діаметр мішкоподібних CAA більше, ніж поздовжній діаметр. Їх часто бачать дистальніше від стенозу і схильні до тромбозів або розривів. Веретеноподібні аневризми охоплюють всю окружність судини, мають більші поздовжні вимірювання і не мають ніякого відношення до стенозу. Розмір: маленький (діаметр 8 мм) [3].
Захворюваність коливається від 0,3% до 5,3% (в середньому 1,65%). У чоловіків більше CAA, ніж у жінок: 2,2% проти 0,5%. Найбільш частими місцями є праві коронарні (40% -70%), LCX (23,4%) та LAD (32,3%) артерії. Ліва головна коронарна артерія уражається значно менше (0,1% -3,5%) (рис. 5) [4,5]. Поширеність гігантських CAA серед загальної популяції становить лише 0,02% [1].
Рисунок 5: Розподіл та частота аневризм коронарних артерій
ЛМ, ліва головна коронарна артерія; LAD, ліва передня низхідна артерія; LCX, ліва циркумфлексна артерія; RCA, права коронарна артерія
Етіологія CAA варіюється залежно від віку та географічного району. Атеросклероз відповідає за половину ВГА на Заході, за ним слідують вроджені (17%) та інфекційні (10%) аневризми. Хвороба Кавасакі є основною причиною розвитку ГАА в Японії [3]. Запальні розлади та захворювання сполучної тканини, як правило, пов’язані з ектазіями і частіше спостерігаються у молодих пацієнтів [3]. До ятрогенних причин належать травми від індукційного тиску в балоні, втручання при гострому інфаркті міокарда, вживання нестероїдних протизапальних препаратів, стероїдів та колхіцину, що може спричинити неправильне загоєння. Кокаїн викликає важку гіпертензію та звуження судин, тим самим пошкоджуючи ендотелій та сприяючи утворенню CAA [6].
Вважається, що CAA в ІХС викликані турбулентним кровотоком, що пошкоджує стінку [3]. Однак мають бути й інші фактори, оскільки у більшості пацієнтів з ІХС не розвивається ГАА.
Зазвичай пацієнти протікають безсимптомно, і більшість CAA виявляються випадково. Виступ залежить від етіології та/або ускладнень. Ускладнення CAA включають емболізацію, розрив, утворення фістули, тампонаду, гемоперикард, дисекцію, спазм судин та здавлення судин [2,3].
Коронарна ангіографія залишається найкращим методом ідентифікації САА [2]. Він надає інформацію про місцезнаходження, розміри та форму CAA, але він бачить лише просвіт судини. Таким чином, справжній розмір CAA можна недооцінити, або CAA можна пропустити, якщо його тромб закупорює [4]. Внутрішньосудинне ультразвукове дослідження виправляє ці обмеження, надаючи трансмуральні зображення та інформацію про структуру стінки та склад просвіту [4,7]. КТ-коронарографія надає швидку інформацію про місцезнаходження, форму, розмір та склад стінки САА, але не має можливості лікування. КТ-ангіографія корисна для наступних пацієнтів з відомими CAA [4].
Лікування CAA залежить від форми захворювання, етіології, розміру, локалізації, асоційованої інфекції та ступеня атеросклерозу [4]. У дорослих з ІХС слід розпочати медичне зменшення серцево-судинних факторів ризику. Слід починати довготривалі антитромбоцити та потенційно антикоагуляцію, оскільки тромбоз та/або емболія викликають занепокоєння [8]. Черезшкірне втручання із встановленням стента може проводитися при аневризмі діаметром до 10 мм [9]. Хірургічне втручання показано пацієнтам, які не є кандидатами на черезшкірне втручання, обструктивну ІХС та великі мішкоподібні аневризми з ризиком розриву [4,10].
Висновки
Перший випадок CAA був опублікований в 1812 році. Його виявили посмертно після раптової смерті. З тих пір наше розуміння патології, етіології та розвитку ХАА покращилось. Сьогодні ми можемо знайти ці потенційно смертельні аневризми під час рутинної ангіограми, а не після забою. Однак управління ними все ще є складним завданням, і воно повинно бути спеціально адаптоване до кожного пацієнта. Потрібні додаткові дослідження для виявлення пацієнтів, які ризикують діагностувати CAA раніше, краще керувати нею та запобігти ускладненням.
- Діагностична модель на основі мікробіома кишечника для прогнозування хвороби коронарних артерій Сільськогосподарський журнал
- Генетичний аналіз клініки Клівленда пов'язує ожиріння з діабетом, ішемічною хворобою серця; Клівленд
- Кава, мате, асаї та квасоля є основним фактором, що сприяє антиоксидантній здатності бразильців; s
- Камені в жовчному міхурі та дієта з низьким вмістом жиру Товариство розсіяного склерозу
- Ембріональні стовбурові клітини пропонують обіцянку лікування розсіяного склерозу - UConn Today