Інгібування корозії вуглецевої сталі в 1 М розчині соляної кислоти водним екстрактом Thevetia peruviana
Анотація
Інгібуючий ефект Thevetia peruviana щодо корозійної поведінки вуглецевої сталі в 1 М HCl вивчали методом втрати ваги, поляризацією, електрохімічним імпеданс-спектроскопією змінного струму та методами електрохімічної модуляції частоти. Встановлено, що ефективність інгібування залежить від концентрації екстракту та температури середовища. Результати показали, що цей екстракт діє як інгібітор змішаного типу. Опір передачі заряду збільшується, але ємність подвійного шару зменшується за рахунок збільшення концентрації екстракту. Було встановлено, що досліджуваний екстракт діє шляхом адсорбції на поверхні вуглецевої сталі і підпорядковується ізотермі адсорбції Темкіна. Вплив температури на швидкість корозії за відсутності та присутності екстракту досліджували, деякі активували та розраховували параметри адсорбції. Результати електрохімічних методів добре узгоджувалися з результатами вимірювання втрати ваги.
Вступ
Ця робота є продовженням попередніх робіт і спробою оцінити інгібуючу дію природи Thevetia peruviana про корозію С-сталі в 1 М HCl з використанням хімічних та електрохімічних методів.
Матеріали і методи
Склад зразків матеріалу
Рішення
1-М агресивний розчин (соляна кислота) готували в лабораторії, розводячи відповідний об'єм аналітичного сорту 37% HCl дводистильованою водою. Кислоту стандартизували стандартним розчином карбонату натрію.
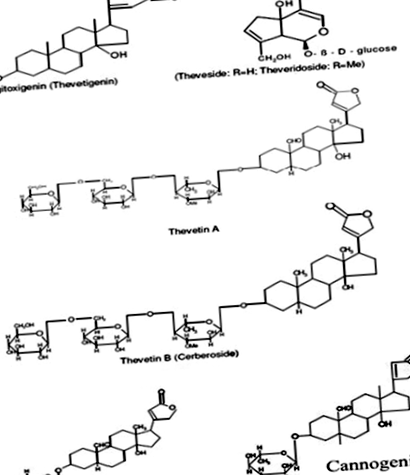
Хімічна структура сполук, присутніх у рослині (Thevetia peruviana)
Thevetia peruviana належить до сімейства Apocynaceae і його зазвичай називають жовтим олеандром або пілаканхером. Всі частини рослини містять різноманітні серцеві глікозиди [21]. На рисунку 1 показані деякі важливі хімічні складові, присутні в рослині.
Структури серцевих глікозидів та їх вільних агліконів, знайдені в Thevetia peruviana Рослина
Приготування рослинного екстракту
Висушену рослину подрібнювали на циліндричну дробарку на невеликі шматочки 5–10 мм і екстрагували дводистильованою водою. Екстракт отримували змішуванням 100 г висушеної рослини в 250 мл води при 80 ° С протягом 30 хв. Екстракт залишали на ніч, потім фільтрували через фільтрувальний папір, заливали до 1000 мл дводистильованою водою і, нарешті, зберігали в холодильнику в скляних колбах, звужених гвинтовою пластиковою кришкою [22].
Тести на схуднення
Для вимірювання втрати ваги використовували зразки розміром (2 × 2 × 0,2) см. Зразки послідовно стирали різними серіями наждачного паперу змінних сортів, починаючи з найгрубішого (80) і переходячи поступово до найтоншого (1200) сорту, знежиреного ацетоном і сушеного на повітрі. Експеримент зі зниженням ваги був завершений у 100 мл 1 М розчину HCl без і з різними концентраціями досліджуваного екстракту. Швидкості корозії (CR) визначали, використовуючи таке рівняння [23]:
Тут Δм - втрата маси, s - відкрита площа поверхні зразка (см 2), і т - час занурення. Ефективність гальмування,% IE та ступінь покриття поверхні, θ, були визначені з використанням наступного рівняння [24]:
Тут CRcorr і CRinh - це швидкість корозії вуглецевої сталі без і з витяжкою відповідно.
Газометричний метод
Для дослідів виділення водню використовували листи вуглецевої сталі розміром (2 × 2 × 0,2 см). Перед кожним експериментом поверхні зразків вуглецевої сталі обробляли, як і раніше. Зразок вставляли в склянку місткістю 100 мл виділеного водню, що виділявся, і збирали через бічне плече, з'єднане гнучкими поліетиленовими трубками, з газовою бюретою, що стояла в мензурці, наповненій водою. Це дозволило виміряти варіацію об'єму водню, що виділився під час розчинення металу, як функцію часу. Експерименти проводились за відсутності та присутності різних концентрацій екстракту. Швидкість корозії (r) приймали за нахил прямих ліній, отриманий із співвідношення об'єму виділеного водню та часу. Ефективність інгібування (% IE) розраховували наступним чином:
Ось, р f і р i - швидкість корозії за відсутності та присутності екстракту.
Тести на потенціодинамічну поляризацію
Експерименти з потенціодинамічної поляризації проводили в звичайній триелектродній комірці з використанням платинової марлі як протилежного електрода та насиченого каломелевого електрода (SCE) в якості електрода порівняння. Робочий електрод готували з квадратного листа вуглецевої сталі такого ж хімічного складу, як показано в таблиці 1, вкладеного в епоксидну смолу політетрафторетилену, щоб площа відкритої поверхні становила 1 см 2. Перед кожним випробуванням поверхню електрода попередньо обробляли таким же чином, як і в експериментах з втратою ваги. Перед вимірюванням електрод занурювали в розчин із потенціалом розімкнутого контуру на 25 хв до досягнення стійкого стану. Клітина була обладнана таким чином, щоб температура під час кожного експерименту підтримувалась постійною та вимірюваною. Потенціал робочого електрода був збільшений ± 250 мВ в районі потенціалу корозії, а анодна та катодна криві були отримані від -0,7 до 0,7 В при швидкості сканування 1 мВс -1. Всі експерименти проводили у свіжоприготованих розчинах при 25 ° C, і результати повторювали тричі для перевірки відтворюваності. Ефективність інгібування для кожної концентрації екстракту та покриття поверхні, θ, були розраховані за наступним рівнянням [25]:
Ось, i корр і i inh - щільності корозійного струму, розраховані на основі екстраполяції схилів Тафеля без та з інгібіторами.
Тести електрохімічної імпедансної спектроскопії (EIS)
Вимірювання імпедансу (EIS) проводили, використовуючи ту саму компоновку комірок, що і раніше, з каркасною системою Gamry на базі ESA400. Вимірювання EIS проводили з використанням сигналів змінного струму з амплітудою від 5 мВ до піку до потенціалу розімкнутої ланцюга в діапазоні частот від 100 кГц до 0,5 Гц. Всі дані імпедансу були встановлені у відповідну еквівалентну схему за допомогою програмного забезпечення Gamry Echem Analyst.
Випробування електрохімічної частотної модуляції (EFM)
Експерименти EFM проводили, застосовуючи сигнал потенційного збурення з амплітудою 10 мВ з двома синусоїдами 2 і 5 Гц. Вибір частот 2 і 5 Гц базувався на трьох аргументах [26]. Більші піки використовувались для розрахунку щільності корозійного струму (i корр), схили Тафель (β c і β а) та фактори причинності CF2 і CF3 [27].
Електрохімічні вимірювання проводили за допомогою Gamry Instrument Potentiostat/Galvanostat/ZRA (PCI4-G750). Сюди входять програми Gamry, програмне забезпечення DC105 для корозії постійного струму, програмне забезпечення EIS300 для електрохімічної імпедансної спектроскопії (EIS) та EFM140 для вимірювань електрохімічної частотної модуляції (EFM) разом із комп’ютером для збору даних. Програмне забезпечення Echem для аналітиків версії 6.03 було використано для побудови графіків, графіків та підгонки даних.
Аналіз поверхні
Поверхня вуглецевої сталі спочатку стиралася за допомогою різних наждачних паперів (марки 80–1200) і змивалась дводистильованою водою перед зануренням зразків на 1 год у 1 М HCl за відсутності та наявності оптимальної концентрації досліджуваної рослини екстракт. Після цього часу занурення зразки промивали дводистильованою водою, повністю висушували і монтували в спектрометр без подальшої обробки. Корозійні поверхні вуглецевої сталі досліджували за допомогою рентгенівського дифрактометра Philips Energy Dispersive (pw-1390) з Cu-трубкою (CuKa1, l = 1,54051 Å) та скануючим електронним мікроскопом (SEM, JEOL, JSM-T20, Японія).
Результати і обговорення
Тести на схуднення
Втрати маси зразків вуглецевої сталі реєстрували через різні часові інтервали занурення (30, 60, 90, 120, 150 та 180 хв) при різних температурах (25, 30, 35, 40 та 45 ° C); тут показана лише крива втрати ваги при 25 ° C (рис. 2). Значення% IE при різних температурах наведені в таблиці 2. Результати показали, що присутність Thevetia peruviana екстракт пригнічував швидкість корозії зразків вуглецевої сталі в 1 М розчині HCl. Зазначалося, що% IE збільшується при збільшенні концентрації рослинного екстракту, як показано в таблиці 2. Це можна пояснити адсорбцією молекул екстракту на поверхні сталі. Ця адсорбція зменшує розчинення сталі, блокуючи місця корозії, а отже, зменшуючи втрату ваги, одночасно збільшуючи ефективність із збільшенням концентрації екстракту.
Крива втрати ваги під час розчинення вуглецевої сталі за відсутності та наявності різних концентрацій Thevetia peruviana екстракт при 25 ° C
Ізотерми адсорбції
Як правило, при кислотній корозії інгібітори діють шляхом адсорбції на поверхні металу. Адсорбція інгібітора може визначати структурний заряд подвійного шару, тим самим зменшуючи швидкість часткових електрохімічних реакцій. Більше того, адсорбція, яка особливо відбувається на активних ділянках поверхні металу, може перешкоджати реакційній здатності металу в процесі розчинення. З іншого боку, якщо за адсорбцією супроводжується реакція гідратації або відновлення або полімеризації самого інгібітора, можуть утворитися товсті шари, які поводяться як справжній фізичний бар'єр. У будь-якому випадку, знання адсорбційної поведінки інгібіторів є важливим для визначення механізму його дії. Ізотерма адсорбції дає зв'язок між охопленням межі розділу з адсорбованими видами та концентрацією виду в розчині. Інтерпретація ефективності адсорбентного типу інгібітора може бути покращена внесенням даних в одну з відомих ізотерм адсорбції, яка представлена на рис. 3. Встановлено, що ізотерма адсорбції Темкіна [28] добре підходить для експериментальних даних.
Графіки адсорбції Темкіна для вуглецевої сталі в 1 М HCl при різних температурах у присутності різних концентрацій Thevetia peruviana екстракт
Вплив температури
Вплив температури на швидкість розчинення м'якої сталі в 1 М HCl, що містить різні концентрації досліджуваного інгібітора, перевіряли шляхом вимірювання втрати ваги в діапазоні температур від 25 до 45 ° C. Вплив підвищення температури на швидкість корозії (k corr) та% IE були отримані в результаті вимірювання втрати ваги. Результати показали, що зі збільшенням температури спостерігається зниження k корр, тоді як% IE збільшується. Енергію активації (\ (E _ ^ \)) корозійного процесу розраховували за допомогою рівняння Арреніуса (рівняння 6) [34]:
Ділянки Арреніуса для швидкості корозії (k кор.) вуглецевої сталі в 1 М HCl за відсутності та наявності різних концентрацій Thevetia peruviana екстракт
- Характеристики пригнічення та адсорбції зеленої корозії екстракту листя Luffa cylindrica на м’якій основі
- ЕФЕКТИ ІНГІБІТОРІЇ КОРРОЗІЇ ДЕЯКИХ БАЗОВ SCHIFF S НА МІЛОЇ СТАЛІ В КИСЛОТИХ СЕРЕДОВИЩАХ
- Неорганічно-органічна наносистема на основі вуглецевих точок для двофотонної візуалізації та біосенсора варіації рН
- Цикл вуглецю та клімат Землі
- Керівництво з отруєння чадним газом Причини, симптоми та варіанти лікування