Харчова калориметрія
Аудиторія
Старшокласники (10-12)
Період часу
Налаштування: 5 хвилин
Активність: 40 хвилин
Прибирання: 5 хвилин
Стандартні та освітні очікувальні
Стандартний: Енергія та взаємодії
Очікуваний: Q.CF1- Матерія та їх взаємодія: перетворення енергії та маси
Індикатори: ES.Q.CF1.IE. 4, 14 y 10
Після завершення діяльності студенти зможуть:
- Це пояснює різні типи їжі, які здатні виробляти тепло та енергію.
- Проаналізуйте різні типи матеріалів, з яких виготовляють їжу.
- Кількісно визначте кількість хімічної енергії, що зберігається в різних типах їжі (наприклад, білках, вуглеводах, жирах).
- Це пояснює вплив розміру банки та взаємозв'язок кількості води в банку.
Словник та визначення:
- Тепло
- Енергія
- Температура
- Калориметрія/Термодинаміка
- Калорійність
- Білки
- Вуглеводи
- Жири
Наукова довідка
Горіння - це процес, за допомогою якого матеріал (зазвичай те, що зазвичай називають паливом) перетворюється, в результаті чого виділяється тепло. Компоненти їжі (тобто білки, вуглеводи, жири) можна спалювати, щоб визначити кількість енергії, що зберігається всередині. Енергія з їжі набувається організмом після того, як їжа перетравлюється і засвоюється. Для експериментального отримання цього значення необхідний калориметр. Основний принцип калориметра полягає у використанні енергії, що виділяється вибраною їжею під час згоряння, для нагрівання води, яка міститься в жерстяній банці. Фундаментальний принцип полягає в тому, що енергія, що виділяється як тепло, їжею, повністю поглинається водою. Це правда, оскільки ЗАКОН ЗБЕРЕЖЕННЯ МАСИ ТА ЕНЕРГІЇ повинен виконуватися. Математичним співвідношенням, що використовується для обчислення кількості теплоти, поглиненої водою, є
Qwater = mwater Cp (Tf - Ti)
Qwater - тепло, що поглинається водою (у калоріях)
Mwater = маса води в банку (може бути розрахована за щільністю води (1 г/мл)
Ср - теплоємність води (1кал/г С)
Tf - кінцева температура води
Ti - початкова температура води
Скажімо, що ви використовували 50 мл води і що початкова температура становила 23 oC, а кінцева температура 25 oC.
Знаючи, що густина води становить 1 г/мл при 25 oC, отже, ми маємо 50 г води.
ЯЧ = 50 г (1 кал/г oC) (25-23) oC
Пам'ятайте, що на етикетках продуктів ви бачите калорійність (еквівалент ккал, або 1000 кал). Отже, якщо ви вимірюєте вагу того, що ви спалили (перед тим, як спалити), ви можете розрахувати кількість тепла, яке виробляється будь-якою вагою їжі, а потім порівняти з тим, що написано на етикетці.
Наприклад, скажімо, що шматок їжі важив 50 мг.
це означає, що у вас є 2Cal/g. На порцію 100 г ви отримуєте 200 кал.
- Комерційний розмір порожня їжа може.
- Маленька порожня банка з їжею (
10 унцій) (підійде випарена молочна банка).
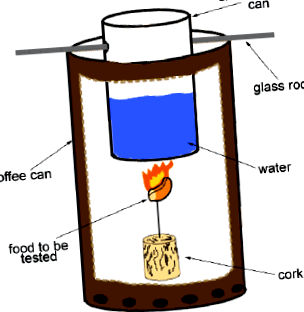
Фігура 1. Розташування калориметра.
Вирішення проблем
-Розрахунки не відповідають тому, що написано на етикетці
Аналіз передбачає, що "все" тепло, що виділяється, "поглинається" водою. Отже, втрати тепла потрібно мінімізувати за рахунок:
- ізоляція вашої зовнішньої банки (див. вище методи)
- використовуйте всередині невелику металеву банку (не використовуйте склянку)
- з використанням дистильованої води (теплова потужність води передбачалася, і тому будь-яка домішка води з крана вплине на вимірювання). Ідеальним буде використання деіонізованої води
Переконайтеся, що їжа була повністю спожита. Це нормально, що в кінці у вас є залишки чорного кольору. Головне, щоб ви візуально не бачили незгорілих деталей. Якщо це трапиться, почніть спочатку з нового твору. Можливо, спробуйте той, який менше.
Якщо ви отримаєте завищену ціну, можливо, термометр торкався металу біля основи банки. Це потенційно може спричинити завищення температури, яку досягає вода.
-Їжа не загоряється
Нормально, що деякі продукти харчування загоряються легше, ніж інші. Однак переконайтеся, що вся їжа, яку ви використовуєте, суха. Вологість може ускладнити горіння. Є деякі продукти, які досить зручні у вживанні. Деякі пропозиції:
- Сирні затяжки
- Чітос
- Кукурудза
- Горіхи
-Їжа загоряється, але вона швидко вимикається після того, як ви поклали банку зверху.
Причина, швидше за все, полягає в тому, що споживається кисень і полум’я його позбавляється. Переконайтеся, що банка не плоска на прилавку, а менша банка не надто велика. Це є причиною того, чому банка може мати отвори на дні.
- Які основні хімічні структури жирів, цукрів та білків?
- Чи відрізняються ці типи молекул за кількістю енергії, яку вони містять?
- Якщо для маленьких ми можемо використовувати склянку або керамічний флакон, як ви думаєте, ви отримаєте подібні результати?
- Якщо ви спалюєте одну і ту ж їжу, але використовуєте різну кількість води, чи очікуєте ви, що кінцевий результат буде однаковим?
Додаткові ресурси:
- http://www.watchknow.org/Video.aspx?VideoID=17223
- http://www.chemistryexplained.com/Ge-Hy/Heat.html
- http://hyperphysics.phy-astr.gsu.edu/hbase/thermo/spht.html
Дослідження студентів
Студенти можуть захотіти пов’язати цей експеримент із реальним світом шляхом подальших експериментів чи досліджень, пов’язаних з харчовими продуктами та їх калорійністю; потреба у висококалорійній їжі для спортсменів та дітей, що розвиваються, порівняно з дорослими; матеріали для транспортних засобів, включаючи матеріали, що використовуються в двигунах, двигунах тощо для відведення тепла; космічні човникові плитки тощо. Студенти можуть захотіти створити продукт своїх результатів досліджень, наприклад, традиційну наукову роботу, огляд відповідних досліджень, презентацію PowerPoint, або знайти відповідні відеоролики або зробити власні відео.
- Броснан, переглянутий Л. Падва, К. Горман, Л. Гілоні, Е. Каненгізер Під редакцією Лінди Падви та Девіда Хенсона, (2006). Калориметрія - Вимірювання теплової енергії. Університет Стоні Брук
Аткінс, П., де Пола, Дж. (1978/2010). Фізична хімія, (перше видання 1978 р.), дев'яте видання 2010 р., Oxford University Press, Oxford UK.
Кондепуді, Д. (2008), Вступ до сучасної термодинаміки, Чічестер, Великобританія: Уайлі, Лебон, Г., Джо, Д., Касас-Васкес, Дж. (2008). Розуміння нерівноважної термодинаміки: основи, застосування, межі, Спрінгер-Верлаг, Берлін.
Сайзер, Ф і Уітні, Е. 1997. Концепції та суперечки щодо харчування. 7-е видання Вадсворт: Каліфорнія.
Електронні посилання:
Калориметрія-еквівалент води калориметрія: vlab.amrita.edu/?sub=2&brch=190&sim…1 Theoryvlab.amrita.edu/?sub=2&brch=190&sim…
Студентський робочий лист з теплової енергії: харчова калориметрія
Назва експерименту: ________________________________ Дата: ________ Ім'я: ____________________
Розробити a керівне запитання або запитання для експерименту:
- Які основні хімічні структури жирів, цукрів та білків?
- Чи відрізняються ці типи молекул за кількістю енергії, яку вони містять?
- Якщо для маленьких ми можемо використовувати склянку або керамічний флакон, як ви думаєте, ви отримаєте подібні результати?
- Якщо ви спалюєте одну і ту ж їжу, але використовуєте різну кількість води, чи очікуєте ви, що кінцевий результат буде однаковим?
- Аналізує наведену нижче етикетку, яка дає просте пояснення того самого, використовуючи інформацію, яку вивчають у лабораторії.
- Громада організовує участь у навчанні з питань харчування та харчування, ставлення та харчовий ризик у Росії
- Харчова служба The Nutrition Group
- Свідоцтво про харчування та харчування - Інтернет; Коледж професійної освіти
- Нарізану кубиками сушену папайю купуйте оптом з їжі, щоб жити
- Калорії в папайї Як використовувати цей низькокалорійний фрукт для схуднення - їжа NDTV