Збільшення вісфатину після схуднення, викликаного гастропластичною хірургією
Відділення внутрішніх хвороб I лікарні Rudolfstiftung, Відень, Австрія
Відділення внутрішніх хвороб I, лікарня Rudolfstiftung, Juchgasse 25, 1030 Відень, Австрія. Електронна пошта: [email protected] Шукати інші статті цього автора
Кафедра клінічної фармакології, Віденський медичний університет, Відень, Австрія.
Центральна лабораторія лікарні Rudolfstiftung, Відень, Австрія
Відділення внутрішніх хвороб I, лікарня Rudolfstiftung, Відень, Австрія
Відділення внутрішніх хвороб I лікарні Rudolfstiftung, Відень, Австрія
Відділення внутрішніх хвороб I лікарні Rudolfstiftung, Відень, Австрія
Відділення внутрішніх хвороб I, лікарня Rudolfstiftung, Juchgasse 25, 1030 Відень, Австрія. Електронна пошта: [email protected] Шукати інші статті цього автора
Кафедра клінічної фармакології, Віденський медичний університет, Відень, Австрія.
Центральна лабораторія лікарні Rudolfstiftung, Відень, Австрія
Відділення внутрішніх хвороб I лікарні Rudolfstiftung, Відень, Австрія
Відділення внутрішніх хвороб I лікарні Rudolfstiftung, Відень, Австрія
Анотація
Завдання: Нещодавно описаний адипокін вісфатин виробляється у вісцеральному жирі і, як пропонується, впливає на резистентність до інсуліну. Щоб дослідити, чи пов’язані концентрації вісфатину із змінами маси тіла, цей адипокін вимірювали у інсулінорезистентних пацієнтів з важким ожирінням до та після гастропластичної операції.
Методи та процедури дослідження: Вісфатин, інтерлейкін-6, високочутливий С-реактивний білок, оцінка моделі гомеостазу на інсулінорезистентність (HOMA-IR) та інші клінічні параметри оцінювали у 36 пацієнтів з важким ожирінням (28 жінок; середній вік 43 роки) із медіаною ІМТ 44,3 кг/м 2 (95% довірчий інтервал, 43,3-48,1 кг/м 2).
Результати: Після операції ІМТ зменшився до медіани 31,9 кг/м 2 (30,1 - 35,1 кг/м 2) (стор
Вступ
Методи та процедури дослідження
Результати
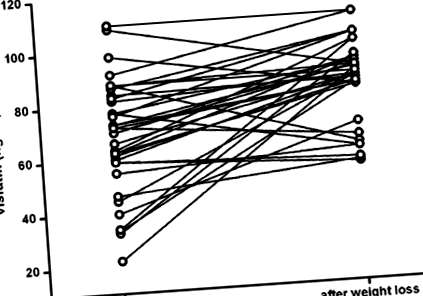
Гастропластична хірургія супроводжувалася масивною втратою ваги, на що вказує зниження ІМТ. Через 12 місяців усі пацієнти досягли мінімальної ваги, яка згодом залишалася стабільною. Рівні інсуліну натще, глюкози та HOMA-IR знижувались у всіх пацієнтів, тоді як зміни концентрацій вісфатину в плазмі були неоднорідними, але зростали у більшості пацієнтів після гастропластики. Зниження вісфатину після схуднення спостерігалося лише у семи пацієнтів (рис. 1). Зниження ваги було пов'язане зі значним зниженням IL-6 та hsCRP. Крім того, систолічний та діастолічний артеріальний тиск, загальний холестерин, ліпопротеїн-холестерин низької щільності та тригліцериди помітно знизилися, тоді як ліпопротеїн-холестерин високої щільності збільшився після втрати ваги (Таблиця 1).
Індивідуальні концентрації вісфатину до та після втрати ваги, спричиненої гастропластичною хірургією (n = 36).
| ІМТ (кг/м 2) | 44,3 (43,3-48,1) | 31,9 (30,1 - 35,1) | Таблиця 2. Коефіцієнти рангової кореляції Спірмена між змінами вісфатину та змінами параметрів результату |
| ΔBMI | -0,28 (0,145) |
| ΔТілесна вага | -0,19 (0,322) |
| ΔSBP | -0,14 (0,500) |
| ΔDBP | -0,16 (0,446) |
| ΔПості інсуліну | -0,35 (0,040) |
| ΔГлюкоза натще | −0,14 (0,407) |
| ΔHOMA ‐ IR | −0,45 (0,007) |
| ΔХолестерин | 0,0002 (0,999) |
| ΔLDL | −0,05 (0,782) |
| ΔHDL | 0,04 (0,838) |
| ΔТригліцериди | 0,08 (0,647) |
| ΔIL ‐ 6 | 0,09 (0,638) |
| ΔhsCRP | 0,10 (0,604) |
- SBP, систолічний артеріальний тиск; DBP, діастолічний артеріальний тиск; HOMA-IR, оцінка моделі гомеостазу на інсулінорезистентність; ЛПНЩ, ліпопротеїди низької щільності; ЛПВЩ, ліпопротеїни високої щільності; IL ‐ 6, інтерлейкін 6; hsCRP, високочутливий С-реактивний білок.
Обговорення
Це поздовжнє дослідження демонструє, що зниження ваги після гастропластичної хірургії пов'язане зі значним збільшенням концентрації циркулюючого нового адипокіну вісфатину у пацієнтів із сильним ожирінням. Параметри, пов’язані з метаболічним синдромом та хронічним субклінічним запаленням, явно зменшувались після втрати ваги у цих пацієнтів. Зниження інсулінорезистентності було обернено пов’язане із підвищенням рівня вісфатину.
Відповідно до раніше опублікованих даних ((1)), IL-6 та hsCRP знизилися після втрати ваги. In vitro було продемонстровано, що IL-6 залежно від часу регулює синтез вісфатину та пригнічує мРНК вісфатину в адипоцитах ((6)). Зменшення субклінічного запалення, що вказується на зниження IL-6 та hsCRP у нашому дослідженні, може бути пов’язане із підвищенням концентрації вісфатину у плазмі крові. Однак дані in vitro можуть не бути безпосередньо порівнянними з результатами in vivo, що могло б пояснити, чому нинішні висновки не показали кореляції між IL-6 та концентрацією вісфатину, що циркулює. З іншого боку, було показано, що фактор, що підвищує колонію перед В-клітинами, виражається на запальних стимулах і підвищується в нейтрофілах пацієнтів із сепсисом ((12)). Ці суперечливі висновки можуть принаймні частково пояснити відсутність кореляції між вісфатином та запальними маркерами в нашій когорті дослідження. Подальші експериментальні та клінічні дослідження будуть необхідні для вивчення впливу запалення на вісфатин та навпаки.
На закінчення, це дослідження демонструє, що велика втрата ваги після гастропластичної хірургії пов'язана зі збільшенням плазмових концентрацій нового адипокіну вісфатину. Збільшення концентрації вісфатину суттєво пов’язане зі зниженням резистентності до інсуліну, спричиненим втратою ваги.
Подяка
Для цього дослідження не було фінансування/сторонньої підтримки.
- Міхір Джайн, найважчий підліток у світі, схуд на 100 кг в результаті хірургічного втручання. Це єдина відповідь
- Камені в нирках, поширені після операції для схуднення - The New York Times
- Втрата ваги Міссі Елліотт схудла хірургічним шляхом
- Як відновити схуднення після шунтування шлунка Bari Life
- Шлунковий куля покривається страховою хірургією Орегона для схуднення