Утворення коротколанцюгових жирних кислот мікробіотою кишечника та їх вплив на метаболізм людини
Дуглас Дж. Моррісон
Центр досліджень навколишнього середовища шотландських університетів, Університет Глазго, Східний Кілбрайд, Шотландія
Том Престон
Центр досліджень навколишнього середовища шотландських університетів, Університет Глазго, Східний Кілбрайд, Шотландія
АНОТАЦІЯ
Утворення SCFA є результатом складної взаємодії між дієтою та мікробіотою кишечника в середовищі просвіту кишечника. Відкриття рецепторів у цілому ряді типів клітин і тканин, для яких коротколанцюгові жирні кислоти SCFA є природними лігандами, призвело до підвищеного інтересу до SCFA як сигнальних молекул між мікробіотою кишечника та господарем. SCFA представляють основний потік вуглецю з раціону через мікробіоти кишечника до господаря, і з'являються докази регулюючої ролі SCFA у місцевому, посередницькому та периферичному метаболізмі. Однак відсутність добре розроблених та контрольованих досліджень на людях перешкоджає нашому розумінню значення SCFA у метаболічному здоров'ї людини. Цей огляд має на меті об’єднати останні результати щодо ролі SCFA в метаболізмі людини, щоб підкреслити багатогранну роль SCFA у різних метаболічних системах.
Вступ
Виробництво SCFA мікробіотою кишечника
SCFA виробляються головним чином шляхом сахаролітичного бродіння вуглеводів, які уникають травлення та всмоктування в тонкому кишечнику, а шляхи виробництва SCFA відносно добре вивчені 4 і нещодавно детально описані. 5 Основними продуктами є форміат, ацетат, пропіонат та бутират. Лактат також є основною органічною кислотою, що отримується в результаті ферментації вибраних, часто швидко ферментованих НДК. 6 Відносно незначні кількості жирних кислот з розгалуженим ланцюгом також виробляються, головним чином, шляхом ферментації амінокислот з розгалуженим ланцюгом, отриманих з білка. 7 Амінокислотне бродіння може також сприяти виникненню SCFA, головним чином за рахунок виробництва ацетату та пропіонату. Порівняно мало відомо про роль формату в кишечнику. Він пов’язаний з метаногенезом і, як видається, підвищений при запальних станах. 8,9 Лактат також може далі метаболізуватися до ацетату, пропіонату та бутирату за допомогою ряду організмів, що перехресно годують. 10-12
Місце виробництва SCFA та біологічний градієнт від просвіту кишки до периферії
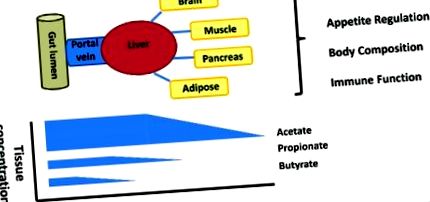
Існує сильний біологічний градієнт для кожного SCFA від просвіту кишечника до периферії, що призводить до різного впливу SCFA на клітини та тканини (рис. 1). Основна робота постраждалих від раптової смерті вперше висвітлила значне зниження рівня бутирату щодо ацетату та пропіонату в епітелії кишечника, а також значне зменшення вмісту пропіонату щодо ацетату в печінці у людей. 29 Це також спостерігалося нещодавно при дослідженнях стабільного ізотопного потоку у людини, де печінкова здатність використовувати SCFA врівноважує вироблення SCFA в кишечнику, що призводить до незначного виведення спланхнічного пропіонату та бутирату. 30,31 Ці спостереження дозволяють припустити, що роль SCFA слід враховувати в кожному типі клітин або тканин у межах цього біологічного градієнта. Взаємодія між використанням епітелію та цілісністю, використанням спланхніки та периферичною доступністю вимагає розмежування, щоб визначити, чи підвищена продукція всіх SCFA або селективне збільшення окремих SCFA у певних тканинах визначає деякі спостережувані метаболічні ефекти.
Просвіт кишечника є основним місцем виробництва, але градієнт концентрації падає з просвіту на периферію із селективним поглинанням бутирату в епітелії, пропіонату в печінці та ацетату на периферії. Значення для фізіології господаря цього біологічного градієнта недостатньо вивчене.
SCFA і цілісність кишечника
SCFA та гомеостаз глюкози
На додаток до прямого сигналу, виведеного SCFA з кишечника, є супутні сигнали, що генеруються в результаті первинної продукції SCFA в просвіті кишки. Гормони кишечника, що виробляються ентероендокринними клітинами в епітелії товстої кишки, також роблять сприятливий вплив на гомеостаз глюкози. Механізми впливу гормонів кишечника на гомеостаз глюкози були детально розглянуті в інших 53,54 місцях і виходять за рамки цього огляду. Однак вироблення SCFA мікробіотою в просвіті кишечника є важливою початковою подією для сигналу, що походить від кишкового гормону. 55,56
Вплив SCFA на ліпідний обмін
SCFA та регулювання апетиту
SCFA та імунна функція
Печінка вміщує цілий ряд типів клітин, які взаємодіють за допомогою малих молекул та вторинного імунного сигналу цитокінів. Вважається, що проникність бар’єру кишечника є ключовим фактором у визначенні прозапального навантаження, що досягає печінки. 36 Відміна накопичення тригліцеридів гепатоцитів та етерифікація жирних кислот, а також зменшення окиснення жирних кислот та реагування на інсулін спостерігається в моделі виснаження клітин Купфера в мишах, що значною мірою опосередковується TNF-α. 88 Останні дані також свідчать про те, що бутират пригнічує активність TNF-α, IL-6 та мієлопероксидази, запобігаючи активації NF-ΒΒ у клітинах Купфера. 89 Існує мало даних щодо ацетату та пропіонату, які могли б бути при вищому потоці через печінку. Хоча потрібні додаткові докази для встановлення ролі SCFA у регуляції запалення печінки, прямо чи опосередковано, ці дослідження демонструють важливість осі кишечника і печінки у запальних та метаболічних системах, і що SCFA може відігравати важливу роль в обох.
Роль SCFA також поширюється на периферичну імунну функцію. Нещодавнє дослідження продемонструвало, що ацетат опосередковує запалення суглобів на моделі миші подагри за рахунок складання запального запалення та продукування IL-1β, яке частково залежить від FFAR2. 90 Подібний захисний ефект нещодавно спостерігався для бутирата на моделі подагри мононуклеарних клітин периферичної крові, хоча для помірного продукування прозапальних цитокінів IL-1β, IL-6, IL-8 та IL- необхідні високі концентрації бутирату 1β. 91 Розгляд біологічного градієнта впливу SCFA на різні типи імунних клітин може мати вирішальне значення для визначення фізіологічно значущих результатів при імунно-опосередкованому та запальному захворюванні.
Висновки та перспективи на майбутнє
SCFA разом з іншими метаболітами, що потрапляють в печінкову портальну систему, швидко транспортуються до печінки. Роль молекулярної передачі сигналів на різних типах клітин печінки погано охарактеризована. SCFA може діяти на резидентні макрофаги та гепатоцити, хоча може існувати функціональна селективність для кожного SCFA. Гормони інкреції можуть також впливати на гепатоцити та периферичні тканини. Загальним впливом цієї подвійної системи передачі сигналів, здається, є підтримка здорової печінки за допомогою регуляції печінкового метаболізму та запалення та контролю потоку жирів жиру, отриманого з жиру. Периферійні ефекти SCFA виглядають специфічними для тканини. SCFA може регулювати інсулін у підшлунковій залозі, потік FFA з адипоцитів, центри апетиту в мозку та забезпечувати паливо для м’язів. Однак ця багатогранна роль вимагає подальших досліджень з добре розробленими та контрольованими дослідженнями на людях.
Скорочення
Розкриття потенційних конфліктів інтересів
Автори не мають заявляти про конфлікт інтересів.
Фінансування
Лабораторія стабільної ізотопної біохімії при SUERC частково підтримується грантами BBSRC (BB/L004259/1, BB/H004815/1, BB/H532091/1, BB/L025418/1) та Стратегічним партнерством уряду Шотландії (RESAS).
- Незамінні жирні кислоти
- Блог про жирні кислоти для активації спалювання жиру
- Критичні відмінності між харчовими добавками та жирними кислотами Омега-3, що відпускаються за рецептом
- Dockside Hotel Apartments London Docklands, Short Stays near Excel
- Катехіни та проціанідини в ягодах видів вакцинії та їх антиоксидантна активність