Тема 14 Харчування при хворобах підшлункової залози
Йоганн Окенга, доктор медичних наук, професор.
Деп. гастроентерології,
Ендокринологія та харчування,
Klinikum Bremen Mitte,
Санкт-Юргенштрассе 1,
28177 Бремен, ФРН
Мета навчання
- Знати про фізіологію та патофізіологію ХП (хронічний панкреатит);
- Знати цілі лікування в ХП щодо харчування;
- Щоб зрозуміти показання до різних харчових втручань при ХП.
Зміст
- Вступ
- Фізіологія підшлункової залози
- Патофізіологія хронічного панкреатиту
- Клінічні особливості ХП
- Харчовий статус у CP 5.1 Склад тіла 5.2 Метаболічна ситуація
- Лікування, пов’язане з харчуванням 6.1 Терапевтичні цілі 6.2 Заміна ферменту підшлункової залози 6.3 Лікування болю 6.4 Рекомендації щодо дієти 6.5 Роль ентерального годування
- Резюме
- Клінічний випадок
- Тест самооцінки
- Список літератури
Ключові повідомлення
- Екзокринна функція підшлункової залози необхідна для адекватного перетравлення проглоченої їжі;
- Основною екзокринною функцією підшлункової залози є виділення бікарбонатних та травних ферментів, таких як ліпаза, протеїназа та амілаза, коли потрапляє їжа потрапляє в дванадцятипалу кишку;
- ХП характеризується прогресуючою втратою клітин ацинарних і протокових каналів з подальшим зниженням екзокринної секреції;
- Основними клінічними наслідками екзокринної недостатності підшлункової залози (відзначається у 25% - 45% хворих на ХП) є порушення травлення жиру та стеаторея;
- Хронічний і особливо постпрандіальний біль є ознакою ХП (60% - 90% пацієнтів) і є основною причиною анорексії;
- Ендокринна недостатність підшлункової залози (цукровий діабет) зазвичай розвивається в кінці хвороби;
- Збільшення енергетичних витрат через хронічне запалення може призвести до подальшого погіршення стану харчування;
- Харчове лікування - це лише частина мультимодального лікування при ХП, наступне за значенням - контроль болю та заміщення ферменту підшлункової залози в ротовій порожнині;
- Під час подальшого спостереження харчова оцінка повинна бути задокументована;
- Харчові цілі полягають, по-перше, у забезпеченні оптимальної енергії, субстратів і вітамінів, а по-друге, уникненні заподіяння болю в підшлунковій залозі;
- Адекватне заміщення ферментів підшлункової залози є головною основою харчової допомоги у хворих на ХП з екзокринною недостатністю підшлункової залози;
- Харчова терапія повинна складатися з високої калорійності (35 ккал/кг/24 години), високого вмісту білка (1,0-1,5 г/кг/24 години) та збагаченої вуглеводами дієти з помірною кількістю жиру (0,7-1,0 г/кг/24 години);
- Модифікація дієтичного споживання жиру (наприклад, тригліцериди із середньою ланцюгом) необхідна лише в тому випадку, якщо ферментна терапія підшлункової залози не дає результатів;
- Додаткове ентеральне харчування (годування ковтками або зондом) показано, якщо пероральне годування не досягає терапевтичних цілей;
- Під час важкого гострого нападу панкреатиту пацієнта слід лікувати як гострий панкреатит (див. Модуль 14.1).
1. Вступ
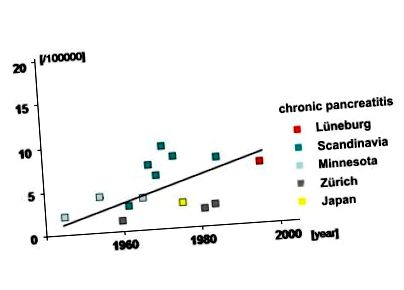
Захворюваність на хронічний панкреатит зросла за останні 60 років (Рис. 1) і зараз в промислово розвинутих країнах захворюваність становить до 10 на 100 000 людських років. Це спостереження може бути зумовлене кращою діагностикою, але також може бути пов’язано із серйозними змінами у способі життя в західних індустріальних країнах. У розвинених країнах майже 70 - 80% хворих на ХП мають тривалий анамнез високого споживання алкоголю (> 80 г/добу). Поряд з алкоголем, куріння, здається, є додатковим фактором ризику, і очевидно, що існує сильна позитивна кореляція між великим споживанням алкоголю та сильним курінням. Виявлено кілька інших етіологічних факторів, включаючи генетичну схильність до ХП, але, незважаючи на велике розслідування, приблизно у 20% пацієнтів неможливо встановити конкретну причину, і ці пацієнти класифікуються як такі, що мають ідіопатичний панкреатит.
У наступному тексті будуть описані лише наслідки та лікування ХП щодо екзокринної підшлункової залози. Для конкретного лікування ендокринної недостатності підшлункової залози, будь ласка, зверніться до розділу про діабет (Тема 21).
2. Фізіологія підшлункової залози
Екзокринна реакція екзокринної підшлункової залози залежить від часу (Рис.2) і пов'язані з кількома факторами (Рис.3). Екзокринна підшлункова залоза складається здебільшого з ацинарних клітин, але додатково з центроацинарних і клітин проток. Тоді як ацинарні клітини синтезують> 10 травних ферментів, клітини протоки відповідають за вироблення бікарбонату, необхідного для нейтралізації шлункової кислоти та підвищення рН в дванадцятипалій кишці для отримання оптимального лужного середовища для ферментів підшлункової залози, а також тонка кишка межує з травними ферментами.
Блукаючий нерв та гормони секретин та холецистокінін (CCK) відповідають за стимуляцію екзокринної підшлункової залози. Ферменти підшлункової залози перетравлюють крохмаль (амілазу), ліпіди (ліпазу) та білок (трипсин та інші протеолітичні ферменти). Найважливішим стимулом для секреції підшлункової залози є наявність поживних речовин у просвіті дванадцятипалої кишки.
На секреторну реакцію підшлункової залози впливає не тільки кількість, а й склад поживних речовин у просвіті дванадцятипалої кишки (Рис.3).
3. Патофізіологія хронічного панкреатиту
Через втрату ацинарних і протокових клітин (Рис.4) секреторна здатність екзокринної підшлункової залози зменшується. Великий фізіологічний резерв підшлункової залози є причиною того, що клінічні ознаки порушення травлення жиру виникають в кінці ХП, як правило, коли 80% секреторної здатності підшлункової залози втрачено.
Порушення травлення жиру (стеаторея;> 10 г жиру в калі протягом 24 годин) є основною проблемою у цих пацієнтів. Стеаторея обумовлена (i) зменшенням секреції бікарбонату підшлункової залози, що призводить до більш швидкої та повної інактивації ліпази в кислій дванадцятипалій кишці; (ii) подальше порушення всмоктування ліпідів за рахунок денатурації жовчної кислоти в кислій дванадцятипалій кишці; (iii) швидка деградація ліпази в просвіті тонкої кишки через її більшу вразливість до протеолізу - тим самим зменшуючи період активності ліпази; (iv) обмежена здатність екстрапанкреатичної ліпази (шлункової); (v) відсутність компенсуючих ферментів, що перетравлюють тригліцериди, в кишковому кордоні кисті. Оскільки жир є таким основним джерелом енергії, порушення травлення жиру створює високий ризик білково-енергетичного недоїдання, а також спричиняє дефіцит мікроелементів та вітамінів.
Креаторея (надлишкові втрати азоту в калі:> 2,5 г азоту в калі в добу) виникає лише тоді, коли вихід трипсину становить менше 10% від норми. Проблема досліджень балансу азоту полягає в труднощах відокремити внесок у втрату азоту в калі, що потрапляється в організм, порівняно з білками, що виділяються в шлунково-кишковий тракт, та бактеріями. Отже, вплив добавок ферментів на порушення перетравлення білка недостатньо добре охарактеризований. Окрім підвищеного ризику недоїдання, збільшений об’єм стільця та вміст жиру спричиняють такі абдомінальні симптоми, як біль, повнота, здуття, діарея, метеоризм та метеоризм. Від 20 до 25% випадків з екзокринною недостатністю підшлункової залози також можуть мати ускладнення переростання бактерій, що може додатково сприяти діареї та іншим симптомам ШКТ.
4. Клінічні особливості хронічного панкреатиту
Основним симптомом ХП є біль, який може проявлятися як повторними легкими або помірними нападами, так і як стійкий і невідступний біль у животі та спині.
Середня затримка між появою перших симптомів та ознаками порушення травлення становить приблизно 8-9 років при алкогольному хронічному панкреатиті та більше 15 років при ідіопатичному безалкогольному панкреатиті. У меншості пацієнтів клінічні ознаки екзокринної підшлункової залози передують іншим особливостям стану.
Пацієнти зі значною стеатореєю зазвичай відзначають рідкий, жирний, смердючий об’ємний стілець, який важко промити. Подальші клінічні прояви та ускладнення ХП наведені в Таблиця 1.
5. Харчовий статус у ХП
5.1 Вага тіла та склад тіла
Втрата ваги відбувається у пацієнтів із порушенням травлення та у тих, у кого знижений прийом їжі через біль у підшлунковій залозі. Хоча втрата ваги є частим симптомом при ХП, доступні лише обмежені дані про стан харчування хворих на ХП. Пацієнти з симптоматичним ХП мають нижчий індекс маси тіла, знижену худорляву масу та жирову масу порівняно зі здоровими контролерами. Гіпотрофія пов'язана з вищою захворюваністю (наприклад, більша частота післяопераційних ускладнень після операції з приводу хронічного панкреатиту). Отже, пацієнтів з недостатнім харчуванням слід виявляти та лікувати. Оцінка поживності виконується легко. Втрата ваги з часом, індекс маси тіла, антропометрія та деякі лабораторні показники є корисними параметрами. Крім того, показники харчового скринінгу, напр. суб’єктивна глобальна оцінка (SGA), показник харчового ризику ESPEN (ESPEN-NRS; див. www.espen.org) доступний для виявлення тих пацієнтів з дефіцитом харчування, які мають ризик розвитку ускладнень.
5.2 Метаболічна ситуація
У пацієнтів з хронічним панкреатитом витрати енергії у спокої збільшуються на 30-50%. Втрата ендокринної функції на пізніх стадіях захворювання також призводить до непереносимості глюкози і, зрештою, до відвертого діабету. Непереносимість глюкози зустрічається у 40-90% усіх випадків тяжкого хронічного панкреатиту під час перебігу захворювання. У 20-30% усіх пацієнтів розвивається інсулінозалежний діабет (тип3с). Це також пов'язано з порушенням вивільнення глюкагону та зниженням протирегуляторної здатності у разі інсулінової гіпоглікемії. Отже, у цих пацієнтів може розвинутися гіперглікемія, а також гіпоглікемія. Рекомендації полягають у прийнятті звичайного режиму їжі зі звичайними крохмалистими вуглеводами, не пропускати прийоми їжі, а приймати невеликі часті прийоми їжі, а при необхідності - індивідуальну оцінку та консультування з дієтологом.
5.3 Мінерали, мікроелементи та вітаміни
Рівень мінеральних речовин, мікроелементів та вітамінів у циркуляції знижується у хворих на ХП із порушенням травлення жиру: сюди входять магній, кальцій, незамінні жирні кислоти, а також вітаміни А, D, Е та К. остеомаляція та остеопороз. Недавній огляд повідомляє про дефіцит вітаміну А до 16%, вітаміну D у 33-87%, вітаміну Е до 27% та вітаміну К у 13-63% пацієнтів з хронічним панкреатитом.
6. Лікування, пов’язане з харчуванням
Через багатофакторний характер харчових проблем у хворих на ХП, важливо зробити індивідуальний аналіз основних причин втрати ваги у кожного пацієнта перед початком лікування. Харчове лікування завжди є частиною мультимодального плану лікування, що стосується всіх аспектів стану пацієнта.
6.1 Терапевтичні цілі
Цілі дієтичного втручання полягають не лише у лікуванні усталеного недоїдання, але також у вирішенні основної причини, наприклад, порушення травлення та порушення всмоктування, з метою запобігання розвитку подальшого недоїдання.
6.2 Заміна підшлункової залози
Введення належної кількості екзогенних ферментів підшлункової залози необхідне для корекції порушення засвоєння білків та ліпідів (Рис.5). Відповідна кількість ліпази на один прийом їжі (до 80 000 ОД) необхідна для забезпечення адекватного ліполізу. Для цих ферментних добавок не визначена доза. Зазвичай кількість необхідних добавок ферментів залежить від ступеня стеатореї, а не азотореї. Симптоматичне полегшення стеатореї та контроль ваги - практичні кінцеві точки цієї терапії. Зменшення 72-годинної екскреції жиру з калом є більш об’єктивним параметром, але збір незручний для пацієнта, нелегкий в обробці, і аналіз зараз недоступний у більшості лабораторій. Важливо давати ферменти до і під час їжі, щоб забезпечити адекватне змішування. Якщо реакція ферментного лікування не задовільна, можна спробувати додати інгібітор кислоти (інгібітор протонної помпи). Зменшення навантаження на дванадцятипалу кишку може запобігти інактивації ліпази в тонкій кишці. Оскільки розростання бактерій є частою проблемою при поглибленому ХП, це слід враховувати у пацієнтів з невдалим лікуванням.
6.3 Лікування болю
Біль є одним із основних симптомів ХП і має великий вплив на якість життя. Тому успішне лікування болю - це перший крок у лікуванні ХП. Контроль болю становить важливу основу для успіху інших аспектів лікування, включаючи харчування. Кожен пацієнт повинен вести щоденник знеболення, щоб допомогти оцінити ефективність знеболення.
Для болю доступні наступні речовини або стратегії, лікування яких повинно бути індивідуальним відповідно до реакції кожного пацієнта та обставин.
6.4 Рекомендації щодо дієти
6.5 Роль ентерального годування
Роль ентерального харчування у ХП досі суперечлива і не була адекватно досліджена у відповідних рандомізованих дослідженнях. Можливі показання до ентерального харчування перераховані в Таблиця 2.
7. Підсумок
Гіпотрофія - часта характеристика пацієнтів із ХП, порушення функції травлення та біль є двома основними причинами його розвитку. Дієтотерапію завжди слід розглядати як невід'ємну частину загальної мультимодальної медичної та хірургічної терапії хронічного панкреатиту. Часто призначають дієту з низьким вмістом жиру, але вона несе ризик зменшення загального споживання енергії, тим самим погіршуючи ступінь недоїдання. Отже, такий підхід може бути рекомендований лише тим пацієнтам, у яких контроль болю та добавки ферментів не дозволяють вирішити шлунково-кишкові симптоми. Годування через сип або ентеральну трубку - варіанти для пацієнтів, які не реагують на медикаментозну терапію, або для тих, хто переживає операцію.
8. Клінічний випадок
У 43-річного чоловіка (176 см, 66 кг, ІМТ 21 кг/м 2) спостерігалися періодичні болі у верхній частині живота та втрата ваги на 4 кг/місяці. В анамнезі виявлено періодичні епізоди гострого панкреатиту за останні 5 років. Пацієнт повідомляв про частоту стільця 3-5 об’ємних стільців на добу. УЗД верхньої частини живота (Рис.6) була проведена та виявлена неправильна паренхіма підшлункової залози з множинним кальцинозом.
Пацієнту було наказано розпочати екзогенні добавки ферментів підшлункової залози, як зазначено вище. Крім того, він отримував ліки для контролю болю на основі нестероїдних анальгетиків. Через тиждень йому було призначено повторну зустріч. Під час наступного візиту він повідомив про нормалізацію спорожнення кишечника з 1-2 стільцями на день та покращення апетиту та споживання калорій.
Q5: Чи потрібна пацієнтові в цій ситуації спеціальна дієта? Q6: Чи потрібна конкретна оцінка стану поживності?
Протягом наступних 3 місяців пацієнт набрав 4 кг маси тіла (ВМ = 23 кг/м 2) і загалом покращив свій харчовий статус. Протягом наступних 5 років він залишався стабільним без потреби у спеціальній харчовій підтримці.
Через шість років після діагностики екзокринної недостатності підшлункової залози через хронічний панкреатит у нього знову розвинулися епізоди підвищеної частоти стільця (до 4 разів на день) і схуднення (2 кг/4 місяці). Збільшення дози добавки ферменту підшлункової залози не покращило ситуацію. Для виключення злоякісної пухлини підшлункової залози було проведено КТ (Рис.7).
Після введення інгібітора протонної помпи частота стільця зменшилася до 1-2/день, а втрата ваги припинилася.
На жаль, пацієнт потрапив до лікарні через 5 тижнів із позашляховою пневмонією. Під час надходження він зазначив, що він втратив 3 кг ваги за попередні 2 тижні.
Q9: Після початку антибіотикотерапії пацієнт швидко покращився і тепер запитує, що він може зробити, щоб збільшити свою вагу під час одужання від пневмонії.
Згодом у пацієнта була висока температура та підвищені показники запалення. Діагностовано ендокардит, і, незважаючи на антибіотики, пацієнт перейшов у важкий септичний стан. Потрібна була кардіохірургія із заміною клапана. Згодом пацієнта лікували у відділенні інтенсивної терапії з вентиляцією та ентеральним харчуванням.
Q10: Яку ентеральну формулу слід використовувати?
- Керівні вправи ThatCallRak щодо діабету 2 типу - огляд аерозольного харчування Alivemax
- Чому вам не потрібні вуглеводи після тренування Міфи про харчування після тренування порушені
- (8) Найкращі засоби для зниження апетиту, які є природним та безпечним харчуванням для еволюції TRANS4ORM сплетення
- Хочете схуднути та жити здоровіше, допоможе програма наставника з питань харчування
- Чиста лінія - WPC 80 1кг - GoldTouch Nutrition