Статеві відмінності в метаболізмі енергії необхідно враховувати при зміні способу життя людей
1 Клінічна школа Святого Георгія, медичний факультет, Університет Нового Південного Уельсу, Сідней, штат Новий Південний Уельс 2052, Австралія
2 Медичне відділення лікарні Святого Георгія, Когара, штат Нью-Йорк 2217, Австралія
Анотація
Жінки мають більшу частку жиру в порівнянні з чоловіками. Однак жінки споживають менше кілоджоулів на кілограм нежирної маси і спалюють жир переважно під час фізичних вправ у порівнянні з чоловіками. Під час гестації жінки накопичують ще більшу кількість жиру, що не можна пов’язати виключно зі збільшенням споживання енергії. Ці спостереження дозволяють припустити, що взаємозв'язок між споживаними кілоджоулями та використаними кілоджоулями різний у чоловіків та жінок. Причина цих статевих відмінностей в енергетичному обміні невідома; однак, це може стосуватися статевих стероїдів, відмінностей в інсулінорезистентності або метаболічних ефектів інших гормонів, таких як лептин. Розглядаючи модифікації способу життя, слід враховувати статеві відмінності в енергетичному обміні. Більше того, з’ясування регуляторної ролі гормонів в енергетичному гомеостазі є важливим для розуміння патогенезу ожиріння, і, можливо, в майбутньому це може призвести до способів зменшення жиру в організмі з меншим обмеженням енергії.
1. Вступ
Перша половина цієї статті присвячена розбіжностям між чоловіками та жінками: викладено гендерні відмінності ФМ, обговорено аспекти енергетичного метаболізму, які можуть враховувати ці відмінності, та обговорено ключові метаболічні ролі гормонів яєчників. На цьому тлі друга половина цієї статті присвячена структурі тіла та енергетичному балансу під час вагітності.
2. Гендерні відмінності у складі тіла протягом усього життя
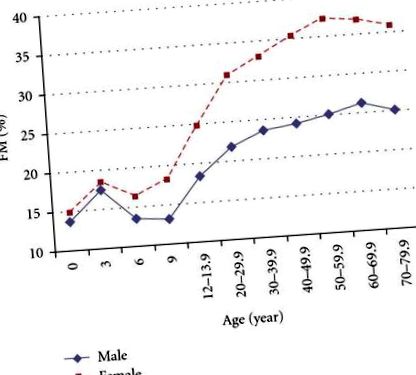
Як і багато ссавців, люди демонструють суттєві відмінності у нежирній масі (ШЖМ) та ФМ між статями. Національне обстеження здоров’я та харчування III (NHANES III) з 15 912 суб'єктів показав, що неіспаномовні білі жінки у віці від 12 до 80 років мають більш високий відсоток ФМ, ніж чоловіки, починаючи з пубертату і варіюючи від 6% до 11% вище за кожне вивчене десятиліття (див. Таблицю 1 та рисунок 1) [10]. Інші дослідження також підтверджують думку, що значні статеві розбіжності у складі тіла починаються із статевим дозріванням [3]. Ця різниця між статями зберігається в усіх етнічних групах і спостерігається у всіх популяціях, хоча на її величину впливають етнічні, генетичні та екологічні фактори [11]. Мало того, що різниця у відсотках ЧМ між статями, є також добре відома різниця у розподілі жиру в організмі.
3. Гендерна різниця в енергетичному обміні
Можна припустити, що жінки накопичують більше жиру, оскільки вони споживають більше енергії, ніж витрачають, або що вони споживають жир ефективніше. Однак, якщо порівнювати добове споживання енергії в когорті суб'єктів NHANES III, чоловіки споживали більше енергії, навіть після того, як налаштувались на знежирену масу (187 кДж кг -1 проти 170 кДж кг -1) [1, 10]. Одне з можливих пояснень полягає в тому, що жінки ефективніше зберігають енергію та зберігають її як жир. Підтвердженням цього поняття є визнання того, що жінки повинні зменшити споживання їжі на більшу частку, щоб досягти такого ж ступеня втрати ваги, як і чоловіки [12]. Іншим спостереженням є те, що в першій половині вагітності жінки збільшують рівень ФМ без очевидного збільшення споживання енергії або зменшення витрат. Ця здатність збільшувати FM без суттєвого збільшення споживання енергії вказує на існування метаболічних адаптацій, які можуть сприяти різниці статей у FM.
3.1. Вправа Метаболізм
Різниця у швидкості окислення глюкози та жиру під час фізичних вправ, схоже, не пояснює гендерну різницю у ЧМ. Жінки переважно спалюють паливну суміш із підвищеним вмістом жиру та глюкози під час фізичних вправ [13]. Незважаючи на це, жінки втрачають менше жиру, ніж чоловіки, стикаючись із подібним дефіцитом енергії [14–17]. Це може бути пов’язано з більш ефективним накопиченням жиру в періоди поза фізичними вправами [18, 19], враховуючи, що у більшості здорових людей менше 5% дня витрачається на фізичні вправи. Більш висока маса жиру у жінок може дозволити їм переважно використовувати це джерело енергії як паливо під час тренувань, тоді як у неспортивні періоди жінки накопичують жир ефективніше порівняно з чоловіками.
3.2. Метаболізм після їжі
Оскільки жінки не споживають більше енергії в порівнянні з чоловіками, проте переважно окислюють жир під час фізичних вправ, цілком логічним є припущення, що їх більший рівень ФМ обумовлений збільшенням накопичення жиру в періоди нетренування. Дійсно, було виявлено, що жінки відразу після фізичних навантажень повертаються до стану зниженого окислення жирних кислот, яке зберігається годинами [21]. Крім того, повідомляється, що випуск вільних жирних кислот після їжі з жирової тканини нижчий у жінок, ніж у чоловіків [22, 23]. Кілька поперечних досліджень, що порівнювали чоловіків і жінок, продемонстрували, що чоловіки окислюють більший відсоток вживаного жиру [24, 25]. Використовуючи радіодинаміки, ці автори також показали, що поглинання жирних кислот після їжі підшкірними та жировими тканинами нижньої частини тіла було вищим у жінок, ніж у чоловіків. Оскільки кількість енергії, витраченої в станах після абсорбції та після прийому їжі, більша, ніж під час фізичних вправ, це буде мати велике значення для загального накопичення жиру та FM.
Вважається, що естроген частково відповідає за це зменшення окислення жирних кислот після їжі. Проспективні дослідження з використанням пероральної естрогенної терапії повідомили про зменшення окислення жирних кислот після їжі. Одне дослідження виявило значне зменшення окислення жирних кислот після їжі, пов’язане з незначним збільшенням FM [27]. Подібні зміни були виявлені у жінок з дефіцитом гормону росту при пероральній терапії естрогенами [28]. В іншому дослідженні повідомлялося про більш значне зменшення окислення жирних кислот після їжі пероральним естрогеном порівняно з трансдермальною терапією, пов’язаною зі значним збільшенням рівня ФМ [29]. Це спостереження, яке залежить від шляху, підвищує ймовірність того, що пероральна естрогенна терапія впливає на печінку під час метаболізму першого проходження. Отже, дослідження з використанням екзогенних естрогенів продемонстрували, що ефективне накопичення жиру у жінок опосередковується зменшенням окислення жирних кислот після їжі, швидше за все, через естрогенний вплив на печінкову переробку харчових жирів.
Однак метаболічний ефект лікування екзогенним естрогеном може відрізнятися від ендогенних естрогенів з кількох причин. Екзогенні синтетичні естрогени, як правило, є більш потужними [30], і вони мають різні фармакокінетичні властивості [31]. Існує кілька типів ендогенних естрогенів, і кожен може мати дещо різні або синергетичні дії [30]. Перспективні дослідження під час гіпероестрогенного стану вагітності ідеально підходять для вивчення впливу ендогенних естрогенів на окислення жирних кислот після їжі. Однак логістичні труднощі вивчення вагітності перед вагітністю означають, що на сьогоднішній день існує обмежена кількість перспективних досліджень, що мають достатній обсяг вибірки, щодо енергетичного обміну під час вагітності. Spaaij та ін. [32] досліджував 27 жінок від вагітності до пологів. Вони виявили, що окислення жиру після їжі не відрізнялося від значень препрегнантів протягом перших 13 тижнів і фактично зростало після цього. У поперечних дослідженнях Nagy та King [33] не виявили різниці в окисленні жирних кислот після їжі між 6 невагітними та 10 вагітними, тоді як більш масштабне дослідження (
) виявили значне зменшення окислення жирних кислот у групі вагітних [34]. Однак через значні варіації між предметами, результати перехресних досліджень слід інтерпретувати з обережністю.
На закінчення було показано, що зменшення окислення жирних кислот після їжі сприяє посиленню FM. Екзогенне лікування естрогеном викликає це зменшення, можливо, пригнічуючи печінкову переробку харчових жирів під час метаболізму першого проходження. Однак через складну дію ендогенних естрогенів, невелику кількість досліджень та невідповідність у структурі досліджень, вплив ендогенних естрогенів на метаболізм вимагає подальших досліджень.
4. Регулювання обміну речовин і складу тіла за допомогою статевих гормонів
Більша частка ФМ серед жінок та збільшення ФМ у першій половині вагітності можуть бути зумовлені впливом статевих гормонів на метаболічні процеси, такі як ліполіз та зберігання жирних кислот. У переглянутій літературі є дані, що свідчать про те, що ці ефекти можуть опосередковуватися через печінкові мішені, адипоцитарні мішені та адипокіни, такі як лептин. Однак те, як ці шляхи взаємодії є складним і загалом недостатньо зрозумілим.
4.1. Печінкові цілі
Естроген може надавати інгібуючу дію на окислення жирних кислот у печінці, головне місце метаболізму жирних кислот. Кілька в пробірці Дослідження на мишачих гепатоцитах показали, що фармакологічні концентрації естрогену знижують кетогенез (продукт окислення жирних кислот) та збільшують вбудовування жирних кислот у тригліцериди [9, 35]. Подібні висновки були зареєстровані у людей, де пероральна естрогенна терапія, яка проводилась жінкам з гіпогонадою та постменопаузою, зменшувала постпрандіальне окислення жиру та підвищувала рівень тригліцеридів [29, 36–38]. Це вказує на те, що екзогенний естроген направляє внутрішньопечінкові жирні кислоти подалі від окисних шляхів і в ліпогенні шляхи.
Навпаки, ефекти ендогенних естрогенів набагато важче з’ясувати. Дослідження, що порівнювали жінок у фолікулярній та лютеїновій фазах менструального циклу, не виявили різниці в енергетичному обміні, можливо тому, що зміна рівня естрогену різниться, а також є вплив прогестерону [24, 39]. Дослідження, що співвідносять концентрацію естрогену та окислення жирних кислот після їжі у вагітних та невагітних осіб, розглядали метаболізм жиру у всьому організмі, а не виділяли вплив на печінку. Крім того, прогестерон, який, як було показано, має синергетичний та антагоністичний ефект, залежно від системи органів, з естрогеном у цьому контексті не вивчався [8].
4.2. Адипоцитарні цілі
Рецептори естрогену, прогестерону та андрогену присутні в жировій тканині [26]. Як видно з таблиці 2, експресія цих рецепторів змінюється залежно від депо та статі [40, 41]. Рецептори естрогену вищі у підшкірних відкладеннях у жінок, що може пояснити, чому у жінок спостерігається більша кількість підшкірних сідничних та стегнових відкладень жиру [40, 41]. Генетичні чоловіки з нечутливістю до андрогенів мають габітус жіночого тіла [42], тоді як жінки, яким дають екзогенні андрогени або страждають від вірілізаційних розладів, розвиватимуть габітус чоловічого тіла [40, 43–45]. У жінок у постменопаузі спостерігається збільшення співвідношення талії та стегна та кількості депо вісцеральної жирової тканини [32, 46, 47], яке частково змінюється при введенні естрогену [48]. Усі ці дані свідчать про те, що зв'язування статевих гормонів з рецепторами жирової тканини, можливо, сприяє адипогенезу в деяких регіонах тіла. Хоча, як відомо, багато генів в адипоцитах транскрипційно регулюються статевими гормонами [26], точні клітинні механізми до кінця не з’ясовані.
4.3. Лептин
Лептин - гормон, отриманий з жирової тканини, який пригнічує збільшення жиру, сприяючи гіпофагії та гіперметаболізму [49]. Таким чином, лептин відіграє важливу роль у допомозі ФМ залишатися відносно постійним протягом дорослого віку. Існує різниця між рівнями рівнів лептину, яка розвивається в період статевого дозрівання, і, як вважають, індукується статевими гормонами.
У жінок концентрація лептину вища на кілограм маси тіла, ніж у чоловіків. Ця різниця усувається після коригування концентрації статевих гормонів у циркуляції [50]. Дослідження виявили, що вироблення лептину пригнічується андрогенами, а стимулюється естрогенами [26, 50]. Естроген має прямий вплив на FM, оскільки підвищує експресію лептину в адипоцитах [51]. Центральні ефекти можуть також бути присутніми, оскільки в ядрах гіпоталамусу були виявлені рецептори естрогену, що контролюють енергетичний гомеостаз. Циркулюючі естрогени пропонується зв’язувати з цими рецепторами та змінювати чутливість гіпоталамусу до опосередкованих лептином сигналів, впливаючи таким чином на секрецію лептину і, можливо, впливаючи на метаболізм і навіть фертильність [52–54].
Однак взаємозв'язок між лептином, естрогеном та складом тіла є складним, оскільки при менопаузі чи при замісній терапії естрогеном лептин не змінюється [26]. Втрата ваги пов’язана зі зниженням рівня лептину та гіпогонадизмом [55]. Крім того, гіперандрогенія та зменшення стрибків естрогену при полікістозі яєчників не впливають на рівень лептину [56, 57]. Отже, на роль лептину в регуляції ФМ потенційно може впливати естроген, однак механізм дії не повністю зрозумілий.
5. Енергетичний баланс при вагітності
Жіноче розмноження вимагає підвищеної кількості енергії. Проте протягом історії жінки доводили свою концепцію до кінця в широкому діапазоні харчових умов. Це говорить про наявність потужних метаболічних адаптацій [3]. Під час гестації потрібна енергія для росту тканин зачаття та розмноження, підтримки цих тканин та підготовки до лактації. Батт і Кінг [58] виявили, що середній приріст ваги в 13,8 кг, що включає 4,3 кг жиру, відповідає гестаційним потребам у енергії. На основі цієї моделі Продовольча та сільськогосподарська організація, Всесвітня організація охорони здоров’я та Університет ООН розрахували енергетичну потребу вагітності 360–370 МДж. Це дорівнює додатковим 1300 кДж/день, що на 15% перевищує потреби невагітних. Однак, як було показано, гестаційні вимоги коливаються від 30 МДж до 520 МДж у жінок, які недоїдають та недоїдають [59]. Ця мінливість вказує на наявність метаболічних адаптацій для підтримки вагітності в різних харчових умовах.
Теоретично цей додатковий попит можна задовольнити або збільшенням споживання енергії, зменшенням витрат та/або мобілізацією запасів жиру. На відміну від очікувань, численні проспективні та поперечні дослідження показали, що перша половина вагітності пов’язана з незначним збільшенням споживання енергії або його відсутністю [6, 60–62]. В одному дослідженні жінки прослідковувались протягом вагітності та повідомляли, що споживання енергії в першому триместрі вагітності ідентичне до вагітності [63]. Замість зменшення витрат енергії поступово зростали під час гестації [4, 64, 65]. Подібним чином про зміни в термогенезі, викликаному дієтою під час вагітності, не повідомлялося постійно, і тому зменшення термогенезу, спричиненого дієтою, може не враховувати позитивний енергетичний баланс [4, 33, 66–70].
Ці вищезазначені спостереження підвищують можливість того, що енергетичні витрати вагітності покриваються зменшенням загальних енергетичних витрат. Однак переконливі дані не показують, що значне збільшення споживання енергії або зменшення витрат енергії є основним фактором, що сприяє збільшенню ЧМ у першій половині вагітності. Важливо також зазначити, що вагітність є дуже пластичним метаболічним станом, оскільки навіть недоїдаючі жінки можуть підтримувати ФМ [59]. Отже, причина гестаційного набору жиру може бути головним чином через зміни метаболічних шляхів, що регулюють окислення або зберігання певного палива, особливо жиру.
6. Висновок
Протягом свого репродуктивного життя жінки підтримують більшу частку жиру в організмі порівняно з чоловіками, і ця різниця посилюється під час гіпероестрогенного стану вагітності. Однак дослідження не змогли продемонструвати надлишок енергії за всіма показниками. Можливо, жінки недооцінюють споживання їжі; проте деякі дослідження повідомляють, що чоловіки недооцінюють споживання їжі порівняно з жінками [71]. Також слід враховувати відмінності у фізичній активності між статями. Жінки мають більший відсоток жиру в організмі, і цілком можливо, що гормони яєчників, особливо естроген, можуть враховувати ці спостереження, сприяючи перетворенню харчової енергії після їжі у жир. Ця теорія повинна бути підтримана великими проспективними дослідженнями та дослідженнями під час природних гіперестрогенних станів, таких як вагітність. Дія естрогенів може бути опосередкована через гепатоцитні та адипоцитарні мішені та через регуляцію гормонів, таких як лептин. Потрібні подальші дослідження, щоб з’ясувати, як ці гормональні шляхи взаємодіють та впливають на цілі.
Розглядаючи модифікацію способу життя, слід враховувати різницю в статі в енергетичному обміні. Потрібно використовувати цілі, що враховують стать, а не лише масу тіла або споживання енергії. Враховуючи високу поширеність ожиріння в сучасному суспільстві, важливо розуміти фактори, що регулюють енергетичний гомеостаз і згодом сприяють надлишку жирових відкладень. У майбутньому це розуміння може завершитися стратегіями контролю або зменшення набору жиру, які не лише підкреслюють обмеження енергії.
Список літератури
- Танці на полюсі плюс розмір - все, що вам потрібно знати - Basicinvert78 Блог танцюриста на полюсі
- Одне, що мені потрібно цього Різдва, і багато чого - Блог
- Merz - Поширені запитання - Все, що вам потрібно знати про продукцію Merz Spezial
- Порушення метаболізму та харчування Семаглютид, プ ラ セ ボ (セ マ ル ル チ ド) の 臨床 試 験 - 臨床 試 験 登録 -ICH GCP
- ЗАРАЗ Пивовар; s Дріжджі 454g Body Energy Club