Роль біогенних амінів в огляді харчової токсикології - Роль біогенних амінів у
Роль біогенних амінів у харчовій токсикології: огляд
1 Університет наук про здоров'я (Стамбул), медичний факультет Хамідіє, кафедра медичної біохімії, Стамбул, Туреччина
2 Міністерство охорони здоров’я, Невшехірська державна лікарня, відділення урології, Невшехір, Туреччина
3 Університет Істіньє, медичний факультет, Стамбул, Туреччина
Анотація
Біогенні аміни, які відповідають за реалізацію багатьох фізіологічних умов нашого організму, - це сполуки, які можуть вироблятися мікроорганізмами, особливо у ферментованих продуктах з високим вмістом білка. Вони можуть мати шкідливий вплив на здоров’я людини лише у тому випадку, якщо їх приймати у великих кількостях разом з їжею. Однак у осіб з порушенням антитоксичного метаболізму, який відповідає за детоксикацію, навіть менші кількості можуть викликати токсичні ефекти. Найпоширенішими наслідками для здоров’я є нудота, блювота, сильний головний біль, гіпотонія, гіпертонія, тахікардія, різні алергічні реакції, біль у животі та смерть у більш важких випадках. З цих причин законодавство про біогенні аміни в продуктах харчування було встановлено з деякими обмеженнями. Виробників продуктів харчування попросили дотримуватись цього законодавства. Однак, незважаючи на всі запобіжні заходи, біогенні аміни з продуктів харчування не були повністю видалені. Потрібні подальші дослідження для пошуку ефективних рішень для запобігання утворенню біогенних амінів. Крім того, споживачів потрібно поінформувати про цю проблему.
Отримано 10 січня 2020 р .; Прийнято 16 січня 2020 р .; Опубліковано 18 січня 2020 р .;
Академічний редактор:Махіпал Сінгх Сангла, Університет Галготіаса, Департамент судових експертиз, Індія
Перевірено на наявність плагіату: Так
Огляд:Односліпий
Конкуруючі інтереси
Автори заявили, що не існує конкуруючих інтересів.
Цитування:
Вступ
Потенціал біогенного утворення амінів мікроорганізмів у ферментованих продуктах харчування може бути абсолютно різним. Це пов’язано з ферментною активністю декарбоксилази мікроорганізмів. Тому виявлення бактерій з активністю ферменту декарбоксилази є важливим для запобігання накопиченню біогенних амінів у продуктах харчування. Крім того, ці шкідливі сполуки повинні бути відомі як для здоров'я людини, так і за якості їжі. Сьогодні в багатьох країнах існують законодавчі акти щодо вмісту та кількості біогенних амінів у ферментованих продуктах. Ці законодавчі акти та норми в основному спрямовані на запобігання накопиченню біогенного аміну в харчових продуктах. Вони орієнтовані на виробника 1, 4, 5. Однак ці заходи не повністю обмежили утворення біогенного аміну. Також підвищення обізнаності споживачів є одним з найефективніших рішень у цьому плані.
Біогенні аміни
Біогенні аміни - це органічні сполуки азоту з невеликою молекулярною масою. Біогенні аміни утворюються внаслідок декарбоксилювання амінокислот під час перетворення вуглеводних одиниць молочної кислоти та органічних сполук мікроорганізмами, що забезпечують дозрівання їжі (бродіння). При прийомі у великій кількості вони викликають харчову інтоксикацію. Токсична кількість біогенних амінів утворюється під час переробки, приготування та зберігання багатих білком рослинних і тваринних продуктів. Природні біогенні аміни в клітинах тварин і людини утворюються шляхом декарбоксилювання амінокислот або амінування та трансамінування альдегідів та кетонів. Це особливо молекули, що мають ароматичну та гетероциклічну структуру. П'ять природних біогенних амінів (дофамін, норадреналін, адреналін, гістамін та серотонін) відіграють важливу роль в організмі як нейромедіатори 6, 7, 8. Однак вони можуть спричинити шкідливі наслідки, якщо приймати їх разом з великою кількістю їжі.
Відповідне середовище потрібне для реакцій декарбоксилювання під час утворення біогенних амінів. Це середовище забезпечується процесами приготування харчових продуктів, такими як наявність вільних амінокислот, мікробне забруднення та термічна обробка. Біогенні аміни (такі як адреналін, гістамін, тирамін та серотонін), які беруть участь у нормальних фізіологічних процесах, слід оцінювати інакше, ніж токсичні біологічні аміни 6, 9, 10, 11. Усі біогенні аміни, що походять від катехолу, складаються з амінокислоти тирозину, яка є загальним попередником. Біогенні аміни можна дуже точно виявити за допомогою GS-MS або HPLC 12 .
Дофамін
Дофамін, важливий біогенний амін, відповідальний за почуття мотивації та винагороди, синтезується шляхом декарбоксилювання 3,4-дигідроксифенілаланіну (рис. 1). Дофамін зазвичай міститься в смугастому тілі, яке відіграє важливу роль у координації рухових рухів тіла 13, 14. Вважається, що цей регіон дегенерував при хворобі Альцгеймера. Отже, для компенсації зниженого дофаміну вводять L-допу, яка може переходити гематоенцефалічний бар’єр при лікуванні. Однак не слід ігнорувати стан ферментів декарбоксилази, що перетворює молекули дофаміну, та периферичний катаболізм L-допи. Як відомо, як тільки L-допа приймається, вона швидко катаболізується в кишечнику та периферичних тканинах. Тому L-допу вводять разом з карбідопою, інгібітором дофаміндекарбоксилази, який не проходить гематоенцефалічний бар'єр, та селегіліном, інгібітором моноаміноксидази (МАО) 15, 16. Однак гідразин, продукт розпаду карбідопи, є генотоксичним і, можливо, канцерогенним. Дофамін також використовується для лікування шоку, оскільки збільшує ниркові артерії та активує β-адренергічні рецептори в серці та збільшує серцевий викид.
Фігура 1. Біогенні амінні нейромедіатори, синтезовані з амінокислот тирозину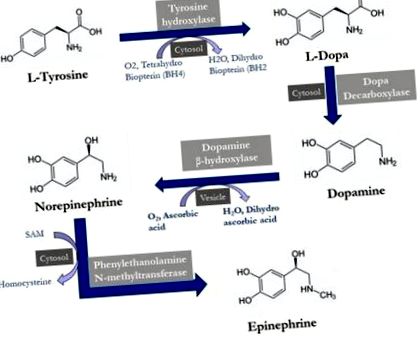
У дослідженні, що вивчає ниркові ефекти біогенних амінів; Встановлено, що дофамін та 5-гідрокситриптамін перетворюються один на одного за допомогою ароматичного ферменту L-амінокислоти декарбоксилази в клітинах канальців нирок 17. L-допа та дофамін впливають на перенесення Na + за межі клітини та K + всередині клітини шляхом оборотного інгібування Na + -K + АТФази. Ці вазоактивні аміни діють на дофамінергічні рецептори в ниркових та коронарних судинах, збільшуючи кровотік, не змінюючи артеріального тиску. Тому вони прискорюють клубочкову фільтрацію, одночасно збільшуючи нирковий кровотік. Він також інгібує синтез альдостерону та насоси Na-K АТФази, що призводить до натрійурезу 18, 19. Це ускладнює утримання води в внутрішньосудинній зоні. Це також свідчить про те, що біогенні аміни, що надходять з їжею, можуть призвести до змін артеріального тиску та ниркових ефектів через внутрішньониркові перетворення. Це спричинить більш серйозні проблеми зі здоров'ям у пацієнтів із порушенням антитоксичного метаболізму, пацієнтів з артеріальною гіпертензією/гіпертоніком та хворих із захворюваннями серця або нирок.
Рівень дофаміну пов'язаний з деякими урологічними захворюваннями. Наприклад, було встановлено, що бупропіон, інгібітор зворотного захоплення норадреналіну-дофаміну (НДРІ), зменшує рухливість сперми у щурів при дозі ≥30 мг/кг. Однак повідомляється, що метилфенідат, NDRI, збільшує частоту сперми при патологічній морфології хвоста у щурів, збільшує кількість сперматогоній та сперми та зменшує кількість круглих сперматид. Крім того, повідомляється, що сибутрамін скорочує проходження сперми з епідидимісу та зменшує загальну кількість сперми в епідидимісі у щурів 20. Чен Г. та ін. продемонстрував, що порушення шляху рецептора дофаміну-2 у базолатеральній мигдалині у щурів може сприяти розвитку неорганічної еректильної дисфункції (ЕД), а також, що агоністи рецепторів дофаміну-2 можуть реабілітувати ЕД у моделей щурів з неорганічним ЕД 21 .
Норадреналін
Інший біогенний амін, норадреналін, синтезується з дофаміну за допомогою ферменту дофаміну β-гідроксилази, що знаходиться у везикулах. Звідси він транспортується до адренергічних нервових закінчень. Найвидатнішим класом нейронів, що експресують норадреналін, є симпатичні клітини гангліїв 13, 14, 22. Норадреналін також є важливим передавачем locus coeruleus, ядра стовбура мозку, пов'язаного зі сном і пильністю, увагою та поведінкою годування. Як показано на малюнку 2, норадреналін - це нейромедіатор, який діє на гладкі м'язи в постгангліонарних симпатичних нейронах, викликаючи скорочення або розслаблення тип рецепторів. Дофамін - це нейромедіатор, який модулює холінергічну передачу в вегетативних гангліях. Він також пригнічує реабсорбцію Na + та H2O у нирках та викликає розширення судин 23, 24, 25. Адреналін і норадреналін - це нейрогуморальні агенти, які виділяються в кров через мозковий мозк надниркових залоз. Кількість вивільненого адреналіну досить висока у порівнянні з норадреналіном. Всі ці біогенні аміни необхідні для фізіологічних функцій організму. Однак, приймаючи їх у великих кількостях, вони викликають серйозні проблеми.
Малюнок 2. Розташування норадреналіну (NE), адреналіну (E) та ацетилхоліну (ACh) на прегангліонарному та постгангліонарному нервових закінченнях у симпатичній нервовій системі.
Надлишок норадреналіну в різних тканинах був пов’язаний з деякими захворюваннями. Наприклад, у дослідженні Stein et al. Було повідомлено, що норадреналін підвищується в сечі у пацієнтів з інтерстиціальним циститом 26. Diederichs та ін. повідомляли, що внутрішньокавернозне введення норадреналіну (залежно від дози) зменшує ерекцію статевого члена через кавернозний нерв. Симпатична стимуляція зменшує або повністю усуває ерекцію пеніса, спричинену ацетилхоліном або вазоактивним кишковим поліпептидом. Було зроблено висновок, що норадреналін є важливим нейромедіатором у контролі детумесценції пеніса 27 .
Адреналін
Адреналін присутній у мозку на нижчих рівнях, ніж інші катехоламіни. Його ще називають адреналіном. Фенілетаноламін-N метилтрансфераза, яка синтезує адреналін, присутня лише в нейронах, які секретують адреналін. Функція нейронів, що містять адреналін, у центральній нервовій системі до кінця не вивчена. У катаболізмі катехоламінів беруть участь два основних ферменти - мітохондріальна моноаміноксидаза (МАО) та цитоплазматична катехол-О-метилтрансфераза (КОМТ) у нейронах та гліальних клітинах. Інгібітори цих ферментів використовуються як антидепресанти в психіатричних клініках 22, 28, 29. Особливо він виробляється мозковим речовиною наднирників, який є постсинаптичним гангліозним органом, досягаючи периферичних тканин через кровообіг. Він виробляється мозковим речовиною наднирників, який є постсинаптичним ганглієм, і досягає периферичних тканин через кровообіг.
Адреналін має багато життєво важливих ефектів і має місце в лікуванні. Наприклад, він все ще успішно використовується при лікуванні екстрених випадків приапізму 30. Крім того, внутрішньоміхурове введення адреналіну пригнічувало крововиливи та запалення в сечовому міхурі у моделі щурів, що має геморагічний цистит, індукований циклофосфамідом 31 .
Гістамін
Гістамін - це біогенний амін, синтезований з гістидину гістидиндекарбоксилазою. Гістамінметилтрансфераза та МАО беруть участь у його катаболізмі. Гістамін та гістидиндекарбоксилаза знаходяться в нейронах гіпоталамуса, а гістамінові рецептори інтенсивно знаходяться в нейронах майже у всіх регіонах головного та спинного мозку. Гістамін опосередковує збудження та увагу в центральній нервовій системі, а також ацетилхолін та норадреналін 32, 33. У периферичних тканинах гістамін виділяється з тучних клітин у відповідь на пошкодження тканин та алергічні реакції. Гістамін також ефективний для модуляції скорочення сечового міхура. Стромберга та ін. повідомлялося, що стимуляція гістамінових рецепторів H1 спричиняла скорочення як власної пластинки, так і тканини детрузора сечового міхура. Активація гістамінових рецепторів Н2 лише запобігає опосередкованому скороченню рецептора Н1 у власній пластині, а не в тканині детрузора. На основі цих результатів рецептори Н1 та Н2 можуть бути потенційними мішенями в майбутньому при лікуванні гіперактивного сечового міхура та інших порушень скорочення сечового міхура 34 .
Серотонін
Малюнок 3. Синтез 5-гідрокситриптаміну з амінокислоти триптофану
Обговорення
Хоча біогенні аміни присутні в низьких концентраціях у свіжих продуктах, вони можуть призвести до більш високих ефектів, ніж очікувалося, особливо якщо їх приймати разом з багатими білками тваринами. Біогенні аміни в перероблених ферментованих харчових продуктах, біогенні аміни, що утворюються в результаті мікробного декарбоксилювання, харчові продукти, біогенні аміни, що утворюються в результаті дезамінування альдегідів та кетонів, також можуть підвищувати рівень крові до високих рівнів 38, 39. Як і в продуктах з високим вмістом білка, таких як ферментація або термічна обробка риби та рибних продуктів, м’яса та м’ясних продуктів, молока та молочних продуктів; Продукти з низьким вмістом білка, такі як вино, пиво, овочі, фрукти, також можуть містити високий рівень біогенних амінів 38, 40 .
На додаток до природних біогенних амінів існує багато різних видів біогенних амінів, які мають ризик прийому всередину. Найважливішими з них є кадаверин, путресцин, спермін, спермідин, агматин, фенілетиламін, тирамін, триптамін, гістамін, кадаверин, агматин, спермін та спермідин 41, 42. Кожен з цих біогенних амінів, навіть якщо його приймати у великих кількостях, має потенційні токсичні ризики. Більше того, токсичні ефекти, як правило, зумовлені ефектом декількох біогенних амінів, а не одного біогенного аміну. Найбільш токсичними з цих біогенних амінів та найважливішими з точки зору безпечності харчових продуктів є гістамін та тирамін 43. В основному їх виробляють ферментовані продукти та інтенсивна мікробна активність. Коли гістамін приймається у високих концентраціях, він викликає викид адреналіну та норадреналіну, стимуляцію гладкої мускулатури, стимуляцію сенсорних та рухових нейронів, гіпотонію та алергічні реакції. Тирамін викликає гіпертонію, тахікардію, гіперкапнію, гіперглікемію та головний біль.
Вперше ароматичні аміни були визначені канцерогенами в лакофарбовій промисловості. Зокрема, 4-амінобіфеніл та 2-нафтиламін є добре відомими канцерогенами сечового міхура людини. Ці гетероциклічні ароматичні аміни є продуктами піролізу білків, які також містяться в пересмаженій їжі та тютюновому димі 48. Вживання тютюну та вплив на нього професійних ароматичних амінів є двома визначеними факторами екологічного ризику раку сечового міхура, і запобігання їх впливу суттєво сприяло зниженню смертності, особливо серед чоловіків 49. Міжнародне агентство з досліджень раку (IARC) повідомило, що у більшості країн при раку, пов'язаному з сигаретами, що є запасом ароматичних амінів, пов'язаний з цим ризик сягав до 50% у чоловіків та 25% у жінок 50. Більше того, повідомлялося, що одним з найбільш чітко визначених факторів ризику нирково-клітинної карциноми є сигарета, джерело ароматичного аміну 51. Крім того, дослідження на тваринах показали, що α-дифторметилорнітин, інгібітор біосинтезу поліамінів, може інгібувати утворення пухлини шкіри 52 .
Sıddıqui та ін. встановлено, що 5-гідрокситриптамін викликає проліферацію в клітинах, а антагоністи 5-гідрокситриптаміну пригнічують проліферацію в різних пухлинних клітинах, таких як карцинома простати, карцинома легенів та карцинома товстої кишки 53. У дослідженні, яке досліджувало вплив серотоніну на карциному передміхурової залози людини (Abdul et al.), Повідомлялося, що серотонін, біогенний амін, збільшує ріст пухлин передміхурової залози і, отже, може бути ціллю для лікування 54 .
Висновок
Як результат, оскільки біогенні аміни є фактором, що сприяє розвитку раку, а також викликає багато токсичних ефектів, кількість біогенних амінів у тваринних та рослинних продуктах харчування є важливим. Тому, як і раніше, необхідні дослідження, які знайдуть ефективні рішення для запобігання утворенню біогенних амінів. Крім того, про це слід поінформувати як виробників, так і споживачів.
Розкриття інформації
У цій роботі немає жодного потенційного конфлікту інтересів авторів. Автори не отримали фінансової підтримки для цього дослідження.
- Вулкан від Unico Nutrition Review Хороший жиросжигатель
- Роль харчування в геріатричній реабілітації - PubMed
- Що таке дієта Sirtfood Тут є огляд дієтолога з блогу харчування HUM
- Вулкан жироспалювач Unico Nutrition Review
- Unico Nutrition Vulcan Review (ОНОВЛЕНО 2018) - чи справді це працює