Рандомізоване, подвійне сліпе і плацебо-контрольоване дослідження кленбутеролу при денервованій атрофії м’язів
1 відділення хірургії кисті лікарні Хуашань Університету Фудань, Шанхай 200040, Китай
2 Clinical Development, Neurology & Pain, R&D, Allergan Inc., 2525 Dupont Dr., Irvine, CA 92612, USA
Анотація
-Показано, що адренергічні агоністи, такі як кленбутерол, сприяють гіпертрофії здорових скелетних м’язів та зменшують втрату м’язів у деяких патологічних станах як у тварин, так і у людей. Ми мали намір дослідити клінічну ефективність кленбутеролу щодо послаблення атрофії м’язів, спричиненої денервацією. Методи. Було використано подвійне сліпе, контрольоване плацебо, паралельне та рандомізоване дослідження. 71 пацієнту, який страждав від пошкоджень плечового сплетення, було призначено або кленбутерол (60 μг, заявка) або плацебо протягом 3 місяців. До і в кінці дослідження пацієнтам проводили фізичні обстеження, біопсію біцепса плеча, електроміограми (ЕМГ) та інші лабораторні дослідження. Результати. Порівняно з лікуванням плацебо, кленбутерол значно пом'якшив зменшення площ поперечного перерізу м'язових волокон I та II типів та полегшив зменшення амплітуд потенціалу фібриляції без будь-яких негативних наслідків. Висновки. Кленбутерол безпечно покращував денервовану атрофію м’язів у цій когорті; таким чином, рекомендується проводити більші клінічні дослідження для того чи іншого
агоністи щодо індукованої денервацією атрофії м’язів.
1. Вступ
Показано, що селективні бета-2-адренергічні агоністи збільшують масу скелетних м’язів і функціонують у фізіологічних умовах у різних видів. Це пояснюється їхньою роллю в контролі синтезу та деградації білка через
та Gβγ зв’язані сигналізації та Ca 2+/залежні від убиквітину шляхи відповідно [1]. β2 агоністи також покращують виснаження м’язів тварин при денервації, бічному аміотрофічному склерозі, м’язовій дистрофії, знежиренні, старінні та моделях розвантаження міокарда [2–8].
У пацієнтів з умовами іммобілізації або м’язовою дистрофією, β2 агоністи, такі як кленбутерол, збільшують м’язову масу тіла та покращують функції скелетних м’язів [9–11]. Крім того, кленбутерол (до 720 μг/добу) сприяє одужанню міокарда у пацієнтів з атрофією розвантажувального міокарда в результаті застосування допоміжних апаратів лівого шлуночка [12–14].
У порівнянні з іншими β2 агоністи, кленбутерол, засіб тривалої дії та функціонально селективний засіб, є найефективнішим препаратом для запобігання виснаження м’язів з найменшими побічними ефектами [13, 15–18]. Однак клінічна ефективність кленбутеролу при денервованій атрофії м'язів ще не повідомляється; денерваційна атрофія м’язів залишається незадоволеною медичною потребою. Також статус атрофії м’язів в кінцевому рахунку визначає функціональне відновлення відновлених пошкоджень периферичного нерва [19]. На основі β2 ролі агоністів у сприянні гіпертрофії неушкоджених скелетних та серцевих м’язів, а також у запобіганні втраті м’язів у доклінічних дослідженнях, ми висунули гіпотезу, що кленбутерол може пом’якшити денервовану атрофію м’язів у людей. Нинішнє пілотне випробування перевірило вплив кленбутеролу на уповільнення денерваційної індукованої атрофії м’язів у пацієнтів.
2. Матеріали та методи
2.1. Пацієнти
2.2. Дизайн
Пацієнтів набирали з 5 терапевтичних бригад під керівництвом незалежних слідчих у відділенні. Їх позначали номерами випадків і випадковим чином розподіляли по групам кленбутеролу або плацебо. Коди зберігалися окремо. На це посилався організатор лише в кінці дослідження або коли сталася важка несприятлива подія. Ні члени терапевтичної групи, ні пацієнти не знали, до якої групи був призначений пацієнт. Співробітники обстеження ЕМГ та обробник/оцінювач зразків біопсії були замасковані від розподілу лікування. Кленбутерол був сформульований як 60 μг/10 мл у закупорених скляних пробірках фармацевтами. Всього було виготовлено 20 000 пробірок кленбутеролу або плацебо відповідно. Стабільність полиці при 4 ° C тестували, щоб гарантувати сталість активного фармакологічного інгредієнта протягом усього періоду дослідження. Кожному пацієнтові виписували 200 пробірок кленбутеролу або плацебо і просили приймати ліки всередину 60 μг двічі на день протягом 3 місяців (
2.3. Загальні лабораторні оцінки
Перед випробуванням кожного пацієнта приймали та проводили набір лабораторних обстежень, включаючи електрокардіограму з 12 відведеннями, рентген грудної клітки, тест легеневої функції та кілька досліджень функції печінки. Також реєстрували азот сечовини крові, креатинін, час кровотечі, протромбіновий час, глюкозу, кальцій, фосфор, електроліти та загальний аналіз крові з диференціалами. До кінця випробування всі пацієнти повторили вищезазначені обстеження незалежно від їх груп.
2.4. ЕМГ-обстеження
2.5. М'язова біопсія
Всім 71 пацієнтам під час операцій з відновлення нервів безпосередньо перед початком дослідження проводили біопсію м’язів у середині біцепса плечової кістки. Зразки біопсії покривали тальком і заморожували в замороженому ізопентані, попередньо охолодженому в рідкому азоті. 10 μСвіжі зрізи кріостату товщиною м виготовляли на мікротомі кріостата при −20 ° C і встановлювали на предметних стеклах. На кожній пробі проводили фарбування міофібрилярної аденозинтрифосфатази при рН 4,6 або 9,4, щоб показати типи клітковини [22]. Площі перерізу волокна вимірювали приблизно на 300 волокнах з трьох різних полів огляду за допомогою обчислюваної системи аналізу зображень; середнє значення було розраховано для кожного типу волокна в кожній пробі. До кінця випробування, якщо ЕМГ та фізичні обстеження не виявили ознак реіннервації плечового м’яза біцепса, пацієнтів з обох груп просили повторно проводити біопсію біцепса плечового суглоба, якщо пацієнти повністю відповідали інструкціям щодо дослідження. Зразки м’язів обробляли, як і раніше.
2.6. Статистичний аналіз
Вся інформація про пацієнта та обстеження були введені в програмне забезпечення SPSS. Зміни амплітуд потенціалу фібриляції та площ поперечного перерізу протягом дослідного періоду у кожного пацієнта використовували для статистичного аналізу.
було прийнято як статистичне значення.
3. Результати
3.1. Характеристика досліджуваних
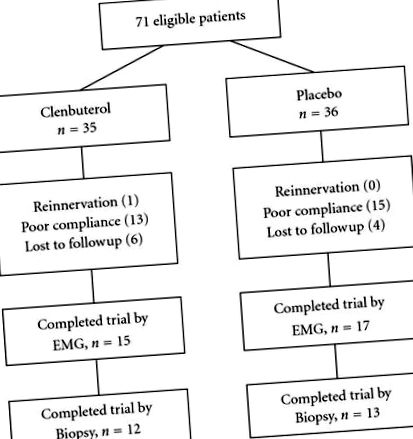
35 пацієнтів було рандомізовано у групу кленбутеролу, а 36 пацієнтів було розподілено у групу плацебо. Погана відповідність (відсутність прийому ліків за призначенням та затримка подальшого візиту) та втрата до подальшого спостереження становили 19 випадків у групі, яка отримувала кленбутерал або плацебо, відповідно. У одного пацієнта групи кленбутеролу спостерігалися ознаки реіннервації плечового м’яза біцепса (М2) через 3 місяці після перенесення діафрагмального нерва. Це було визначено за допомогою фізичних та ЕМГ-обстежень. 15 пацієнтів у кленбутеральній групі та 17 пацієнтів у групі плацебо повністю підпорядковувались рекомендаціям 3-місячного дослідження, не маючи ознак реіннервації плечового м’яза біцепса (рис. 1). Серед них 12 пацієнтів у групі кленбутеролу та 13 пацієнтів у групі плацебо приймали повторні біопсії м’язів. Пацієнтами були переважно молоді люди, які страждали від мотоциклетних аварій чи інших травм. Істотних відмінностей у віці між двома групами лікування не було. Час денервації до зарахування до пробного періоду становив близько 5 місяців - період не суттєво відрізнявся між групами (табл. 1). Усі пацієнти приймали подібні хірургічні процедури та звичайні додаткові методи лікування. Ці ключові характеристики зробили порівнянними пацієнтів обох груп.
3.2. Ефективність уповільнення атрофії м’язів
Денервовані м'язи виробляють спонтанні, повторювані одноволокнисті розряди, які представлені у вигляді потенцій фібриляції та виявляються за допомогою електроміографії. Амплітуди потенціалів фібриляції добре корелюють із розмірами м’язових волокон [20, 21]. Пацієнти, які отримували кленбутерол, мали середнє зниження на 57 μV в амплітудах потенціалів фібриляції, тоді як пацієнти, які приймали плацебо, мали в 4 рази більше зменшення за той самий проміжок часу (таблиця 2, малюнок 2).
У цьому дослідженні денервовані м’язові волокна з часом атрофувались, а волокна I типу мали менше зменшення площ поперечного перерізу, ніж тип II, незалежно від методів лікування, подібно до результатів, про які повідомлялося в інших роботах [20]. Зменшення площ поперечного перерізу у волокнах I та II склало 413 та 512 μм 2, у пацієнтів, які отримували кленбутерол. Однак ці зменшення розміру клітковини відповідно становили 66% та 60% у пацієнтів, які отримували плацебо (Таблиця 2, Малюнок 3).
3.3. Моніторинг несприятливих подій
З усіх пацієнтів лише один пацієнт відчував минущу напругу м’язів через 2 дні після введення кленбутеролу. Ніякого спеціального втручання не проводилось, крім спостереження та подальшого спостереження; дискомфорт зник після відволікання уваги на півдня. Електрокардіограма (ЕКГ) одного пацієнта зафіксувала новоутворення синусової аритмії та брадикардії через 3 місяці прийому кленбутеролу. У нього не було скарг на дискомфорт.
Шість пацієнтів у групі кленбутеролу мали аномалії ЕКГ перед зарахуванням, а саме: синусова аритмія (2 випадки), синусова брадикардія (1 випадок), неповний блок гілок правого пучка (1 випадок), висока шлуночкова напруга (1 випадок) та обертання проти годинникової стрілки серця (1 випадок). Усі вони не мали відповідних симптомів і не потребували лікування за консультацією з кардіологами. Лікування кленбутеролом протягом 3 місяців не змінило їх присутність ЕКГ.
До кінця дослідження у семи пацієнтів групи плацебо зафіксували незначні відхилення в ЕКГ (4 випадки), глюкози (2 випадки) та креатиніну (1 випадок). Не було відхилень у роботі легенів, функції печінки, часу кровотечі, протромбінового часу, електролітів або загального аналізу крові. Жодних скарг на тремтіння м’язів, тахікардію, запаморочення, зміни апетиту чи діарею протягом періоду випробування не надходило в жодній групі.
4. Обговорення
У цьому дослідженні ми змогли набрати спеціальну когорту пацієнтів років двадцяти. Це допомогло мінімізувати наслідки старіння на атрофію м’язів та усунути цей потенційно незрозумілий фактор у дослідженні, оскільки спонтанна денервація виникає зі старінням [23, 24]. Усі пацієнти мали травматичні пошкодження плечового сплетення з однаковими періодами поранення. Розміри м’язових волокон зменшуються з часом протягом першого року [20]. У цьому дослідженні пацієнтів спостерігали переважно з третього по восьмий місяць, період швидкої атрофії. Це часове вікно могло сприяти розкриттю ефективності кленбутеролу. Крім того, у всіх пацієнтів досліджували лише один ідентичний м’яз з повною денервацією, усуваючи таким чином різницю в компонентах м’язових волокон, супутню вивченню різних або частково іннервованих м’язів. Такі подібності зробили дві групи порівнянними. Велика кількість пацієнтів спричинена головним чином нещасними випадками на мотоциклах та будівництві через перехід від економічної модернізації в Китаї.
Це перше клінічне дослідження, яке показує, що кленбутерол в 120 μг/добу, ослаблена денерваційна атрофія м’язів у людини. Повідомляється, що кленбутерол, з додатковими дозами від 120 до 720 μг/день протягом 12 тижнів, збільшує масу і силу здорових скелетних м’язів у людини [13, 14]. Дослідження на тваринах показують, що денервовані скелетні м’язи в 20 разів чутливіші до кленбутеролу, ніж здорові м’язи та серце [25]. Тому 120 μВважається, що г/день кленбутеролу є досить високою дозою для знеструмлених м’язів пацієнтів. У цьому дослідженні для оцінки ефективності використовували зміни розмірів клітковини та потенцій фібриляції, допомагаючи уникнути незрозумілих факторів, що виникають внаслідок коливань базальних рівнів між особами. Отже, здається, що менше пацієнтів повинні були дійти висновку, ніж кількість, необхідна для дослідження, обмеженого лише порівнянням кінцевих точок.
У дослідженнях на тваринах та великій популяції амплітуди потенціалу фібриляції відображають розміри волокон денервованих м’язів [20, 21, 26]. Було зазначено, що лікування кленбутеролом полегшило зменшення амплітуд потенціалу фібриляції на 300%, тоді як атрофія розмірів волокон уповільнена лише на 66% або 60% у волокнах типу I або II відповідно. Ця розбіжність може бути пов’язана з тим, що перевірялися різні м’язові волокна, особливо оскільки розміри м’язових волокон суттєво різняться навіть в одному окремому зразку біопсії денервованого м’яза (рис. 3). У цьому дослідженні були проаналізовані лише найбільші амплітуди потенціалу фібриляції, які, ймовірно, походять від великих м’язових волокон. Біопсії, як правило, збирали невеликий пучок м’язових волокон, що відображає загальний стан атрофії м’язів і тому повинен служити золотим стандартом. Однак потенціали фібриляції здаються більш чутливими при виявленні ефективності терапевтичних засобів, які, отже, можуть бути використані як проміжний сурогатний маркер для майбутніх досліджень.
Реіннервація м’язових волокон, наприклад, шляхом регенерації аксонів після хірургічного ремонту, часто зупиняє атрофію м’язів і відновлює функції м’язів [27]. Розуміючи це, ми вилучили пацієнта з частковою реіннервацією плечового м’яза двоголового м’яза з аналізу атрофії м’язів, щоб уникнути втручання в дію препарату. Оскільки відстань регенерації нерва варіюється у пацієнтів з різною довжиною кінцівок, ми не змогли визначити, чи був випадок реіннервації наслідком лікування кленбутеролом. Хоча нещодавні дослідження на тваринах показують, що кленбутерол сприяє регенерації периферичних нервів і запобігає втраті нейронів при патологічних станах за допомогою регулюючого фактора росту нервів, основного фактора росту фібробластів та трансформуючого фактора росту.-β1 [5, 28, 29]. Ми не могли зробити висновок, чи сприяє кленбутерол регенерації нервів, враховуючи короткий період спостереження. Щоб вибухнути це, майбутні дослідження можуть розшарувати пацієнтів на вимогливу тривалість регенерації та подовження часу лікування та спостереження.
Скелетні м’язи містять усі три β-підтипи адренорецепторів (β1, β2 і β3), приблизно в 10 разів більша частка βІзоформа 2-адренорецепторів, ніж β1 або β3 рецептора [30, 31]. Експресія рецепторів підтипу залишається перевірятись в умовах денервації в наступних дослідженнях. І навпаки, серцевий м’яз містить приблизно вдвічі більше β1-адренорецептори, ніж β2 [1]. Це формує теоретичну основу для регулювання доз β2 агоністи впливають на скелет, а не на м’язи міокарда. Дійсно, належні дози β2 агоністи, такі як кленбутерол, розділяють вплив на різні типи м’язів у пацієнтів [9–11]. Серед відомих β2 агоністи, кленбутерол, мабуть, має найбезпечніший серцевий профіль. Для детальної розробки кленбутерол дають по 1000 μг/кг/день, не викликав гіпертрофії міокарда у щурів, а гіпертрофію скелетних м’язів [32]. Хоча надзвичайно висока доза кленбутеролу (2000 μг/кг/добу) у тварин може спричинити серцеву гіпертрофію, яка досі є фізіологічною за своїми функціями, структурою та експресією генів, і в кінцевому підсумку вона не має патологічних змін [8, 17, 33]. Послідовно, кленбутерол (до 720 μг/добу) сприяє одужанню серця у пацієнтів з атрофією розвантажувального лівого шлуночка [12–14].
Фізіологічна доза кленбутеролу у щурів, 10 μг/кг/добу, ослаблена денервована атрофія м’язів, не впливаючи на серце та не спричиняючи загибелі міоцитів [25, 34]. Ця доза була розрахована на основі метаболічної маси тіла, яка становить 10 μг/кг/день у щурів еквівалентно 1 μг/кг/добу для людини - доза, безпечно застосовувана при лікуванні астми [25, 35]. Доза в поточному дослідженні становила 120 μг/день (
2 μг/кг/добу для людини вагою 60 кг). Він добре переносився і не асоціювався з явним дискомфортом, за винятком одного пацієнта з тимчасовою нервозністю. Синусова брадикардія, що повторюється після випробування на кленбутерол, здавалася, не має значення для активації β1/2 агоніста, що зазвичай призводить до тахікардії. Більше того, кленбутерол у сучасній дозі не посилював раніше існуючих незначних відхилень ЕКГ. Це узгоджується з попередніми повідомленнями про те, що вплив кленбутеролу на серце можна спостерігати в дозі до 2100 μг/день у комбінованій терапії для пацієнтів, які використовують допоміжний пристрій лівого шлуночка. Навіть у цих дозах важких побічних ефектів не спостерігалося, окрім тремтіння та м’язових судом [12, 13]. У нашому дослідженні після 3-місячного прийому кленбутеролу не було виявлено негативних наслідків для печінки, нирок, легенів або системи кровотворення.
Це пілотне одноцентрове дослідження мало за масштабами. Ефективність була б більш очевидною у більшої групи пацієнтів, або з поступовим збільшенням доз кленбутеролу, або в режимі включення та відключення, щоб уникнути десенсибілізації рецепторів. Недавні дослідження на тваринах також показують, що кленбутерол є нейропротекторним і сприяє регенерації аксонів [5, 28, 29]. Таким чином, у поєднанні зі своєю антиатрофічною функцією, кленбутерол та його вид справді представляють перспективні та безпечні засоби для протидії пошкодженням нервів.
Список літератури
- Фаза III, плацебо-контрольоване, рандомізоване, подвійне сліпе дослідження таблетованої терапевтичної вакцини проти туберкульозу
- РАНДОМІЗОВАНЕ ДВОЙНОСЛІПЕ КОНТРОЛЬОВАНЕ ДОСЛІДЖЕННЯ ЛЕПТИНОВОГО ДОСЛІДЖЕННЯ ШЛУНОВОГО ОБХОДУ
- Рандомізоване випробування Tapas Acupressure Technique® для обґрунтування та вивчення методів зниження ваги
- Пілотне рандомізоване контрольоване випробування на лікування терпимості до лиха щодо турботи про вагу при курінні
- Плацебо-контрольоване рандомізоване дослідження з ліраглутидом на кінцевих точках магнітного резонансу у людей