Тотальна резекція шлунка
Загальна резекція шлунка зменшує ГРЛ у плазмі крові на 65%, що вказує на відносний внесок позашлункових ділянок виробництва ГРЛ у загальний рівень циркуляції крові.
Пов’язані терміни:
- Дванадцятипала кишка
- Гастректомія
- Новоутворення
- Гастрінома
- Венозна виразка
- Кобаламін
- Рак шлунку
- Часткова резекція шлунка
Завантажити у форматі PDF
Про цю сторінку
Біліопанкреатична диверсія
Міні-словник термінів
Гастректомія: Часткове або повне хірургічне видалення шлунка або для лікування деяких захворювань (рак або виразкова хвороба), або для зменшення ваги (зменшення об’єму шлунка або запобігання нормальному дуоденальному транзиту їжі для створення мальабсорбції).
Шлунково-кишковий анастомоз: зв’язок між двома різними шляхами шлунково-кишкової системи для перенаправлення її вмісту.
Колецистектомія: хірургічне видалення жовчного міхура, як правило, що містить жовчні камені (холелітіоз).
Дуоденальний перемикач: нещодавнє визначення хірургічного шунтування, яке реалізує BPD, зберігаючи пілоричний сфінктер на місці.
Лапароскопія: хірургічна техніка з обмеженим доступом, яка дозволяє проводити операції через незначні розрізи живота та оптичний пристрій з метою зменшення післяопераційного болю та ускладнень та скорочення терміну перебування в лікарні.
Варіанти вирішення проблеми із затримкою спорожнення шлунка при хворобі гастроезофагеального рефлюксу
Часткова та тотальна резекція шлунка
Проміжну або тотальну резекцію шлунка проводять для рефрактерного гастропарезу, але його справжня ефективність незрозуміла. 3 Показано, що лапароскопічна субтотальна резекція шлунка може розглядатися як первинне хірургічне лікування гастропарезу, оскільки вона пов’язана із значним поліпшенням симптомів із прийнятною захворюваністю та смертністю. 24 Резекція шлунка також була оцінена при лікуванні рецидивуючої рефлюксної хвороби після фундоплікації. Дванадцять пацієнтам перенесли резекцію шлунка (майже загальну, проксимальну або загальну), а 25 реконструювали за невдалу фундоплікацію із середнім спостереженням протягом 3 років. 37 Обидві групи продемонстрували покращення показників тяжкості симптомів, але гастректомія мала вищу роздільну здатність основного симптому (89% проти 50%). Вищий рівень захворюваності та смертності був у пацієнтів із шлунково-кишкового тракту, але чотири з пацієнтів групи реіндоплікації потребували додаткової хірургічної процедури. Це свідчить про те, що резекція шлунка - це варіант повторного рефлюксу у деяких пацієнтів, особливо у тих, хто мав численні збої в минулому.
Кларк та співавт. оглянув дев'ять пацієнтів, яким була проведена резекція шлунка (загальна, майже загальна, проксимальна) на предмет постфундоплікації, що виснажує шлункову дисфункцію. 38 У пацієнтів можуть бути симптоми через недіагностований ДГЕ до фундоплікації або через дисфункцію блукаючого нерва після операції. У трьох пацієнтів були післяопераційні ускладнення. У семи пацієнтів продовжували спостерігатися симптоми, незважаючи на резекцію шлунка, а троє продовжували потребувати ентерального харчування через зонд для годування. Ці результати показують, що, хоча показано, що резекція шлунку покращує гастропарез і рецидивуючий рефлюкс окремо, його вплив на дисфункцію шлунка після фундоплікації пов'язаний з неоптимальними результатами.
Рак шлунка
Лікування та виживання
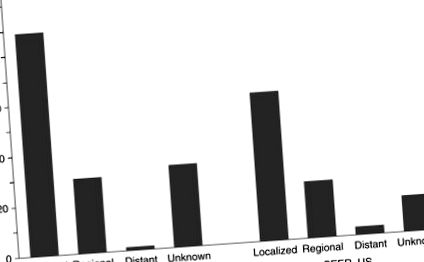
Малюнок 6. П'ятирічне відносне виживання (%) за стадією діагнозу: Осака, Японія, та SEER, США.
Від Ajiki, W., Tsukuma, H., Oshima, A., 2004. Тенденції захворюваності на рак та виживання в Осаці. В: Tajima, K., Kuroishi, T., Oshima, A. (Eds.), Статистика смертності та захворюваності від раку Японія та світ - 2004. Монографія Ганна про дослідження раку № 51, с. 137–163; Базель: Каргер; Національний інститут раку, 2007. Спостереження, епідеміологія та кінцеві результати. http://www.seer.cancer.gov/ (дата доступу: листопад 2007 р.).
Виживання раку, як правило, гірше у пацієнтів із низьким соціально-економічним статусом, ніж у пацієнтів з вищим статусом, а також у чорношкірих у порівнянні з білими в США. Однак такої різниці не видно для виживання раку шлунка (Coleman et al., 2004).
Гастректомія з реконструкцією
Еймі М. Краго, доктор медичних наук,. Стівен Р.Т. Еванс доктор медицини, у хірургічних підводних комах, 2009
Оголення та ізоляція шлунково-стравохідного з’єднання та лівих шлункових судин із перетином стравоходу
Під час проксимальної або тотальної резекції шлунка розсічення шлунково-печінкової зв’язки (менший сальник) дозволяє мобілізувати меншу кривушку шлунка. Ліву трикутну зв’язку також можна розрізати, щоб забезпечити кращий вплив стравохідного перерви. Оскільки шлунок втягується вище і праворуч від пацієнта, хірург може візуалізувати ліву шлункову артерію, яка потрапляє в шлунок безпосередньо дистально від шлунково-стравохідного з’єднання (рис. 20-4). Ускладнення, що виникають під час цієї частини процедури, включають пошкодження печінкових вен (під час розрізу лівої трикутної зв’язки), пошкодження заміненої лівої печінкової артерії (під час перетину гепатогастральної зв’язки), пневмоторакс та перфорацію стравоходу. Ці ускладнення вже були розглянуті в Розділі III, Глава 17, Лапароскопічна фундоплікація Ніссена. При тотальній резекції шлунка розтин шлунково-стравохідного з’єднання супроводжується зшиванням стравоходу. Щоб запобігти втягненню мобілізованого стравоходу в грудну клітку, накладіть шовні мітки на дистальний кінець стравоходу перед трансекцією.
Молекулярна біологія кадгеринів
2.1.5.2 Мікроскопія
Повне картографування загальних показників шлунково-кишкового тракту з безсимптомних носіїв мутацій CDH1 майже у всіх випадках показує мікроскопічні, як правило, множинні, вогнища внутрішньослизової (T1a) клітини з печаткою та дифузною клітиною. 2,21 Окремі вогнища внутрішньослизової (T1a) клітини з печаткою (дифузна) карцинома невеликі, коливаються від 0,1 до 10 мм (рис. 15.3 A), і може бути уражена кожна область слизової шлунка.
Малюнок 15.3. Мікроскопічні особливості HDGC: (А) Інвазивний осередок внутрішньослизового клітинного печінково-клітинного (дифузного) раку T1a (початкове збільшення 400 ×). (B) Печінково-кільцева клітинна карцинома in situ (початкове збільшення 400 ×). (C) Пагетоїдне розповсюдження клітин з печаткою (оригінальне збільшення 400 ×).
У профілактичних шлунково-кишкових шляхах як попередники інвазивного раку були ідентифіковані два різні типи уражень: (i) клітинний карцинома сигнального кільця in situ (SRCC), що відповідає наявності клітин сигнального кільця в базальній мембрані, як правило, з гіперхроматичними та деполяризованими ядра (рис. 15.3 Б) та (іі) пагетоїдне поширення клітин-печаткових клітин нижче збереженого епітелію залоз/фовеол (рис. 15.3 С). Показано, що імуноекспресія Е-кадгерину знижена або відсутня при ранніх інвазивних карциномах шлунка (T1a), на відміну від нормальної мембранозної експресії в сусідній неопластичній слизовій. Однак слід пам’ятати, що Е-кадгерин може експресуватись на клітинній мембрані новоутворених клітин (зі зниженою інтенсивністю та/або пунктиром), а також у цитоплазмі. 6
Рак шлунку
Проміжна сума проти тотальної гастректомії
Перше рандомізоване проспективне дослідження, що порівнює проміжні підсумки із загальною шлунковою мозковою хворобою для дистального раку шлунка, було повідомлено Гузі та його колегами. 30 Обидві групи мали однакову захворюваність (33%), смертність (1,3% проти 3,2% відповідно) та 5-річне виживання (48%). Отже, хоча планова тотальна резекція шлунка може бути виконана безпечно, субтотальна та загальна шлунково-мозкова операція дають однакові довгострокові результати у пацієнтів з карциномами дистального відділу шлунка. Більшість хірургів Сполучених Штатів рекомендують субтотальну резекцію шлунка за умови, що можна досягти негативних меж та адекватної лімфаденектомії. Правильна постановка лімфовузлів вимагає обстеження від 10 до 15 вузлів. 31 Негативні краї зазвичай вимагають перерізу дистально в дванадцятипалої кишці та принаймні на 6 см проксимальніше пальпується пухлини. Поля повинні бути підтверджені гістопатологією.
ERCP в хірургічно зміненій анатомії
Саймон К. Ло, у ERCP, 2008
Тотальна резекція шлунка
Зазвичай, що робиться для лікування раку шлунка, повна гастректомія призводить до створення назовні езофагоєюностомії. Один просвіт езофагоєюностомії - це сліпий кінець, тоді як інший - еферентна порожнина кінцівки (рис. 24.16). На короткій відстані від цієї кінцівки проводиться еюноеєюностомія в сторону або вбік для прийому вмісту підшлункової залози та жовчних шляхів. Подібно до гастректомії Roux-en-Y, ендоскоп повинен потрапити в аферентну кінцівку і пройти через проксимальну товсту кишку і більшу частину дванадцятипалої кишки. Але на відміну від часткової резекції шлунка Ру-ен-Y, дуоденоскоп насправді може регулярніше досягати головного сосочка. Після того, як основний сосочок ідентифікується з дуоденоскопом, підхід до канюляції та терапії ERCP досить схожий на підхід до анатомії Білльта II. Але якщо дуоденоскоп занадто короткий, щоб досягти низхідної дванадцятипалої кишки, тоді слід використовувати довгий ендоскоп, що оглядає кінець. У цьому випадку проблема полягає в канюлюванні та лікуванні процесів хвороби без переваг ліфта та можливості бокового огляду.
ERCP в хірургічно зміненій анатомії
Тотальна гастректомія
Зазвичай проводиться при раку шлунка або післяопераційних ускладненнях, тотальна резекція шлунка веде до наскрізної езофагоєюностомії. Один просвіт езофагоеюностомії - це глухий кінець, тоді як інший - це кішка товстої кишки (рис. 31.16). Дистальна дистанція на короткій відстані - це єюноеєюностомія з боку на бік або з боку на бік для прийому вмісту підшлункової залози та жовчних шляхів. Подібно до гастректомії Roux-en-Y, пероральний ендоскоп повинен потрапити в проксимальну товсту кишку перед тим, як прибути до дванадцятипалої кишки. На відміну від часткової гастректомії Ру-ен-Y, дуоденоскоп насправді може дійти до головного сосочка через більш прямий і коротший верхній шлях ШКТ. Після того, як основний сосочок ідентифікується з дуоденоскопом, підхід до канюляції та терапії ERCP є таким, як для анатомії Білльта II. Коли дуоденоскоп не може домовитись про проходження еюноеєюностомії або занадто короткий, щоб дійти до низхідної дванадцятипалої кишки, необхідно використовувати довгий кінцевий оглядовий ендоскоп. Знову ж таки, проблема полягає в канюлюванні та лікуванні процесів хвороби без переваг ліфта та можливості бокового огляду. У цій ситуації застосовуються ті самі методи, що застосовуються при резекції шлунка Ру-ен-Y.
Мегалобластна анемія
Дефіцит вітаміну В12
Профілактика
В умовах, при яких існує ризик розвитку дефіциту вітаміну В12 (наприклад, тотальна резекція шлунка, резекція клубової кишки), слід призначити профілактичний вітамін В12.
Активне лікування
Після точного встановлення діагнозу для початку терапії, а також добавок калію можна використовувати кілька добових доз від 25 до 100 мкг ціанокобаламіну або гідроксикобаламіну. * В якості альтернативи, враховуючи здатність організму зберігати вітамін В12 протягом тривалих періодів, підтримуючу терапію можна розпочинати щомісячними внутрішньом’язовими ін’єкціями в дозах від 200 до 1000 мкг ціанокобаламіну або гідроксикобаламіну. Більшість випадків дефіциту вітаміну В12 вимагають лікування протягом усього життя.
Пацієнти з дефектами, що впливають на кишкову абсорбцію вітаміну В12 (аномалії ІФ або поглинання клубової кишки), реагуватимуть на 100 мкг В12, що вводяться підшкірно щомісяця. Це повністю обходить дефектний крок.
Пацієнти з повним дефіцитом ТС II реагують лише на велику кількість вітаміну В12, а рівень кобаламіну в сироватці крові повинен бути дуже високим. Для підтримки адекватного контролю необхідні дози 1000 мкг в/м два-три рази на тиждень.
Пацієнти з метилмалоновою ацидурією з вадами синтезу коферментів кобаламіну, ймовірно, отримають користь від масивних доз вітаміну В12. Цим дітям може знадобитися 1-2 мг вітаміну В12 парентерально щодня. Однак не всім пацієнтам цієї групи корисний вітамін В12. Можливо, внутрішньоутробно лікувати пацієнтів, що реагують на вітамін В12. Вроджена метилмалонова ацидурія була діагностована ще внутрішньоутробно шляхом вимірювання метилмалоната в навколоплідних водах або материнській сечі.
При мегалобластній анемії, що реагує на вітамін В12, ретикулоцити починають збільшуватися на третій-четвертий день, підніматися до максимуму на шостий-восьмий день і поступово падати до норми приблизно на двадцятий день. Висота кількості ретикулоцитів обернено пропорційна ступеню анемії. Початок зміни кісткового мозку від мегалобластичних до нормобластичних клітин очевидний протягом 6 годин і завершується за 72 години. Неврологічно рівень пильності та чуйності покращується протягом 48 годин, а затримки розвитку можуть наздогнати через кілька місяців у маленьких немовлят. Часто трапляються постійні неврологічні наслідки. Швидкі гематологічні відповіді також отримуються із застосуванням пероральної фолієвої кислоти, але вона протипоказана, оскільки вона не впливає на неврологічні прояви і може спричинити або прискорити їх розвиток.
- Вегетаріанська дієта - огляд тем ScienceDirect
- Тубулопатія - огляд тем ScienceDirect
- Матка Synechia - огляд тем ScienceDirect
- Ureaplasma urealyticum - огляд тем ScienceDirect
- Незвичне ураження молочної залози, що імітує рак Діабетична мастопатія - ScienceDirect