Персоналізоване харчування шляхом прогнозування глікемічних реакцій: факт чи фантазія?
Предмети
Зееві та ін. 1 роблю висновок про високу міжособистісну мінливість постпрандіальних глікемічних реакцій (PPGR), що особисті та мікробіомічні особливості дозволяють точно прогнозувати відповідь глюкози, що перевершує загальну практику, і що короткочасні персоналізовані дієтичні втручання успішно знижують рівень глюкози після їжі. Це, мабуть, свідчить про те, що нам потрібно викинути все, що ми думали, що знали про дієтичні втручання для покращення глікемічного контролю, оскільки це стосується не всіх. Однак складна методологія, величезна кількість зібраних даних та складні цифри (деякі мають> 20 панелей) приховують важливі недоліки в обґрунтуванні дослідження, а також у поданні та інтерпретації результатів, які підривають викладені висновки.
Неправильне обґрунтування
У Вступі зазначено, що «. для досягнення нормального рівня глюкози необхідно зробити вибір їжі, який спричиняє нормальну глікемічну реакцію після їжі… ». Визначення поняття "нормальний" PPGR незрозуміле. Тим не менш, людина з гіперглікемією натще не може мати нормальний PPGR незалежно від того, що вони їдять, і дієта, яка гостро викликає низький PPGR, не обов'язково сприятиме низькому PPGR в довгостроковій перспективі. Автори стверджують, що не існує методу прогнозування PPGR і що глікемічний індекс (ГІ) має обмежену застосовність при оцінці PPGR, спричиненого "реальними стравами, що складаються з довільних комбінацій їжі та різних кількостей". Однак на підтвердження цього вони цитують лише одну статтю, яка не вивчала "страви в реальному житті, що складаються з довільних комбінацій їжі та різних кількостей", і висновки якої ми спростували. 2 Останні дані свідчать про те, що можна прогнозувати PPGR, наприклад, ми показали, що передбачались окремі додаткові ділянки під кривою глюкозної реакції (iAUC), які викликають самостійно підібрані страви для сніданку, спожиті 57 дорослими з ожирінням, страждаючим ожирінням,р= 0,748) за вмістом шлунково-кишкового тракту та вмісту вуглеводів у споживаній їжі та iAUC кожного учасника після прийому 75 г пероральної глюкози. 3
Чи демонструють результати високі варіації між індивідуальними показниками відносної глікемічної відповіді?
Суб'єкти двічі споживали 50 г вуглеводів з глюкози (G), хліба (B) або хліба плюс 30 г вершкового масла (BB) та Zeevi та ін. розраховували iAUC протягом 2 год із використанням постійного моніторингу глюкози (CGM). Очевидно, що отримані iAUCs дуже мінливі; питання полягає в тому, чи обумовлена ця варіація внутрішньо- чи міжіндивідуальною варіацією. Якщо перші, то в середньому (з урахуванням достатньої кількості копій) PPGR різних осіб реагують аналогічно на одне і те ж вживання їжі; якщо останні - ні. Зееві та ін. стверджують, що їх результати демонструють міжособистісні варіації відносної реакції, засновані на фактах, що різні прийоми їжі викликали найвищу глікемічну реакцію у різних людей і що існував великий діапазон нормалізованих глікемічних реакцій.
На підставі їх значень GI, як очікується, B спричинить iAUC на 29% менше, ніж G, BB
25% менше, ніж В у нормальних суб'єктів, 6, 7 і, отже, ВВ
За оцінками, на 47% менше, ніж G. Індивідуальна варіація iAUC, виміряна за допомогою CGM, становить
45%. 8 Коли виражається відносно G, індивідуальні відмінності в iAUC між G та B (наприклад, Gх - Бх для предмета х), як правило, розподіляються із середнім значенням 29%, і с.д. з s (в цьому випадку s= 45%/√2≈32%, оскільки кожен досліджуваний двічі тестував B та G). Площа під нормальною кривою від мінус нескінченності до 0 представляє пропорційні різниці Gх). З s.d.d. з 32%, можна було б очікувати, що B> G у 26% випробовуваних, BB> G у 15% випробовуваних та BB> B у 30% випробовуваних. На основі малюнка 2г, Зееві та ін. 1 виявив, що B> G в
40% випробовуваних, BB> G в
30%, значення схожі на ті, що очікуються випадково. Дещо більше випробовуваних мали B> G і BB> G, ніж очікувалося, і це можна було б пояснити, якби метод Зееві та ін. використовуваний для обчислення AUC не був методом, що застосовувався для ГІ, що малоймовірно. У міжлабораторному дослідженні протокол передбачав, що iAUC слід обчислювати, використовуючи метод Zeevi та ін. претензія на використання; 9, проте> 50% із 28 залучених лабораторій повідомили про невірні значення iAUC. 10 Розрахунок чистого приростового AUC дає вищі значення ГІ і асоціюється з дещо вищими внутрішньо-індивідуальними варіаціями; 11 це зменшило б очікувані різниці між B і G та BB і G і, таким чином, збільшило б очікувану частку різниць, де B> G та BB> G. Незважаючи на це, результати на малюнку 2г можуть бути в значній мірі, якщо не повністю, пояснені внутрішньо-індивідуальними варіаціями та не дають доказів великих між-індивідуальних коливань відносної глікемічної відповіді.
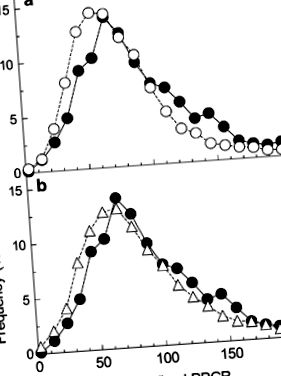
Розподіл глікемічної відповіді, спричиненої хлібом, нормалізований до глюкози, спостерігається Зееві та ін. 1 порівняно з очікуваними розподілами з міжособистісними варіаціями = 0 та високими внутрішньо індивідуальними варіаціями. Заповнені кола: розподіл повідомляє Зееві та ін. на додатковому малюнку S3I. (a) Відкриті кола: розподіл 100 × F/G розрахована з 7000 нормально розподілених випадкових значень для F із середнім значенням 71 і с.д. 22,6 і 7000 нормально розподілених випадкових значень G із середнім значенням 100 і с.д. від 31.8. (b) Відкриті трикутники: розподіл 100 × F/G розрахована з 7000 нормально розподілених випадкових значень для F із середнім значенням 75 і с.д. 26,5 і 7000 нормально розподілених випадкових значень G із середнім значенням 100 і с.д. від 35.4.
Персоналізоване прогнозування перевершує звичайну практику?
Зееві та ін. зробити висновок, що персоналізоване прогнозування перевершує звичайну практику, виходячи з того, що модель прогнозування прогнозувала iAUC краще (р= 0,70), ніж звичайна практика; однак "звичайна практика" включала лише врахування споживання вуглеводів (р= 0,38) або споживання калорій (р= 0,33). Останні є тривіальним і нерелевантним порівнянням, оскільки споживання вуглеводів або калорій не використовується для діагностики гіперглікемії. У клінічній практиці гіперглікемія діагностується шляхом вимірювання рівня глюкози натще, HbA1c та/або тесту на толерантність до глюкози на пероральний прийом 75 г. Зееві та ін. не показали, як їх модель порівнюється з цими методами, і чи варта поліпшена продуктивність, якщо така є, додаткового часу та витрат, необхідних для збору харчового щоденника, антропометрії, анкет, додаткових аналізів крові та зразків фекалій, необхідних для використання їх моделі.
Що Зееві та ін. показав, що використання їхньої моделі прогнозування для зменшення PPGR було не кращим за пораду щодо усунення тих продуктів харчування, які на основі профілів CGM викликали високий PPGR (що називається експертною); середнє зниження PPGR з використанням моделі прогнозування, 46%, було подібним до показника для консультацій на основі експертів, 44%, а індивідуальна різниця у% відповіді PPGR на модель прогнозування, sd = 28%, була дещо вищою, ніж для консультації експертів, 23%. Зееві та ін. не порівнювали свою модель із дієтичними порадами, такими як зменшення споживання вуглеводів або зменшення дієтичного шлунково-кишкового тракту, маневри, які, як відомо, були ефективними у зниженні PPGR. 12, 13 Крім того, Зееві та ін. не вказали склад їхньої “поганої” та “хорошої” дієти, чого зазвичай можна було очікувати при звітуванні про результати будь-якого втручання в їжу.
Висновок
Зееві та ін. внести деякі цікаві та нові знахідки; однак їх результати не демонструють високих міжособистісних варіацій відносних глікемічних відповідей, не показують, що їх модель перевершує сучасні методи виявлення гіперглікемії, і не показують, що персоналізовані рекомендації щодо харчування перевершують стандартні дієтичні рекомендації для лікування високих постпрандіальних реакції на глюкозу.
Список літератури
Зееві Д, Корем Т, Змора Н, Ізраїль D, Ротшильд D, Вайнбергер А та ін. Персоналізоване харчування шляхом прогнозування глікемічних реакцій. Клітинка 2015 рік; 163: 1079–1094.
Wolever TMS, Bhaskaran K. Використання глікемічного індексу для оцінки глікемічної відповіді на змішану їжу. Am J Clin Nutr 2012 р .; 95: 256–257.
Кочан AM, Wolever TMS, Chetty VT, Anand SS, Герштейн HC, Sharma AM. Глікемічний індекс прогнозує індивідуальні реакції на глюкозу після самостійно підібраних сніданків у дорослих з ожирінням з абдомінальним ожирінням, що живуть вільно. J Nutr 2012 р .; 142: 27–32.
Wolever TMS, Jenkins DJA, Vuksan V, Josse RG, Wong GS, Jenkins AL. Глікемічний індекс продуктів у окремих суб'єктів. Догляд за діабетом 1990; 13: 126–132.
Lan-Pidhainy X, Wolever TMS. Чи подібні значення глікемічного та інсулінемічного індексу вуглеводних продуктів у здорових пацієнтів із контролем, гіперінсулінемії та діабету 2 типу? Eur J Clin Nutr 2011 р .; 65: 727–734.
Оуен Б, Wolever TMS. Вплив жиру на глікемічну реакцію у нормальних суб'єктів: дослідження реакції на дозу. Nutr Res 2003; 23: 1341–1347.
Wolever TMS, Mullan YM. Цукор та жир по-різному впливають на реакції глюкози після їжі у звичайних пацієнтів із діабетом 1 типу. Nutr Metab Cardiovasc Dis 2011 р .; 21: 719–725.
Vrolix R, Mensink RP. Варіабельність глікемічної відповіді на окремі харчові продукти у здорових суб'єктів. Випробування Contemp Clin 2010 р .; 31: 5–11.
Wolever TMS, Jenkins DJA. Використання глікемічного індексу для прогнозування реакції глюкози в крові на змішане харчування. Am J Clin Nutr 1986; 43: 167–172.
Wolever TMS, Brand-Miller JC, Abernethy J, Astrup A, Atkinson F, Axelsen M та ін. Вимірювання глікемічного індексу харчових продуктів: міжлабораторне дослідження. Am J Clin Nutr 2008; 87: S247 – S257.
Wolever TMS. Вплив графіка взяття крові та методу обчислення площі під кривою на достовірність та точність значень глікемічного індексу. Br J Nutr 2004; 91: 295–300.
Рейнольдс RC, Stockmann KS, Atkinson FS, Denyer GS, Brand-Miller JC. Вплив глікемічного індексу вуглеводів на денні (10 год) профілі глюкози, інсуліну, холецистокініну та греліну у плазмі крові. Eur J Clin Nutr 2009; 63: 872–878.
McMillan-Price J, Petocz P, Atkinson F, O'Neill K, Samman S, Steinbeck K та ін. Порівняння 4 дієт з різним глікемічним навантаженням на втрату ваги та зменшення серцево-судинного ризику у людей із надмірною вагою та ожирінням молодих людей: рандомізоване контрольоване дослідження. Arch Intern Med 2006; 166: 1466–1475.
- Звички, пов’язані з харчуванням, грецьких підлітків Європейський журнал клінічного харчування
- Ожиріння як вітрина для трансдисциплінарних досліджень Європейський журнал клінічного харчування
- Навчання харчуванню в школах переживає та викликає проблеми Європейський журнал клінічного харчування
- Важка цинга - занижена хвороба Європейський журнал клінічного харчування
- Відповідь на дієти з вищим та нижчим вмістом білка Європейський журнал клінічного харчування