Однорічний аналіз безпеки випробування COMPARE-AMI: Порівняння внутрішньокоронарної ін’єкції CD133 + стовбурових клітин кісткового мозку та плацебо у пацієнтів після гострого інфаркту міокарда та дисфункції лівого шлуночка
Самер Мансур
1 Кардіологічний відділ, Департамент медичної медицини, Центр лікарні університету Монреаля (CHUM), 3840, Rue Saint Urbain, Монреаль, Квебек, Канада H2W 1T8
2 Axe Cardio-Métabolique, Center de Recherche du CHUM (CRCHUM), Монреаль, Квебек, Канада H2W 1T7
Денис-Клод Рой
3 Département d'Hematologie, Hôpital Maisonneuve-Rosemont (HMR), Монреаль, Квебек, Канада H1T 2M4
Вінсент Бушар
4 Медичний факультет, Університет Монреаля, Монреаль, Квебек, Канада H3C 3J7
Луї Матьє Стівенс
2 Axe Cardio-Métabolique, Center de Recherche du CHUM (CRCHUM), Монреаль, Квебек, Канада H2W 1T7
5 Відділення хірургічного лікування Кардіака, Департамент хірургічного лікування, Центр лікарні університету Монреаля (CHUM), Монреаль, Квебек, Канада H2W 1T8
Франсуа Гобейл
1 Кардіологічний відділ, Департамент медицини, Центр лікарні університету Монреаля (CHUM), 3840, Rue Saint Urbain, Монреаль, Квебек, Канада H2W 1T8
Ален Рівард
1 Кардіологічний відділ, Департамент медицини, Центр лікарні університету Монреаля (CHUM), 3840, Rue Saint Urbain, Монреаль, Квебек, Канада H2W 1T8
2 Axe Cardio-Métabolique, Center de Recherche du CHUM (CRCHUM), Монреаль, Квебек, Канада H2W 1T7
Гай Леклерк
1 Кардіологічний відділ, Департамент медичної медицини, Центр лікарні університету Монреаля (CHUM), 3840, Rue Saint Urbain, Монреаль, Квебек, Канада H2W 1T8
Франсуа Рівз
1 Кардіологічний відділ, Департамент медицини, Центр лікарні університету Монреаля (CHUM), 3840, Rue Saint Urbain, Монреаль, Квебек, Канада H2W 1T8
2 Axe Cardio-Métabolique, Center de Recherche du CHUM (CRCHUM), Монреаль, Квебек, Канада H2W 1T7
Ніколас Нуазе
2 Axe Cardio-Métabolique, Center de Recherche du CHUM (CRCHUM), Монреаль, Квебек, Канада H2W 1T7
5 Відділення хірургічного лікування Кардіака, Департамент хірургічного лікування, Центр лікарні університету Монреаля (CHUM), Монреаль, Квебек, Канада H2W 1T8
Анотація
Терапія стовбурових клітин кісткового мозку стала перспективним підходом для поліпшення загоєння інфарктного міокарда. Незважаючи на початковий ажіотаж, нещодавні клінічні випробування з використанням неоднорідних препаратів стовбурових клітин показали змінні та змішані результати. Виділені гемопоетичні стовбурові клітини CD133 + - це клітини-кандидати з високим потенціалом. У цьому документі ми повідомляємо про однорічний аналіз безпеки для початкових 20 пацієнтів, які були залучені до дослідження COMPARE-AMI, першого подвійного сліпого рандомізованого контрольованого дослідження, що порівнює безпеку, ефективність та функціональний ефект внутрішньокоронарної ін’єкції вибраних клітин CD133 + до плацебо після гострого інфаркту міокарда з постійною дисфункцією лівого шлуночка. За один рік не існує жодних ускладнень, пов’язаних з протоколом, таких як смерть, інфаркт міокарда, інсульт або стійка шлуночкова аритмія. Крім того, фракція викиду лівого шлуночка значно покращилася через чотири місяці порівняно з початковим рівнем і залишалася значно вищою через рік. Ці дані вказують на те, що в умовах дослідження COMPARE-AMI внутрішньокоронарне введення вибраних стовбурових клітин CD133 + є безпечним та здійсненним у пацієнтів з дисфункцією лівого шлуночка після гострого інфаркту міокарда.
1. Вступ
Незважаючи на покращення рівня виживання після інфаркту міокарда (ІМ) з недавніми медичними та хірургічними досягненнями [1], зниження серцевої діяльності, пов'язане з незворотною втратою життєздатних кардіоміоцитів, залишається основною клінічною проблемою [2]. Внутрішньокоронна ін'єкція клітин-попередників виникла як цінний терапевтичний підхід для покращення загоєння ішемічного серця. Незважаючи на використання різних експериментальних протоколів із змішаними клітинами, що показують неоднозначні результати [3], чотири недавніх мета-аналізи трансплантації стовбурових клітин кісткового мозку (BMSC) в умовах гострого ІМ довели доцільність та безпеку та продемонстрували незначний, але позитивний функціональний ефект [4–7]. Однак наразі існує невизначеність щодо того, хто із популяції BMSC є найбільш потужним у стимулюванні ангіогенезу та репарації серця. Кровотворні клітини CD133 + мають високу приживлюваність, мультипотентність та ангіогенну здатність і виявляються цінними для відновлення серця при експериментальному інфаркті міокарда [8–11].
На фазі, яку я вивчаю, Bartunek et al. тестували IC-ін'єкцію клітин CD133 + у пацієнтів після гострого ІМ та продемонстрували значне покращення функції та перфузії лівого шлуночка (ЛШ) порівняно з контролем [12]. Однак вони відзначали в оброблюваній групі збільшення коронарних подій із більшою проліферацією в стенті та більшими втратами просвіту в нестентованих сегментах інфарктної (ІЧ) артерії [13]. Слід зазначити, що ці дані були отримані в результаті ретроспективного аналізу, і в них відсутні рандомізовані контролі. Таким чином, ми розробили дослідження COMPARE-AMI, перше рандомізоване, подвійне сліпе, плацебо-контрольоване однофазне дослідження фази II, що порівнює IC ін’єкцію клітин CD133 + з плацебо при реконструкції серця у пацієнтів з гострим ІМ та стійкою дисфункцією ЛШ [ 14, 15]. Тут ми повідомляємо про однорічний аналіз безпеки перших рандомізованих пацієнтів.
2. Методи
2.1. Дизайн дослідження та цілі
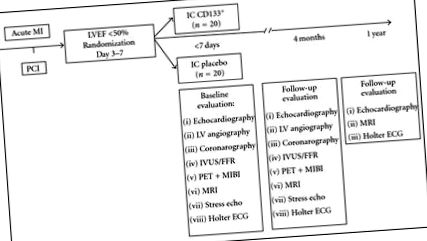
Дослідження COMPARE-AMI - це одноцентрове, рандомізоване, перспективне, подвійне сліпе, подвійне сліпе, плацебо-контрольоване клінічне випробування фази II, що досліджує доцільність, безпеку та ефективність введення ІС вибраних аутологічних CD133-збагачених гемопоетичних BMSC у порівнянні з плацебо у пацієнтів після гострого ІМ із стійким дисфункціональним міокардом, незважаючи на успішну реперфузію катетера. Блок-схема випробування докладно представлена на малюнку 1. Основною кінцевою точкою дослідження є сукупність кінцевих точок безпеки та ефективності, спрямованих на визначення змін у прогресії коронарного атеросклеротичного навантаження проксимально та дистальніше стентованого сегмента артерії винуватця через 4 місяці порівняно з вихідним рівнем та зміною фракція викиду лівого шлуночка (LVEF) через 4 місяці відносно вихідного рівня. Вторинні кінцеві точки включають появу великої несприятливої серцевої події (MACE), що визначається як смерть, ІМ, інсульт та реваскуляризація судин цілі (TVR) або поява основних аритмій, що визначаються як стійка шлуночкова аритмія або пережита раптова смерть. За пацієнтами спостерігають протягом 2 років, і дані будуть невідомі через 12 місяців після рандомізації останнього пацієнта.
Блок-схема пробного періоду COMAPRE-AMI. ІМ вказує на інфаркт міокарда, ЧКВ черезшкірне коронарне втручання, фракцію викиду лівого шлуночка ЛШФ, внутрішньокоронарний ІК, ЛШ лівого шлуночка, ВМД, внутрішньосудинне ультразвукове дослідження, дробовий резерв потоку FFR, позитронно-емісійну томографію ПЕТ, сенемібі МІБІ-технецій 99 м ЕКГ-електрокардіограма.
2.2. Вивчення населення та протоколу
Коротше кажучи, пацієнти у віці від 30 до 75 років мають право, якщо вони представили гострий ІМ з підвищенням ST, успішно компенсований за допомогою імплантації коронарного стенту і продемонстрували значну стійку дисфункцію ЛШ, визначену ЛШН ≤50%, але ≥25% на ехокардіографії, отриманій протягом 48 годин після успішної реперфузійної терапії. Письмова інформована згода отримується протягом 7 днів після початку гострого ІМ, якщо у пацієнта відсутні будь-які критерії виключення, такі як відомий попередній ІМ, кардіогенний шок, хронічна кардіоміопатія, захворювання печінки, ниркова недостатність, супутнє захворювання із тривалістю життя менше 1 рік, алкогольна або наркотична залежність, протипоказання до аспірації кісткового мозку (БМ), переливання крові за попередні 24 години, хвороба кровотворення, хронічне запальне захворювання, злоякісне новоутворення, інсульт за попередні 3 місяці або транзиторна ішемічна атака за попередні 24 години . Протокол дослідження був схвалений Health Canada (CTA 113925 та ITA 123840) та комісією з огляду інституційної етики.
Функціональна оцінка міокарда проводиться за допомогою ехокардіографії, магнітно-резонансної томографії серця (МРТ), ангіографії лівого шлуночка, ехокардіографії, одномісної фотонної комп’ютерної томографії сенемібі технецію 99 м та позитронно-емісійної томографії з [17] флуородезоксиглюкозою на початковому етапі та через 4 місяці спостереження. МРТ серця та ехокардіографія повторюються через 1 рік спостереження.
2.3. Оцінка безпеки
Для визначення безпеки ін’єкції IC введення суспензії клітин CD133 + проводять стандартні лабораторні дослідження, що включають кількість білих кров’яних клітин (WBC), С-реактивний білок (CRP), креатинкіназу (CK) та креатинкіназу м’язів та мозку (CK- Вимірювання типу MB та тропоніну Т проводили до, через 30 та 60 хвилин, 6 годин та 24 години після ін’єкцій IC. Крім того, всіх пацієнтів постійно спостерігали до виписки та проходили 24-годинний моніторинг ЕКГ на початковому рівні, через 1, 4 та 12 місяців після процедури. Крім того, кількісну коронарну ангіографію, фракційний запас потоку, отриманий за тиском (FFR), та УЗД ультразвукового дослідження проводили в ІЧ-артерії та віддаленій артерії на початковому етапі та 4 місяці спостереження.
2.4. Статистичний аналіз
Для всіх пацієнтів були зібрані вихідні демографічні та клінічні змінні. Інвазивні та неінвазивні аналізи проводили оператори, засліплені всіма клінічними та іншими функціональними даними. Дані подаються як середнє значення ± стандартне відхилення або медіана та інтерквартильний діапазон, коли це доречно. Безперервні змінні аналізували за допомогою t-критерію Стьюдента. Повністю параметризовані моделі поздовжнього змішаного ефекту були побудовані для ехокардіографічного вимірювання, включаючи коефіцієнт для кожного моменту часу на початковому рівні, 4 та 12 місяців (процедура MIXED у програмному забезпеченні SAS, версія 9.1; SAS Institute, Cary, NC). Ці моделі пояснюють кореляцію між повторними вимірами у того самого пацієнта. Для всіх аналізів, Таблиця 1. Середній вік становив 52,2 ± 8,9 року з переважанням чоловіків (90%), а винуватцеве ураження було розташоване на лівій передній низхідній артерії у 90%. Повна оклюзія була відзначена в проксимальному сегменті ІЧ-артерії в 65% випадків. Максимальні значення тропоніну Т та ККМБ становили 10,48 ± 8,34 мг/л та 341 ± 260,7 од/л відповідно, що свідчить про великі інфаркти. Усім пацієнтам була проведена успішна реперфузія зі стентуванням з використанням стента, що елююється лікарським засобом (DES) у 75%, або стента з оголеним металом (BMS) у 25% випадків. Ад'ювантна медична терапія включала аспірин, клопідогрель, β-адреноблокатори, інгібітори ангіотензинперетворюючого ферменту та статини.
Таблиця 1
Демографічні та клінічні характеристики. ІМТ вказує на індекс маси тіла, ІХС ІХС, ЧКВ черезшкірне коронарне втручання, КК креатинікіназу та КК-МБ креатинкіназу - м’язи та мозок.
| Вік (років) | 52,2 ± 8,9 |
| Чоловік (%) | 90 |
| ІМТ | 28 ± 5,7 |
| Діабет (%) | 15 |
| Гіпертонія (%) | 35 |
| Гіперліпідемія (%) | 20 |
| Куріння (%) | 70 |
| Сімейна історія канадських доларів (%) | 15 |
| Двері до повітряної кулі (хв.) | 123,6 ± 97,4 |
| PCI до ін’єкції (дні) | 6,4 ± 2,2 |
| Клас Кілліп | I: 95; II: 5 |
| Максимальний підйом ST (мм) | 11,2 ± 5,5 |
| Q-хвилі при вступі (%) | 55 |
| Пік тропоніну Т (UI/мл) | 10,48 ± 8,34 |
| Пік CK (UI/мл) | 2744 ± 2193 |
| Пік CK-MB (UI/мл) | 341 ± 260,7 |
3.2. Аналіз безпеки
Таблиця 2
Біологічні маркери після ін’єкції ІС, без змін із часом (усі Р = НС). WBC вказує на кількість білих кров'яних тілець, СРР-реактивний білок, КК-креатинікіназу та КК-МБ-креатинкіназу-м'язи та мозок.
| WBC | 8,12 ± 1,6 | 8,65 ± 1,96 | 8,92 ± 2,31 | 7,74 ± 1,94 | 7,29 ± 1,69 |
| CRP | 11,09 ± 12,16 | 10,15 ± 8,56 | 12,15 ± 12,8 | 13,18 ± 14,24 | 13,08 ± 13,96 |
| Тропонін Т | 0,83 ± 1,02 | 0,88 ± 1,07 | 0,91 ± 1,13 | 0,8 ± 0,95 | 0,66 ± 0,84 |
| CK | 167,4 ± 95,6 | 176,5 ± 99 | 204 ± 135,9 | 171,5 ± 85,3 | 160,4 ± 81,97 |
| CK-MB | 46,8 ± 22,2 | 51,33 ± 28,17 | 55,56 ± 27,58 | 72 ± 40,28 | 60,7 ± 39,90 |
Тому Бартунек та ін. провів випробування I фази [12], тестуючи IC ін'єкцію очищеного CD133 + BMSC в гостро інфікований міокард після успішного стентування артерії винуватця. Вони продемонстрували значне покращення функції ЛШ паралельно зі збільшенням перфузії та життєздатності міокарда, що свідчить про потужний ангіогенний ефект ін'єктованих клітин. Однак повідомлялося про такі загрози безпеці у групі, яка отримувала клітини: спочатку невеликий, але значний ріст СРБ, другий шлуночкові аритмії спостерігався у 4 пацієнтів, що лікувались, і третій - більший рівень рестенозу ВМС та ураження de novo знайдено. Більше того, вони підняли можливість ефекту "подібного до Януса", коли в ретроспективному аналізі вони повідомили про значне зменшення діаметрів просвіту та епікардіальної провідності ІЧ-артерії, як оцінювали за даними FFR [13], головним чином на початку порівняно з пізнім введенням IC CD133 + клітин [17], що, здається, відповідає вищому ризику прогресування атеросклерозу. Проте ці дані були отримані в результаті ретроспективного аналізу; їм не вистачає належного рандомізованого контролю та систематичного використання ультразвукової томографії для відстеження змін у судинній стінці.
На закінчення, запропонований експериментальний протокол, в якому IC аутологічні клітини CD133 + вводять після гострого ІМ, є безпечним, без будь-яких серйозних побічних явищ до одного року спостереження. Крім того, спостерігається потенційний сприятливий вплив на відновлення ЛШ включених пацієнтів. Остаточні результати будуть доступні через 1 рік після рандомізації останнього пацієнта; тим часом представлені однорічні результати безпеки виправдовують продовження випробування COMPARE-AMI. Це рандомізоване клінічне дослідження повинно допомогти підтримати терапевтичний потенціал клітин CD133 + для лікування інфрачервоного міокарда.
Подяка
Автори високо оцінюють допомогу доктора. B. Lemieux та C. Ouellette, виконуючи збір кісткового мозку. Вони вдячні Р. Дукло, Р.Н. та К.Лемаю Р.Н. за керівництво дослідженням. Автори отримали фінансову підтримку від fonds de la recherche en santé du Québec, Miltenyi Biotec, Inc. та Boston Scientific в Канаді.
- БД та автомобільна безпека - Коледж громади прибережної Кароліни
- Макдональд; s Японія проти США Порівняння, однакові предмети Різні вироби
- Вимоги до джерел живлення ПЛК та безпеки (аварійні) EEP
- Ожиріння надмірна вага та ризик алергічного риніту Мета-аналіз спостережних досліджень - Чжоу -
- Безпека пісочниці - рости здоровим