Обґрунтованість ефекту лікарського засобу на основі біопсії в модельованій дієтою індукованій миші із ожирінням мишей біопсії, підтвердженої NASH
Анотація
Передумови
Сполуки в клінічній розробці неалкогольного стеатогепатиту (NASH) покращують гістопатологію печінки на моделях ожирілих мишей із ожирінням, підтверджених біопсією, NASH. Оскільки розділ біопсії, який використовується для гістопатологічної оцінки, представляє лише об / Леп об мишей годували дієтою NASH для печінки аміліном (AMLN) протягом 16 тижнів до розшарування на групи лікування, використовуючи біопсійну оцінку рівня I колагену типу I (col1a1). Мишей лікували протягом 8 тижнів або носієм (PO, QD), ліраглутидом (0,4 мг/кг, SC, QD), елафібранором (30 mg/kg, PO, QD) або INT-767 (10 мг/кг, PO, QD). Кінцева кількісна гістологічна оцінка ліпідів печінки (фарбування гематоксилін-еозином), запалення (імуногістохімія хімії галектин-3 (IHC); gal-3) та фіброзу (IHC col1a1) проводилася на кінцевих біопсіях печінки та порівнювалась зі стереологічно відібраними серійними зрізами, що охоплювали медіальна, ліва та права бічні частки печінки.
Результати
Розподіл ліпідів та фіброзу печінки був помітно послідовним між частками, тоді як запалення демонструвало певну мінливість. Хоча INT-767 та ліраглутид значно зменшували загальну масу печінки відповідно на 20 та 48%, елафібранор, як правило, посилював гепатомегалію в Леп об / Леп об -Миші NASH. Усі три сполуки помітно знизили відносний вміст ліпідів у печінці на основі біопсії. Elafibranor та INT-767 значно знизили відносний рівень gal-3 на основі біопсії (P
Передумови
Поширеність неалкогольної жирової хвороби печінки (НАЖХП) зростає у всьому світі разом із збільшенням частоти діабету та ожиріння [1, 2]. NAFLD варіюється від доброякісної неалкогольної жирової печінки (NAFL) з простим стеатозом до не запального стану, безалкогольного стеатогепатиту (NASH) та цирозу [3,4,5], що, за оцінками, є основною причиною кінцевої стадії захворювання печінки протягом декількох років [6,7,8]. На сьогоднішній день не існує ліцензованого лікування НАСГ, однак тривають численні клінічні випробування [9]. Найбільш розвиненими є обетихолева кислота (агоніст ядерного рецептора фарнезоїду X (FXR)), елафібранор (подвійний активований проліфератором пероксисом рецептор (PPAR) -α/δ агоніст), селонсертиб (інгібітор кінази 1, що регулює сигнал апоптозу (ASK1)), і ліраглутид (аналог глюкагоноподібного пептиду-1 (GLP-1) тривалої дії) [9].
На додаток до складного завдання розробки терапевтичних засобів для НАСГ, клінічній діагностиці та подальшим спостереженням перешкоджає незадоволена потреба у надійних неінвазивних діагностичних та прогностичних інструментах [10, 11]. Розвиток NASH непередбачуваний і варіює як за ступенем тяжкості захворювання, так і за ступенем прогресування [12]. Неінвазивні процедури візуалізації, включаючи ультрасонографію, магнітно-резонансну томографію (МРТ) та магнітно-резонансну еластографію (МРЕ), показали потенціал у діагностиці НАФЛ і можуть повторюватися протягом періоду моніторингу захворювання [11]. Однак їх корисність є недостатньою через відсутність чутливості для розмежування між проміжними рівнями тяжкості фіброзу, їх обмеженою доступністю та супутніми витратами [11]. Високочутливі та прогнозуючі тести хімії крові для циркулюючих сурогатних біомаркерів пошкодження печінки досі не отримали схвалення FDA [11]. Відповідно, інвазивні та ризиковані парні біопсії печінки все ще залишаються золотим стандартом для постановки та класифікації NASH та для контролю ефективності лікарських засобів у клінічних випробуваннях [13,14,15,16,17].
Для сприяння розвитку фармацевтичної терапії надзвичайно важливими є тваринні моделі, що відображають клінічний фенотип NASH. Було розроблено кілька моделей, які, як правило, класифікуються на індуковані дієтою, хімічно індуковані або генетичні моделі (нокаут або трансгенні) [18]. Доведено, що різні обезогенні дієти західного типу сприяють розвитку фенотипу NASH у мишей, хоча ступінь тяжкості захворювання часто є слабкою [19]. Однак при дотриманні ≥26 тижнів на дієті з високим вмістом жиру, фруктози та холестерину (дієта NASH для печінки аміліном; AMLN [20, 21]), як показали миші C57BL/6J, вони розвивають печінкові патологічні ознаки NASH, включаючи стеатоз, долькове запалення та дегенерація на балонах, а також фіброз легкого та середнього ступеня [21,22,23,24,25,26]. Ці ознаки ще більше підкреслюються при лептинодефіцитному Леп об / Леп об миші [20, 25, 27, 28]. Фармакологічна ефективність метаболічних та печінкових кінцевих точок вже широко характеризується у цих моделях [20, 26, 29].
Раніше було показано, що Елафібранор, INT-767 та ліраглутид індукують різноманітні фармакодинамічні ефекти на гістопатологію печінки [20, 26, 29,30,31,32,33,34]. Ці три сполуки представляють три абсолютно різні класи препаратів із трьома різними механізмами дії [29, 35,36,37], а також відомо, що вони впливають на загальну масу печінки. Незважаючи на те, що результати, засновані на біопсіях дрібних тканин, обнадійливі, раніше жодні дослідження не застосовували стандартний стереологічний відбір проб золота для оцінки однорідності морфометрії печінки за печінками печінки, а також для оцінки достовірності оцінок біопсії печінки, щоб відобразити фармакологічно зумовлені зміни на цілі печінки миші. Це дослідження має на меті оцінити, чи ефективно відбиває кількісний аналіз зображень на основі біопсії ремоделювання цілої печінки після медикаментозного лікування, порівняно із кількісним цифровим аналізом зображень всієї печінки на основі стереології.
Методи
Тварини та експериментальна установка
Чоловік B6.V-Леп об/JRj (Леп об / Леп об ) мишей (віком 5 тижнів) отримували від JanVier (JanVier Labs, Франція), і група вміщувала по 10 тварин на клітку в контрольованому середовищі (12/12 год при темному світлі, 21 ± 2 ° C при кімнатній температурі та 50 % ± 10% вологості). Миші мали ad libitum доступ до дієти AMLN (D09100301, Research Diets, Нью-Брансвік, США) [21], що містить 40% жиру (18% нежирних речовин), 40% вуглеводів (20% фруктози) і 2% холестерину, або звичайну чау гризунів (Altromin 1324, Brogaarden, Данія), а також водопровідна вода. Мишей тримали на дієті за 16 тижнів до восьмитижневого періоду фармацевтичного втручання (див. Нижче). Протягом усього періоду лікування масу тіла вимірювали щодня. Всі поводження з тваринами, лікування та евтаназія проводились відповідно до протоколу, затвердженого Датським національним агентством із захисту експериментальних тварин з використанням міжнародно визнаних принципів догляду та використання лабораторних тварин (ліцензія № 2013-15-2934-00784, Інспекція експериментів на тваринах, Данія).
Фармакологічне втручання
Обробка тканин та морфометричний аналіз
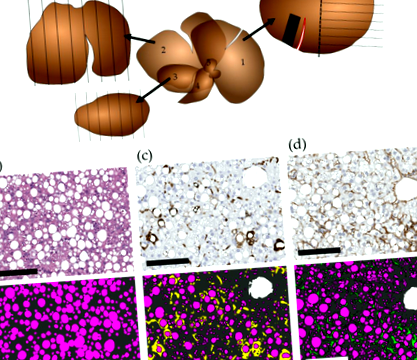
Всю печінку зважували і ділили на ліву бічну, медіальну та праву бічні частки, які потім зважували індивідуально. Згодом ліву бічну частку розділили на дві рівні частини, з яких з однієї частини отримали кінцеву біопсію прямокутної форми. Решта половини, а також медіальна та права бічні частки використовувались для стереологічних аналізів (рис. 1а-в).
Візуалізація стереологічних розрізів та морфометричний аналіз. Схематичне малювання часток печінки, що використовуються для стереології (a); ліва бічна частка (1), включаючи місце добіопсії (червоне), після біопсії (чорний квадрат) та стереологічний зріз (половина частки, позначена пунктиром), медіальна частка (2) та права бічна частка (3) ), а також хвостату частку (4) та папілярний відросток (5). Морфометричний аналіз; стеатоз (b) на зрізах, пофарбованих гематоксиліном та еозином Y, а також імуногістохімії (IHC) галектину-3 (gal-3) (c), а ланцюжка α1 колажу типу I (col1a1) (d). Рожевий призначається стеатозу, темно-сірий - тканині печінки, жовтий - позитивному забарвленню gal-3, зелений - позитивному плямі col1a1. Морфометричні оцінки проводяться за допомогою програмного забезпечення Visiomorph (Visiopharm, Hoersholm, Данія), шляхом піксельної анотації, виключаючи судини на основі розміру (білий призначається судинам), а також виключаючи позитивні плями, що оточують судини gal-3 та col1a1. Шкала шкали = 150 мкм
Статистичний аналіз
Статистичний аналіз проводили з використанням або двостороннього дисперсійного аналізу (ANOVA) з подальшим тестом Туреччини пост-hoc, або одностороннього ANOVA з пост-hoc тестом Даннета (стор
Результати
Внутрішньо- та міждолькова мінливість
Внутрішньо- та міждолькову мінливість аналізували у п’яти мишей, оброблених NASH, оскільки розрахунки потужності оцінили це як достатнє. Морфометричний аналіз ліпідів печінки виявив низьку внутрішньодольову варіабельність (CVi від 0,02 до 0,08) та дещо вищу варіабельність між частками (CV між 0,05-0,08) (рис. 2а). Біологічна мінливість між тваринами становила 43,7% від загальної дисперсії, тоді як внутрішньодольова мінливість становила лише 11,7%. Істотних відмінностей у рівні ліпідів печінки між біопсіями та окремими частками не спостерігалось (рис. 2б).
Найбільш помітні відмінності у мінливості внутрішньої частки спостерігались у морфометрії gal-3 з CVi від 0,04 до 0,47 (рис. 2в). Більше того, рівні gal-3 були значно вищими в медіальній частці порівняно з лівою та правою бічною частками, а також порівняно з рівнями gal-3 на основі біопсії (рис. 2г). Біологічна мінливість становила 8% від загальної дисперсії гал-3, тоді як мінливість у межах частки становила 67,8%.
Внутрішньодолеву мінливість для col1a1 оцінювали до 0,06-0,26 (рис. 2д). Що стосується вмісту ліпідів у печінці, то найбільшим розбіжником дисперсії col1a1 була біологічна мінливість серед мишей, що становило 52,9% від загальної дисперсії, тоді як внутрішньодольова дисперсія становила лише 14,7%. Загалом, оцінки загальних рівнів col1a1 в окремих частках були значно нижчими, ніж оцінки на основі біопсії (рис. 2f).
Вплив на масу тіла та печінки
Леп об / Леп об -Групи NASH страждали ожирінням до лікування (53 ± 1,1 г., n = 12), але показав меншу масу тіла порівняно з віковим чау-годуванням Леп об / Леп об миші, оброблені транспортним засобом (59,6 ± 0,8 г., n = 10) (рис. 3а). Лікування ліраглутидом та елафібранором поступово зменшувало масу тіла (рис. 3а), з максимальною втратою ваги приблизно на 10% порівняно з вихідним рівнем та приблизно на 20% проти дозування транспортного засобу (рис. 3б). INT-767 уповільнив швидкість набору маси тіла, але не зменшив масу тіла нижче базового рівня в Леп об / Леп об -Миші NASH (рис. 3b).
Леп об / Леп об -Миші NASH відзначали гепатомегалію порівняно з контролем, що годували чау (рис. 3c-f). Як ліраглутид, так і INT-767 значно зменшили загальну масу печінки (рис. 3в) і масу правої бічної частки (рис. 3е). Подібна картина спостерігалася для лівої бічної та медіальної часток, що досягало статистичної значущості лише для ліраглутиду (рис. 3d та e). Лікування елафібранором суттєво не впливало на вагу печінки.
Аналіз термінальної біопсії та морфометрії цілої печінки
Усі методи лікування значно знижували відносний вміст ліпідів у біопсії (рис. 4а) та у всій печінці (рис. 4б), що було найбільш вираженим для INT-767 та елафібранору. При врахуванні змін загальної ваги печінки вплив на загальну масу ліпідів був ще більш помітним незалежно від біопсії (рис. 4в) або взяття цільної печінки (рис. 4г). Це також було видно із субаналізу окремих часточок (рис. 4е-г, таблиця 1).
INT-767 та елафібранор суттєво знижували відносні рівні gal-3 у біопсії (рис. 5a) та у всій печінці (рис. 5b), тоді як ліраглутид не впливав на відносні рівні gal-3 (рис. 5a-b). Однак, якщо виражати їх у загальних значеннях, усі сполуки зменшували масу gal-3 незалежно від методу відбору проб (рис. 5c-d) та по всіх частках (рис. 5e-g, таблиця 1).
Жодне з методів лікування ефективно не зменшило відносного col1a1 на основі біопсії (рис. 6a), тоді як INT-767 зменшило відносний col1a1 у цілому в печінці (рис. 6b). Коли виражаються як загальні значення, INT-767 та ліраглутид, але не елафібранор, суттєво знижують загальний рівень печінки col1a1 незалежно від методу відбору проб, тобто біопсії- (рис. 6в) або кількісного визначення на основі стереології (рис. 6г). Тільки INT-767 суттєво зменшив масу col1a1 по всіх частках (рис. 6e-f) і надав найбільш виражений ефект зниження col1a1 серед випробуваних класів препаратів (таблиця 1). Загалом, зменшення маси col1a1 було вищим при стереологічному аналізі порівняно з аналізом на основі біопсії.
Обговорення
Це дослідження мало на меті перевірити достовірність біопсії печінки, що становить менше 1% від загальної кількості печінки, для відображення ремоделювання хвороби цілої печінки після фармацевтичного лікування у чоловіків Леп об / Леп об -Миші NASH. Порівнюючи морфометричний аналіз біоптатів зі стереологічно відібраними зрізами по всій печінці, ми демонструємо, що біопсія в цілому репрезентативна для цілого стану печінки і застосовується для доклінічної оцінки досліджень фармакологічного втручання. Однак, зокрема, ми також демонструємо, що фармакологічно обумовлений вплив на вагу печінки слід ретельно розглядати при порівнянні кінцевих точок, пов'язаних з NASH, у доклінічних дослідженнях.
В той час як вміст ліпідів у печінці демонстрував незначні зміни в межах та між частками, мінливість у межах частки була більш очевидною як для відносного рівня gal-3, так і для col1a1. Ця різниця не дивна і підкреслює необхідність брати біопсії в одній і тій же частині частки при порівнянні динаміки тканин у різних тварин або використовувати неупереджені стереологічні принципи відбору проб, що охоплюють всю печінку. Відмінності рівнів col1a1 в основному пов'язані з часткою капсули Гліссона в зрізі тканини. Капсула Гліссона [40], колагеновий шар, що покриває печінку, збільшується в товщині під час прогресування фіброзу [41, 42]. Відповідно, рівні col1a1 були помітно вищими на верхівкових частинах порівняно з ляпасами, що містять більш високе співвідношення центральних частин частки. Ця ж причина може застосовуватися до мінливості gal-3, оскільки, як відомо, gal-3, отриманий з макрофагів, пов'язаний з міофібробластами, а отже, і фіброзом [43, 44].
Нарешті, слід зазначити, що представлені тут аналізи базувались на кількісній оцінці імуногістохімії gal-3 та col1a1. Ці "панмаркери" запалення та фіброзу широко використовуються в доклінічних та клінічних дослідженнях, але, звичайно, можуть не відображати всі запалення ремоделювання позаклітинного матриксу під час розвитку NASH. Відповідно, обґрунтованість ефективності препарату на основі біопсії, представлену тут, слід розглядати обережно щодо інших маркерів.
Висновок
На закінчення ми повідомляємо, що біопсія печінки може вважатися репрезентативною для ремоделювання, що відбувається у всій печінці Леп об / Леп об -Миші NASH після фармацевтичного лікування, хоча зміни дещо відрізняються за допомогою поглибленої стереологічної оцінки всього органу, як це показано тут для ліраглутиду та INT-767 для оцінки col1a1. В недавньому дослідженні повторні біопсії печінки витягували з лівої бічної частки, медіальної правої частки та медіальної лівої частки у мишей протягом трьох місяців [54]. Незважаючи на те, що ці дані показали, що повторні біопсії печінки з різних часток є здійсненними, наші дані свідчать про те, що слід проводити постійні вимірювання на основі біопсії в одній і тій же частці. Нарешті, ми підкреслюємо важливість впровадження ефектів на загальне ремоделювання печінки при оцінці гістоморфометрії печінки, оскільки кліренс стеатозу або гепатомегалії зміщує відносні значення.
- Вплив вмісту жирних кислот у харчуванні на плечовий хрящ та структуру кістки на моделі миші
- Терапевтичні ефекти адропіну на толерантність до глюкози та використання субстратів при ожирінні, спричиненому дієтою
- Лабораторія Джексона запропонує модель миші для ожиріння та метаболічного синдрому MS-NASH
- Вплив часткового застосування дієти на штучну суміш на зниження ваги та метаболічні показники у людей із ожирінням
- Вплив часткового застосування дієти на штучну суміш на зниження ваги та метаболічні показники у людей із ожирінням