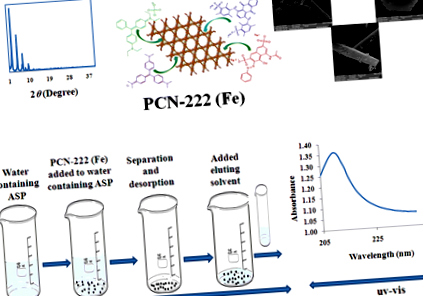
Металоорганічний каркас PCN-222: селективний та високоефективний сорбент для вилучення аспартаму із камеді, соку та дієтичного безалкогольного напою перед його спектрофотометричним визначенням
Анотація
Вступ
Аспартам (ASP; N-L-a-аспартил-1-фенілаланін-1-метиловий ефір), штучний підсолоджувач, в основному використовується у харчових продуктах, безалкогольних напоях, дієтичних продуктах та консервованих фруктах для підвищення якості продукції та терміну зберігання [1]. Існує кілька свідків, які підтверджують наявність взаємозв'язку між прийомом АСП та шкідливими проблемами здоров'я, такими як ожиріння, карієс зубів, канцерогенність, неврологічні проблеми, ризик пухлинних захворювань мозку та лейкемія [2, 3]. Тому необхідно розробити швидкий, простий і чутливий аналітичний метод виявлення ASP у харчових продуктах. За даними спільної продовольчої та сільськогосподарської організації, Всесвітньої організації охорони здоров’я та Експертного комітету з харчових добавок, допустима добова норма споживання ASP становить від 0 до 40 мг/кг маси тіла на день [4].
Спектроскопія (спектрофотометрія, колориметрія та хемілюмінесценція) [5,6,7], електрохімічні методи [8] та хроматографія [9] - найважливіші аналітичні методології, розроблені для визначення ASP. Серед них високоефективна рідинна хроматографія (ВЕРХ) є найпоширенішою методикою, що застосовується для визначення підсолоджувачів, включаючи ASP; але цей метод страждає від високотоксичних органічних розчинників, тривалого часу аналізу та високої вартості.
Спектрофотометрія - приваблива загальноприйнята техніка з перевагами, що включають високу точність, високу точність та низьку вартість аналізу [10], яка підходить для визначення багатьох органічних та неорганічних сполук. Основними недоліками, пов’язаними з цією методикою, є відсутність селективності та нездійсненність виявлення низьких концентрацій аналітів [11]. Ці проблеми можна подолати, застосувавши відповідну техніку екстракції до проведення спектрофотометрії.
Екстракція в твердій фазі (SPE) є одним з найважливіших методів підготовки зразків, який широко застосовується для цієї мети для розділення та попереднього концентрування харчових добавок та штучних підсолоджувачів у різноманітних матрицях зразків [12]. Переваги цього методу включають високу селективність, високу віддачу, хорошу відтворюваність, піддається автоматизації та низьку потребу в органічних розчинниках [13, 14]. У СПЕ сорбент є найважливішою частиною, яка безпосередньо впливає на точність, вибірковість та чутливість вилучення, і багато досліджень зосереджено на вдосконаленні сорбентів СПЕ [15].
Тому ми вирішили підготувати, охарактеризувати та застосувати PCN-222 (Fe) MOF як сорбент для SPE аспартаму, молекули функціональної групи, що містить карбонову кислоту, із зразків з різними матрицями. Були вивчені та оптимізовані експериментальні фактори, що впливають на вилучення.
Експериментальний
Хімікати
Всі реагенти були аналітичного класу і використовувались без подальшого очищення. Хлорид цирконію (IV) (ZrCl4), метил 4-формилбензоат (C9H8O3), пірол (C4H5N), бензойна кислота (C7H6O2), тетрагідрат заліза (II) хлориду (FeCl2 · 4H2O), пропіонова кислота (C3H8O2) хлорхлорид (хлороформ) етанол (C2H6O), метанол (CH4O), глюкоза, сахароза, фруктоза, аскорбат натрію, цикламат, соляна кислота (HCl), N, Nʹ-диметилформамід (DMF), гідроксид натрію (NaOH) і тетрагідрофуран (THF) були отримані від Sigma-Aldrich Chemical Company (MO, США). Аспартам марки реагенту був отриманий від Merck KGaA (Дармштадт, Німеччина). Воду Milli-Q ® (Merck-Millipore, MA, США) використовували (18,3 МОм см -1) протягом усіх експериментів. Основний стандартний розчин аспартаму (1000 мг L -1) готували шляхом розчинення його 1 000 г у 1000 мл дистильованої води. Робочі стандартні розчини готували шляхом послідовних розведень вихідного розчину перед аналізом.
Приладобудування
Синтез MOF PCN-222 (Fe)
PCN-222 (Fe) MOF було синтезовано за допомогою п'ятиступеневого синтезу з комерційно доступного на основі раніше повідомленої процедури за допомогою п'ятиступеневого синтезу [26, 27].
Процедура вилучення твердої фази
Проводили пакетний метод SPE для вилучення ASP, використовуючи PCN-222 (Fe) MOF як сорбент. 250,0 мл розчину зразка переносили в мензурку і доводили його рН до 6,0 за допомогою додавання по краплях або 0,1 М розчину NaOH, або 0,1 М розчину HCl. До розчину додавали 7 мг адсорбенту і струшували на шейкері (200 об/хв, 10 хв), потім центрифугували при 4000 об/хв протягом 8 хв. Водну фазу повністю відкидали. 700 мкл розчину етанол-HCl (99: 1 об/об) додавали до твердої речовини і знову струшували на шейкері (200 об/хв, 15 хв). Нарешті, PCN-222 (Fe) MOF відокремлювали від розчину центрифугуванням при 4000 об/хв протягом 8 хв, а концентрацію ASP в елюції визначали за допомогою спектрофотометрії UV – Vis проти заготовки, приготовленої за тією ж процедурою.
Результати і обговорення
Характеристики PCN-222 (Fe) MOF
Рисунок порошкової рентгенівської дифракції (PXRD) підготовленого MOF PCN-222 (Fe) показаний на рис. 1. Можна помітити, що картина схожа на попередні звіти [26, 27]. Інтенсивні піки на рівні 2θ = 2,5, 4,9, 6,6, 7,1 та 9,9º відносяться до відбиттів (1 0 0), (2 0 0), (2 -1 1), (2 0 1), (4 0 0) та (4 -2 1), відповідно (CCDC No 893,545) [22, 27].
Шаблон PXRD синтезованого MOF PCN-222 (Fe)
Спектр інфрачервоного перетворення Фур'є (FTIR) PCN-222 (Fe) MOF показаний на рис. 2. Піки на рівні близько 1691 та 1417 см -1 пояснюються сильною розтягуючою вібрацією -COO (асиметрична) та -COO (симетрична) зв’язки карбоксилатних груп. Піки приблизно на 1570, 650 та 712 см -1 обумовлені вигином поза площиною C-Hs фенільних кілець [29]. Після сорбції ASP піки інтенсивності при 1700 см -1 і 1570 см -1 зменшувались, що призводило до зміщення в бік нижчих хвильових чисел.
FT-ІЧ-спектр PCN-222 (Fe) та PCN-222 (Fe) -ASP
Пористість підготовленого MOF вимірювали експериментами з адсорбції-десорбції азоту при 77 К. Отримано типову ізотерму типу IV та поверхню Брунауера – Еметта – Теллера (BET) 1650 м 2 г -1, коли процедуру активації було застосовується (рис. 3). Моделювання теорії функціональної щільності сорбції N2 показало, що номінальні MOF мають два типи пор, з розмірами
3 нм (рис. 4) відповідно відповідали трикутним мікроканалам та гексагональним мезоканалам.
Ізотерми адсорбції-десорбції азоту для PCN-222 (Fe) при 77 K
Розподіл пор DFT за розміром для PCN-222 (Fe)
Зображення скануючого електронного мікроскопа (SEM) було застосовано для характеристики морфології синтезованого PCN-222 (Fe) як показано на рис. 5. Як видно на зображенні синтезованого металоорганічного каркасу, воно має типова стрижнеподібна структура, яка була подібною до повідомлених досліджень [30].
SEM PCN-222 (Fe)
Оптимізація процедури SPE
Було вивчено та оптимізовано декілька важливих параметрів, що впливають на ефективність екстракції, включаючи рН розчину зразка, кількість адсорбенту, тип та об'єм елюючого розчинника, час адсорбції та десорбції, як обговорюється нижче. Для цього використовували стандартний розчин 10 мг L -1 ASP.
Вплив рН
РН розчину зразка є одним із найбільш критичних параметрів адсорбції ASP на MOF, що свідчить про його вплив двома факторами: формою аналіту та ділянками поверхневого зв’язування на адсорбенті [31]. РН серії стандартних розчинів ASP змінювався в межах 3,0–9,0, а результати показані на рис. 6. Як видно, оптимальна точка досягається при рН 6,0. Механізм адсорбції аспартаму на MOF PCN-222 (Fe) можна пояснити електростатичною взаємодією між аспартамом та адсорбентом. Згідно з попереднім дослідженням, нульова точка заряду PCN-222 (Fe) MOF спостерігалася при рН = 6,4 [32]. При рН, відмінних від цього значення, поверхневий заряд MOF заряджається. З іншого боку, ізоелектричну точку ASP визначали як 5,25 (pK1 3,18, pK2 7,82) [33]. При рН близько 6 MOF заряджений позитивно, тоді як ASP знаходиться в аніонній формі, тому відновлення збільшується.
Вплив pH на екстракційне відновлення ASP (умови адсорбції: 100 мкл 10,0 мг L -1 розчину ASP; 10 мг адсорбенту; 15 хв контактного часу)
Вплив типу та об'єму елюентів
Вивчався вплив елюентного типу на відновлення ASP з MOF. Випробовували метанол, етанол, ацетонітрил, вода – HCl (99: 1 об./Об.), Метанол-HCl (99: 1 об./Об.) Та етанол-HCl (99: 1 об./Об.). Концентрацію кислоти слід підтримувати на якнайнижчому рівні, щоб запобігти деградації MOF. Отримані результати показані на рис. 7. Кількісне відновлення ASP було отримано з використанням етанол-HCl (99: 1 об./Об.) Як елюент, можливо тому, що кислота може перетворити ASP з аніонної форми в нейтральну.
Вплив типу елюентів на екстракційне відновлення ASP (умови адсорбції: 100 мкл 10,0 мг L -1 розчину ASP; 10 мг адсорбенту; 15 хв контактного часу; рН: 6)
Вплив об'єму елюючого розчинника досліджували в діапазоні 200–1000 мкл (рис. 8). Результати показують, що 700 мкл етанол-HCl (99: 1 об./Об.) Є сприятливим для отримання максимального відновлення екстракції ASP. При більших обсягах спостерігається розбіжний ефект, ймовірно, через ефект розведення елюйованого ASP.
Вплив об'єму елюючого розчинника на відновлення екстракції ASP (умови адсорбції: 100 мкл 10,0 мг L -1 розчину ASP; 10 мг адсорбенту; 15 хв контактний час; рН: 6)
Вплив кількості сорбенту
Ефект дозування адсорбенту на відновлення екстракції ASP в межах 1,0–10,0 мг показано на рис. 9. Максимальне відновлення екстракції було отримано, коли кількість MOF становило 7,0 мг. Як видно, лише незначної кількості адсорбенту було достатньо для вилучення ASP через його високу адсорбційну здатність. Таким чином, 7 мг PCN-222 (Fe) використовували для подальших експериментів.
Вплив кількості MOF PCN-222 (Fe) на відновлення екстракції ASP (умови адсорбції: 100 мкл 10,0 мг L-1 розчину ASP; 15 хв контактного часу; pH: 6)
Вплив часу адсорбції та елюції
Для досягнення найкращого часу рівноваги необхідно оптимізувати час контакту для адсорбції та десорбції аналіту. Час контакту 2, 5, 10, 15, 20 і 25 хв тестували як на екстракцію, так і на вимивання. Результати зображені на рис. 10. Час, необхідний для досягнення рівноваги для адсорбції та елюції, становив 10 хв та 15 хв відповідно. Ця швидка кінетика обумовлена високою питомою поверхнею та великими порами синтезованого MOF.
Вплив часу контакту адсорбції та елюції на відновлення екстракції ASP (умови адсорбції: 100 мкл 10,0 мг L-1 розчину ASP; рН: 6; 7 мг адсорбенту)
Ефект від іонна сила
Вплив іонної сили на ефективність екстракції ASP вивчали, роблячи розчин зразка 0,0–1,0 моль L −1 щодо хлориду натрію, тоді як інші умови експерименту підтримували постійними. Результати показали, що сигнал поглинання ASP майже не залежав від іонної сили розчину; отже, всі екстракційні експерименти проводились без додавання солі.
Вплив обсягу вибірки
Для отримання високого коефіцієнта попередньої концентрації досліджували вплив обсягу зразка на ефективність екстракції ASP в діапазоні 10,0–500,0 мл. Результати показали, що відновлення ASP було дуже ефективним (> 98%) в діапазоні обсягу проби 10–250 мл, а після цього відновлення зменшується. Отже, у подальших дослідженнях було використано 250 мл розчину зразка.
Коефіцієнт збагачення (EF), визначений як відношення об'єму зразка 250 мл до кінцевого об'єму елюції 700 мкл, очікувалося становити 357 разів, що було закрито до 350 разів експериментально.
Вплив перешкод
Селективність даного методу досліджували шляхом аналізу стандартних розчинів, що містять 10 мг L-1 ASP у присутності великих кількостей загальних сполук, які зазвичай існують разом з ASP. Межа допуску була визначена як максимальна концентрація чужорідних видів, що викликає похибку менше ± 5% при визначенні ASP. Результати, узагальнені в таблиці 1, показали, що досліджувані види не перешкоджають попередній концентрації та визначенню ASP запропонованим методом.
Лінійний діапазон, межа виявлення та точність
В оптимальних умовах лінійний діапазон, межа виявлення, коефіцієнт детермінації, коефіцієнт збагачення, точність і точність запропонованого методу були отримані та зведені в таблицю 2. Калібрувальна крива була лінійною в діапазоні концентрацій 0,1-100 мг L - 1 з коефіцієнтом детермінації (R 2) 0,997. Визначення межі відхилення (LOD), отримане з 3 (Sd) заготовки/м (де (Sd) заготовка - це стандартне відхилення десяти послідовних вимірювань заготовки та м - нахил калібрувальної кривої), становив 0,019 мг L -1. Для оцінки сорбційної здатності MOF, в оптимальних умовах адсорбції ASP, 7 мг цього сорбенту додавали до 250,0 мл 10 мг L −1 стандартного розчину ASP і після досягнення рівноваги концентрацію решти ASP визначали за допомогою ВЕРХ шляхом безпосереднього введення 10 мкл розчину та порівняння з калібрувальною кривою. Для кількісних оцінок використовували площі піків.
Встановлено, що адсорбційна здатність становить 356 мг г -1, що було розраховано з наступного рівняння [34]:
де C0 та Ce - початкові та рівноважні концентрації ASP, V (L) - об'єм розчину зразка, а m (g) - доза адсорбенту. Відносне стандартне відхилення (RSD%) семи повторюваних вимірювань для одного і того ж розчину було Таблиця 3 Порівняння запропонованого методу з іншими методами для визначення ASP
Реальний аналіз вибірки
Для оцінки ефективності цього методу для аналізу реальних зразків у складних матрицях запропонована процедура була застосована до визначення ASP у трьох різних зразках, тобто безалкогольному напої кола, персиковому соку та бульбашці.
Сік дегазували та гомогенізували протягом 10 хв в ультразвуковій ванні, а напій кола дегазували, поклавши на шейкер на 15 хв. Для жувальної гумки одну паличку (масою 2,7 г) розбивали на дрібні шматочки (приблизно 3 × 3 мм) і переносили в мірну колбу об'ємом 120 мл і суміш оцтової кислоти, води та хлороформу (1:50:25 об/v) додавали до нього і перемішували при високій швидкості протягом 10 хв. Всі кінцеві розчини фільтрували через 0,45 мкм фільтри і, нарешті, 10-мл аликвоту кожного розбавляли в 100-мл мірній колбі перед аналізом. Визначена кількість ASP спостерігалася у всіх зразках (табл. 4). Для підтвердження достовірності аналізів також був проведений стандартний метод ВЕРХ [35]. Для кращої оцінки ефекту матриці, зразки додавали, додаючи відповідні кількості ASP, та аналізували згідно MOF-SPE/спектрофотометричного методу. Середні показники видобутку коливались від 97% до 104%, при цьому були отримані RSD від 1,0 до 3,6% (n = 3), що чітко показує, що цю процедуру можна успішно застосувати для визначення рівня сліду підсолоджувача ASP у різних зразках. Як приклад, спектр зразка коли з додаванням 50 мкг L -1 ASP і екстрагованого MOF-SPE зображено на рис. 11.
Спектр зразка напою кола з додаванням 50 мкг L -1 ASP після екстракції MOF-SPE
- Росія зміцнить опору на ринку органічного м'яса
- Засоби природного ожиріння - рослинні; Варіанти лікування органічного ожиріння Природні
- Фотолюмінесцентний бічний потік імунологічного аналізу, виявлений оксидом графена, високочутливою на папері
- Розчини для розведення молочних телят Sprayfo можуть виростити молочних телят у високопродуктивних молочних телиць
- Нова технологія сміттяра дозволяє роботам харчуватися металом для отримання енергії - ScienceDaily