Лікування та рецидив аутоімунного панкреатиту
Сун-Хун Місяць
Кафедра внутрішньої медицини, Університет Ульсанського медичного коледжу, Медичний центр Асан, Сеул, Корея.
Мун Хван Кім
Кафедра внутрішньої медицини, Університет Ульсанського медичного коледжу, Медичний центр Асан, Сеул, Корея.
Зробіть Hyun Park
Кафедра внутрішньої медицини, Університет Ульсанського медичного коледжу, Медичний центр Асан, Сеул, Корея.
Анотація
Аутоімунний панкреатит (АІП) - це своєрідний тип хронічного панкреатиту, патогенез якого включає аутоімунні механізми. Реакція стероїдів має значний вплив на діагностику ПДВ, оскільки пацієнти з ПДВ та раком підшлункової залози мають багато клінічних особливостей. Цей огляд зосереджений на лікуванні та рецидиві ПДІ. Метою лікування AIP є зменшення симптомів, серологія, рентгенологічні зміни або гістологія, що також стосується рецидивів. Хоча загальновизнано, що стероїди слід пропонувати хворим на ІПП з активним захворюванням, не існує стандартизованого режиму стероїдів для АІП та немає єдиної думки щодо дози та тривалості графіку індукції та зменшення стероїдів, а також оптимальної тривалості та дози підтримуючої терапії. Отримання консенсусу щодо оптимальної схеми лікування є дуже важливим для зменшення частоти рецидивів. У цьому огляді ми обговорюємо схеми лікування, що застосовуються у багатьох центрах.
ВСТУП
Аутоімунний панкреатит (АІП) - це своєрідний тип хронічного панкреатиту, при якому аутоімунні механізми беруть участь у патогенезі. 1 З клінічного боку стероїдна чутливість AIP передбачає значний вплив, оскільки пацієнти з AIP та раком підшлункової залози мають багато клінічних особливостей. 2
Завдяки японським слідчим здатність діагностувати ПДІ значно покращилася за останнє десятиліття. Однак набагато менше відомо про деталі лікування АІП після постановки діагнозу. Цей огляд зосереджений на лікуванні та рецидиві ПДІ. Це пов’язано з тим, що деякі складності, пов’язані з «лікуванням», мають відношення до «рецидиву» в AIP. Наприклад, досягнення консенсусу щодо оптимального режиму прийому стероїдів може в свою чергу призвести до низького рівня рецидивів.
ВИЗНАЧЕННЯ РЕЗУЛЬТАТІВ ЛІКУВАННЯ
Обговорюючи лікування АІП, важливо використовувати конкретні терміни, які допомагають визначити цілі та відповіді на лікування. 3 Незважаючи на збільшення кількості статей, опублікованих у літературі, існує відсутність консенсусу щодо термінології, пов'язаної з результатами лікування, включаючи ремісію та рецидив. Досягнення консенсусу щодо їх визначення буде важливим для порівняння результатів лікування між різними центрами.
1. Ремісія
Метою лікування AIP є досягнення ремісії. Ремісія може стосуватися симптомів, серології, рентгенологічних змін або гістології. 3 Повна ремісія стосується вирішення симптомів, пов’язаних із захворюваннями, а також серологічних, рентгенологічних та гістологічних відхилень. Вирішення симптомів (симптоматична ремісія) досягається швидко при ВІП, оскільки обструктивна жовтяниця та супутні симптоми можуть зникнути протягом 2-3 тижнів. 3, 4. Однак серологічна ремісія (особливо при нормалізації рівня IgG4 у сироватці крові) та рентгенологічна ремісія (вирішення маси підшлункової залози та/або протокових стриктур) можуть зайняти більше часу. 3 Гістологічну ремісію важче підтвердити через труднощі з проведенням біопсії підшлункової залози. 5 Отже, на практиці кінцевою точкою лікування часто є симптоматична ремісія разом із рентгенологічною ремісією. 3 Прийняття консенсусу щодо визначення ремісії є дуже важливим, оскільки воно має відношення до визначення кінцевої точки лікування.
У нещодавньому звіті Великобританії було оцінено 6 клінічних ремісій з точки зору пре- та постстероїдних симптомів, біохімії печінки та радіологічних проявів. Рівень IgG4 у сироватці крові не був включений у серологічну ремісію. У їх дослідженні всі пацієнти, у яких рівень IgG4 не зміг нормалізуватися під час лікування стероїдами, зрештою рецидивували. Після лікування стероїдами у пацієнтів може спостерігатися постійно підвищений рівень IgG4 у сироватці крові без симптомів або рентгенологічних ознак активності захворювання. 7 Чи представляє це субклінічну активність захворювання, незрозуміло. Можливість того, що постійно підвищений рівень IgG4 у сироватці крові під час лікування може керувати застосуванням подальшої імуносупресії, вимагає подальших досліджень. 6 Деякі пацієнти з рецидивом, у яких рівень IgG4 у сироватці крові не нормалізувався при лікуванні стероїдами, може представляти собою спалах залишкових захворювань, а не справжній рецидив після повної ремісії.
2. Рецидив
Як і при ремісії, рецидив може бути симптоматичним, рентгенологічним, серологічним або гістологічним. 3 Симптоматичний рецидив зазвичай асоціюється з рентгенологічними та серологічними рецидивами. Однак серологічний рецидив (наприклад, підвищений рівень концентрації IgG4 у сироватці крові) може спостерігатися у пацієнтів без симптомів або рентгенологічних ознак активності захворювання. 3 Визначення рецидиву не є єдиним серед авторів. Частота рецидивів може змінюватися залежно від застосованого визначення. На практиці рецидив, як правило, визначають як рецидив рентгенологічних проявів ПДІ (із симптомами або без них) у підшлунковій залозі або позапанкреатичних органах. 3 Визначаючи рецидив, автори, як правило, не розрізняють рецидив підшлункової залози від виникнення захворювання в іншому органі, або de novo, або справжній рецидив раніше лікуваного захворювання в цьому органі. 3
ЛІКУВАННЯ
На відміну від звичайного хронічного панкреатиту, AIP різко реагує на терапію стероїдами. 2 Стероїдна терапія призводить до поліпшення клінічних симптомів та супутніх рентгенологічних та серологічних відхилень. В принципі, спосіб лікування АІП можна класифікувати на медичну та хірургічну терапію. Роль резекційної хірургії ще не з’ясована, і зазвичай це робиться без передопераційних підозр на AIP. Це може бути лікувальним, якщо повністю зняти запалення в так званому масоутворюючому AIP. 8 Однак ми не можемо виключити можливість залучення залишкової підшлункової залози після операції. 9 Згідно з дослідженням Вебера та співавт., Частота рецидивів 10 після панкреатектомії становила 28% (8/29), а жовчарна стриктура була найпоширенішим клінічним проявом. Існує також занепокоєння щодо недостатності підшлункової залози у пацієнтів з рецидивом АІП після часткової панкреатектомії. Враховуючи значну частоту рецидивів після резекції підшлункової залози та сучасну концепцію AIP як системного захворювання, пов’язаного з IgG4, 11, 12 стероїд слід розглядати як перший вибір терапії при AIP.
1. Показання стероїдної терапії
Хоча пацієнти з AIP добре реагують на преднізолон, залишається незрозумілим, чи необхідна стероїдна терапія для всіх пацієнтів з AIP. 13 Існують анекдотичні повідомлення про спонтанну ремісію у хворих на ІПВ. 11, 14 Незважаючи на те, що у деяких пацієнтів з AIP може спостерігатися спонтанна ремісія, використання стероїдів може призвести до ремісії послідовно і швидше, ніж у випадках без лікування. 13, 15 Роль стероїдів у лікуванні безсимптомних рентгенологічних відхилень неясна. Невідомо, чи будуть у безлікованих безсимптомних пацієнтів більше рецидивів, ніж у безсимптомних пацієнтів, які отримували стероїди. Якщо так, це виправдовує лікування безсимптомних пацієнтів. Загальновизнано, що стероїди слід пропонувати хворим на ВІЛ з "активним" захворюванням. Клінічними проявами пацієнтів з більшістю ознак активного захворювання є обструктивна жовтяниця, зумовлена стенозом жовчної протоки або наявністю інших супутніх системних захворювань, таких як ретроперитонеальний фіброз. 11 Навпаки, виявляється, що роль стероїдів у пацієнтів, які перебувають у постгострій фазі з атрофією підшлункової залози, відсутня. 15
У той час як більшість хворих на AIP отримують жовчні стенти під час опрацювання жовтяниці, є деякі пацієнти, у яких жовтяниця полегшується лише стероїдною терапією без необхідності стентування. 16 Незрозуміло, чи можна лікувати непрохідність жовчовивідних шляхів лише стероїдною терапією без необхідності стентування до призначення стероїдів. 16 Якщо біліарний стент ставлять після виявлення жовчних стриктур, видалення стента можливе через 2 місяці після початку прийому стероїдів у більшості пацієнтів.
2. Стероїдний режим
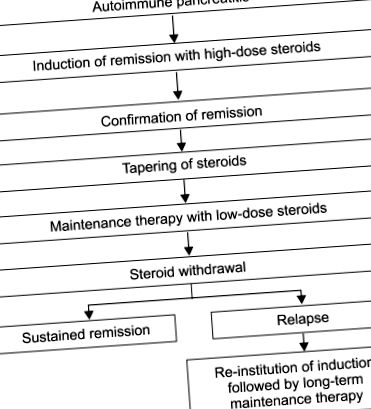
Блок-схема (рис. 1) демонструє стратегію лікування в нашому закладі лікування АІП. Після діагностики починають індукційну дозу преднізолону. Реакція на стероїди оцінюється з точки зору пре- та постстероїдних симптомів, біохімії печінки, рівня IgG/IgG4 у сироватці крові та радіологічних проявів. Після підтвердження клінічної ремісії преднізолон поступово знижується до підтримуючої дози. Підтримуюча терапія низькими дозами стероїдів використовується для запобігання рецидиву захворювання та підтримання ремісії. Нарешті, стероїди зазвичай повністю припиняють.
Алгоритм лікування аутоімунного панкреатиту.
Вибір підтримуючої терапії (низькі дози стероїдів проти інших імуномодулюючих засобів) при рецидиві не встановлений. 15 У клініці Mayo 15 замість використання довготривалих низьких доз стероїдів вони вирішили використовувати азатіоприн (2 мг/кг щодня) для підтримки ремісії у пацієнтів з рецидивом після відміни стероїдів. Вибір препарату для підтримання ремісії потребує подальших досліджень на більшій кількості пацієнтів для оцінки співвідношення ризик/користь (профілактичний ефект при рецидиві проти побічної дії ліків) кожного підходу. Згідно з нещодавньою доповіддю, 24 пацієнта з AIP та IgG4-асоційованим холангітом, стійким до стероїдів та 6-меркаптопурину, лікували виключно ритуксимабом. Ритуксимаб - це химерне моноклональне антитіло, спрямоване проти CD 20, фосфопротеїну, що експресується на поверхні В-лімфоцитів. Вважається, що механізмом дії ритуксимабу є виснаження В-клітин, що призводить до зменшення продукції патогенних аутоантитіл. Ритуксимаб може бути варіантом лікування для пацієнтів з рефрактерним або рецидивуючим AIP або IgG4-асоційованим холангітом. 24
РЕЛАПС
Рецидив після ремісії AIP не рідкість. Рецидиви AIP після ремісії при застосуванні стероїдів зазвичай трапляються приблизно у третини пацієнтів. 16 Іноді підшлункову залозу можна врятувати і задіяти лише позапанкреатичний орган (рис. 2). Здається, симптоми, обумовлені стриктурою жовчних шляхів, можуть бути найпоширенішим клінічним проявом при рецидиві. 16 У пацієнтів спостерігається рецидив AIP або під час підтримуючої терапії стероїдами, або після повного припинення прийому стероїдів. 25
Серійні зображення 67-річного чоловіка з AIP. Перший напад: (A, B) Перед терапією стероїдами КТ показує дифузне збільшення підшлункової залози, а ERCP - звуження (стрілка) дистального відділу загальної жовчної протоки (CBD) та розширення проксимального CBD. (C, D) Після терапії стероїдами збільшення підшлункової залози покращується із зменшенням дилатації CBD. При рецидиві: (E) Перед терапією стероїдами MRCP демонструє мультифокальні стриктури в гомілковому та внутрішньопечінковому жовчних протоках без ураження протоки підшлункової залози. (F) Після лікування стероїдами вирішуються мультифокальні біліарні стриктури.
AIP, аутоімунний панкреатит.
Згідно з нашим дослідженням, 20 середнього періоду спостереження 40 місяців у 13 із 40 пацієнтів (33%) спостерігався рецидив ПДІ. У семи з 13 пацієнтів спостерігався рецидив підтримуючої дози преднізолону (2,5-7,5 мг/добу), а у решти 6 пацієнтів спостерігався рецидив при відсутності стероїдів. Після рецидиву всі вони знову реагували на високі дози преднізолону. Цим пацієнтам із рецидивом підтримуюча терапія стероїдами призначалася з більшою тривалістю та більшою дозою, ніж початкова підтримуюча терапія.
Клінічні наслідки рецидиву AIP такі. Більше половини пацієнтів із багаторазовими рецидивами мали кальцифікації підшлункової залози або камені. 26 При множинних рецидивах AIP може призвести до незворотних пошкоджень з інтенсивним фіброзом, подібним до розвитку звичайного хронічного панкреатиту. 27 Хоча пацієнти з AIP із першим рецидивом знову реагують на стероїди, ця пізня стадія AIP з множинними рецидивами може не виявляти реакції на стероїди. Тому для кращого прогнозу AIP важливе значення мають попередні діагностика та лікування.
1. Провісники рецидиву
Визначення клінічних та/або генетичних предикторів рецидиву ПДІ може мати вирішальне значення для прогнозу та клінічного результату захворювання. Визначення предикторів рецидиву може допомогти нам визначити пацієнтів з високим ризиком, яким дійсно виграє підтримуюча терапія. Для пацієнтів з AIP, які мають предиктори рецидиву, може знадобитися коригувати стратегію лікування, включаючи більш високі дози або довше введення підтримуючої стероїдної терапії або додаткове лікування іншим імунодепресантом. Крім того, для цих пацієнтів може знадобитися більш ретельне спостереження.
1) Клінічний провісник
2) Генетичний провісник
СЛІДУВАТИ
Нещодавно в літературі з’являються повідомлення про рак підшлункової залози, що ускладнює AIP через роки після його діагностики. 35 - 37 Незрозуміло, чи подальший розвиток раку підшлункової залози є справжнім ускладненням тривалого AIP або випадковим явищем у літнього чоловіка, який також випадково мав AIP. 35 Потрібні довготривалі дослідження у великих когортах AIP, щоб визначити, чи схильний AIP до подальшого розвитку раку підшлункової залози, оскільки рак, як правило, виникає через десятки років після початку хронічного панкреатиту. 35
ВИСНОВКИ
Незважаючи на те, що в нашому розумінні було досягнуто значного прогресу в діагностиці ПДІ, знання про оптимальну схему лікування та прогностичні фактори рецидиву ще має пройти довгий шлях. Прийняття консенсусу щодо оптимальної схеми лікування дуже важливо, оскільки це, в свою чергу, може призвести до низького рівня рецидивів. Слід встановити консенсусні визначення щодо результатів лікування. Потрібні подальші дослідження в цій галузі.
- Лікування міо-інозитолом та селеном забезпечує еутиреоз у пацієнтів з аутоімунною системою
- Цілюща сила сміху при лікуванні розладів харчування
- Розуміння анорексії - варіанти приватного лікування
- Розуміння джерел харчового фосфору при лікуванні хворих на хронічну нирку
- Стриктура уретри Причини, симптоми, діагностика та лікування