Комплекс з натуральних волокон зменшує масу тіла у людей із надмірною вагою та ожирінням: подвійне сліпе, рандомізоване, контрольоване плацебо дослідження
Барбара Грубе
1 Практика загальної медицини, Берлін, Німеччина
Пі-Він Чонг
2 Відділ досліджень та розробок, InQpharm Europe Ltd., Лондон, Великобританія
Кай-Жия Лау
2 Відділ досліджень та розробок, InQpharm Europe Ltd., Лондон, Великобританія
Ганс-Дітер Ожеховський
3 Інститут клінічної фармакології та токсикології, Charité Universitaetsmedizin, Берлін, Німеччина
Анотація
Об’єктивна
Запатентований природний комплекс клітковини (Litramine IQP G-002AS), отриманий з Opuntia ficus-indica, і стандартизований за ліпофільною активністю, раніше був показаний в доклінічних дослідженнях та дослідженнях на людях для зменшення поглинання жиру через шлунково-кишковий тракт (GI). Тут ми досліджували ефективність та безпеку IQP G-002AS у зменшенні маси тіла.
Дизайн та методи
У дослідженні взяли участь двадцять п’ять дорослих із зайвою вагою та ожирінням. Суб'єкти отримували консультації щодо фізичної активності та отримували дієтичні консультації, включаючи гіпокалорійну дієту (30% енергії від жиру та 500 ккал дефіциту на добу). Після 2-тижневої фази введення плацебо пацієнтів рандомізували для отримання або 3 г/день IQP G-002AS (IQ), або плацебо. Первинною кінцевою точкою була зміна маси тіла від вихідної; вторинні кінцеві точки включали додаткові заходи щодо ожиріння та параметри безпеки.
Результати
Сто двадцять три суб'єкти завершили 12-тижневу фазу лікування (популяція, призначена для лікування (ITT): 30 чоловіків та 93 жінки; середній ІМТ: 29,6 ± 2,8 кг/м 2 та вік: 45,4 ± 11,3 року). Середня зміна маси тіла від базової лінії становила 3,8 ± 1,8 кг в IQ проти 1,4 ± 2,6 кг у плацебо (Р 2 (20).
Дослідження включало 2-тижневу фазу введення плацебо та 12-тижневу фазу лікування. Фаза обкатки мала на меті оцінити відповідність досліджуваних лікуванню (на основі сукупного споживання таблеток плацебо) та дієтичного режиму. Після завершення 2-тижневої фази обкатки пацієнтів, у яких відповідність лікуванню становило щонайменше 80%, спостерігалося зниження маси тіла і відхилення менше ніж 20% від встановленого добового споживання калорій, було рандомізовано у співвідношенні 1: 1 або до групи IQP G-002AS (IQ), або до групи плацебо. Рандомізація була проведена з використанням блоку розміром 4 незалежним біостатом, використовуючи схему рандомізації BIAS для Windows V9.2 (http://www.bias-online.de).
Протягом 12-тижневого періоду лікування суб'єкти отримували або дві таблетки по 500 мг IQP G-002AS, або відповідне плацебо тричі на день. Випробовуваним було наказано споживати досліджувані ліки після сніданку, обіду та вечері. Таблетка плацебо, ідентична за зовнішнім виглядом IQP G-002AS, містила 500 мг мікрокристалічної целюлози як замінник активних інгредієнтів. Вони були упаковані у пляшки та марковані незалежним фармацевтом для кожного суб'єкта згідно з графіком рандомізації. Всі випробовувані та досліджуваний персонал не були проінформовані про призначення навчальної групи.
Всім випробовуваним було доручено дотримуватися збалансованої з поживної точки зору та м’яко гіпокалорійної дієти протягом 2-тижневої фази обкатки та 12-тижневої фази лікування. Помірковано гіпокалорійний план дієти був розроблений Німецьким інститутом серця, Берлін, Німеччина. Він забезпечував 30% енергії з жиру, 55% з вуглеводів і 15% з білка. Щоденну потребу в енергії оцінювали (для кожного предмета) згідно рівняння Інституту медицини (МОМ) Національних академій на основі віку, статі, маси тіла та рівня фізичної активності (21). Калорії, що містяться в м’яко гіпокалорійній дієті, були еквівалентні передбачуваній добовій енергії, мінус 500 ккал. Крім того, випробовуваним рекомендували поступово збільшувати фізичну активність (30 хв фізичної активності середньої інтенсивності, наприклад, ходьби або їзди на велосипеді).
Плани дієт розподілялись серед усіх суб'єктів на початковому етапі, а вказівки давались з інтервалом у 4 тижні протягом 12-тижневого періоду лікування. Тематичні щоденники видавались на початковому, 4-му та 8-му тижнях, а щоденники щоденного дослідження оцінювались при кожному відвідуванні, крім базового.
Скринінг
Скринінговий візит включав детальну історію хвороби, загальний фізичний огляд та вимірювання артеріального тиску, частоти серцевих скорочень, маси тіла, зросту, окружності талії та вмісту жиру в організмі. Кров брали для клінічної хімії, гематології, ліпідного профілю та тесту на вагітність. Всі зразки крові аналізували централізовано (Medizinisch-Diagnostische Institute, Берлін, Німеччина).
Параметри ефективності
Основним параметром ефективності була зміна маси тіла (кг) через 12 тижнів порівняно з вихідним рівнем. Вагу тіла вимірювали за допомогою відкаліброваної шкали зважування (Tanita BC-420 SMA; Tanita, Токіо, Японія) у пацієнтів, які носили нижню білизну і не мали взуття, на початковому рівні та з інтервалом у 4 тижні, протягом 12-тижневого періоду лікування.
Вторинні параметри ефективності включали частку пацієнтів, які втратили щонайменше 5 і 10% від базової маси тіла; зниження середнього ІМТ; зменшення середньої окружності талії, яке вимірювалось на рівні посередині між бічним нижнім краєм ребра і гребінем клубової кістки; зміна вмісту жиру в організмі (кг та%), яку вимірювали методом біоімпедансу за допомогою перевіреної електронної ваги Таніта BC-420 SMA. Ці параметри також вимірювали на початковому етапі та з інтервалом у 4 тижні протягом 12-тижневого періоду лікування.
Параметри безпеки
Оцінка безпеки включала вимірювання життєво важливих ознак (таких як частота серцевих скорочень та артеріальний тиск у спокої) та оцінку параметрів крові, включаючи: клінічну хімію (електроліти, жиророзчинні вітаміни, функцію печінки та нирок та метаболізм пуринів), гематологічний та ліпідний профіль (загальний холестерин, тригліцериди, ліпопротеїни низької щільності та ліпопротеїни високої щільності). Частоту серцевих скорочень та артеріальний тиск у спокої оцінювали під час кожного відвідування за допомогою стандартного приладу; тоді як параметри крові оцінювали двічі, під час скринінгу та після завершення 12-тижневого дослідження. Суб'єкти також оцінювали переносимість досліджуваних препаратів суб'єктивно в кінці дослідження. Були зареєстровані всі побічні явища, незалежно від їх причинності до лікування.
Статистичний аналіз
Оцінка ефективності IQ базувалася на нульовій гіпотезі про відсутність різниці між IQ та плацебо у середньому зниженні маси тіла.
Розмір вибірки розраховували на основі первинної кінцевої точки, зміни маси тіла від базової лінії. Мінімальний обсяг вибірки 125 суб'єктів (з корекцією 30% відсіву) забезпечував 80% потужності дослідження для виявлення різниці втрат ваги у 1,78 кг між групами при рівні значущості 0,045. Оскільки пілотне випробування не проводилось з IQ, оцінка обсягу вибірки базувалася на обмеженій опублікованій літературі (22-, 23). Тому прослідкуваний тимчасовий аналіз був визнаний необхідним. На основі методу Віттеса-Бріттена рівень значущості був відрегульований до 4,5% (двосторонній тест), що відповідало вимозі номінального рівня значущості О'Брайена-Флемінга. Проміжний аналіз (проведений після того, як половина суб'єктів закінчила 12-тижневе дослідження) показав, що коригування обсягу вибірки не потрібно.
Демографічні та базові характеристики змінних ефективності та безпеки спочатку оцінювали на основі описової статистики. Всі первинні та вторинні змінні, а також змінні безпеки оцінювались як відносні зміни в кожній групі. Параметричний аналіз, такий як незалежний t-критерій, використовувався, головним чином, для визначення різниці між групами. Багаторазові вимірювання ANOVA використовували для оцінки всіх змінних ефективності в проекті повторних вимірювань. Різницю між групами категоріальних змінних проводила статистика χ 2. Крім того, випробовуваних класифікували на групи із зайвою вагою (ІМТ 2) та ожирінням (ІМТ ≥30 кг/м 2), а також аналіз підгруп проводили для визначення ефективності IQP G-002AS лише для осіб із ожирінням та надмірною вагою, дискретно.
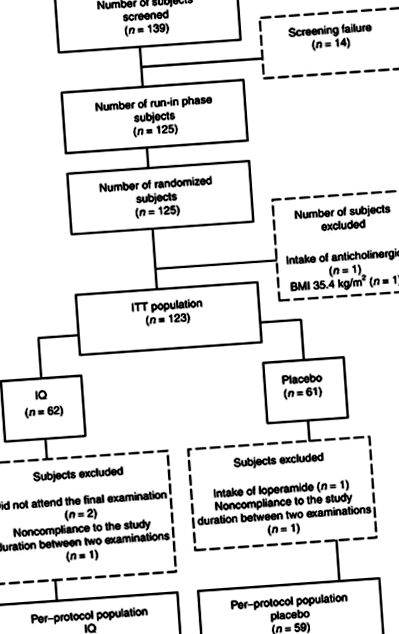
Для всіх статистичних аналізів P 2. Демографічні характеристики населення ITT наведені в таблиці 1. Базові характеристики IQ та плацебо були подібними; не було суттєвої різниці між групами у розподілі за статтю, віком, зростом тіла, масою тіла та ІМТ. В аналізі за протоколом було додатково виключено 5 суб'єктів з 59 суб'єктами в групі IQ та плацебо з причин, як описано на рисунку 1 .
Розробка навчального плану та розташування предметів ITT, намір для лікування.
- Рандомізоване дослідження, що перевіряє ефективність нового підходу до схуднення серед чоловіків
- Протизапальна дієтична комбінація у жінок із надмірною вагою та ожирінням із синдромом полікістозу яєчників
- Дослідження конституції Традиційної китайської медицини, пов'язаної з надмірною вагою, ожирінням та
- Рандомізоване дослідження дієт і вправ на тілі з високим вмістом молочних білків, змінних вуглеводів
- 10 природних способів зменшити дієтичні таблетки Windows для зниження ваги