Комбінована блокада поперекового та крижового сплетень у геріатричних пацієнтів високого ризику, які перебувають у стані неспокійного відновлення перелому міжчеревної кістки стегна
Том 4 | Випуск 1 | Січень-квітень 2018 | сторінка: 21-30 | Сандіп Діван, Четан Прадхан, Атул Патіл, Четан Пурам, Параг Санчеті
Автори: Сандіп Діван [1], Четан Прадхан [2], Атул Патіл [2], Четан Пурам [2], Параг Санчеті [3]
[1] Відділення анестезії, лікарня спеціалізованої хірургії Санчеті, Пуна, штат Махараштра, Індія,
[2] Відділення ортопедії, лікарня спеціалізованих хірургічних операцій Санчеті, Пуна, штат Махараштра, Індія.
[3] Професор та голова лікарні для спеціалізованих хірургічних операцій Санчеті, Пуна, Махараштра.
Адреса листування
Доктор Сандіп Діван,
Відділення анестезії,
Лікарня для спеціалізованої хірургії Санчеті, Пуна, Махараштра, Індія.
Електронна адреса: [email protected]
Анотація
Геріатричне населення з його численними супутніми захворюваннями ризикує розвитку ускладнень, пов’язаних з анестезією. Дані не дозволяють визначити, чи покращує загальна анестезія, епідуральна або спинальна (регіональна) анестезія результати після операції на переломі стегна. Автор (S M D) піддав усі міжперервні переломи 3 та 4 ступеня ASA блокуванню попереково-крижового сплетення. Інтраопераційна гемодинамічна стабільність була ключовою ознакою у всіх пацієнтів, що відображало стабільний післяопераційний сценарій. Позитивний результат, рання взаємодія між пацієнтом та допоміжна рухливість пацієнта на 2-й день призводять до збільшення попиту на блок попереково-крижового сплетення у гериартриках високого ризику з міжчеревними переломами.
Ключові слова: Переломи міжчеревної, місцевої анестезії, блокади поперекового сплетення, нервової блокади, післяопераційного знеболення, блокування крижового сплетення.
Вступ
У цьому випадку серії, що тягнуться з 5 січня 2015 року по 31 січня 2017 року, автор представляє 50 пацієнтів високого ризику з множинними супутніми захворюваннями, перерахованими для відновлення переломів міжчеревця з відкритим зменшенням та внутрішньою фіксацією. Всі хірургічні втручання проводились під комбінованим блоком попереково-крижового сплетення (SPB). Жоден із цих пацієнтів не отримував загального наркозу. Перші 5 складних випадків обговорюються в цій статті. Інші 6/50 випадків наведені в таблиці 1.
Усі 50 пацієнтів без особливих зусиль одужали і були виписані до палати/кімнати після первинного перебування у відділенні критичної допомоги. Будуть обговорені методи блокування попереково-крижового сплетення (LSPB) при операціях на переломах кульшового суглоба, а також наявні дані, ускладнення, суперечки та пропозиції, що розвиваються навколо LSPB.
Звіти про справи
Випадок 2
80-річний чоловік із порушенням функції нирок в анамнезі був госпіталізований з переломом міжчеревця ліворуч. Дослідження крові виявило гемоглобін (Hb) - 8,5 г/дл, БУЛ - 80 мг/дл, а креатинін у сироватці крові 3,0 мг/дл. Ехокардіограф згадав фракцію викиду лівого шлуночка - 28%, діастолічна дисфункція лівого шлуночка (ЛШД) була ІІІ ступеня, гіпертрофія лівого шлуночка та легка регургітація через мітральний та трикуспідальний клапани. УЗД черевної порожнини діагностувало двосторонню гіперехогенну ниркову паренхіму та зміну кортикомедулярної диференціації. Це свідчило про двосторонній розлад нирок. У медичній консультації не рекомендується використовувати нестероїдні протизапальні препарати, аміноглікозиди та дозволяє уникнути гіпотонії та гіпоксії. Вводили LSPB, керований нейростимуляцією. Загальний обсяг блоку поперекового сплетення - 15 мл 0,5% бупівакаїну Загальний обсяг блоку поперекового сплетення - 10 мл 0,5% бупівакаїну. Хірургічна процедура протікала без особливих зусиль. Післяопераційне знеболення тривало 14 годин без необхідності прийому опіатів. Гемодинаміка була стабільною в періопераційному періоді.
Випадок 3
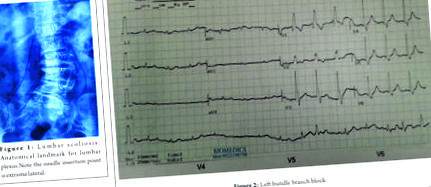
80-річну жінку з важкою бронхіальною астмою, яка не реагує на бронходилататори, стероїди та розпилення, було призначено для відкритого зменшення та фіксації міжчеревного перелому. На ЕКГ виявлено лівий пучок гілки (рис. 2). Ехокардіограф запропонував склеротичний аортальний клапан з градієнтом тиску 50 мм рт.ст., пов'язаною з цим мітральною та трикуспідальною регургітацією, ЛШДД ІІІ ступеня та ЕФ 35%. Її артеріальний тиск при вступі становив 210/100, а наступні показники - 160/94. Було проведено консультування, і вона була направлена на хірургічну процедуру під LSPB. Вводили LSPB, керований нейростимуляцією. Загальний об'єм блоку поперекового сплетення - 18 мл 0,5% бупівакаїну Загальний обсяг блоку крижового сплетення - 8 мл 0,5% бупівакаїну Фібриляція передсердь зберігалася і в періопераційному періоді, хоча гемодинаміка добре підтримувалася.
Випадок 4
92-річна жінка, як відомо, гіпертонічна, і в анамнезі вона перенесла інфаркт міокарда ще 35 років тому, страждала від міжчеревного перелому. На момент прийому її амбулаторний артеріальний тиск (АТ) становив 130/80, частота серцевих скорочень 82/хв, а насиченість киснем у повітрі становила 92%. Її обстеження серцево-судинної системи, дихальної системи та центральної нервової системи було нормальним. Комп’ютерна томографія (КТ) мозку була нормальною. Під час прийому вона отримувала ланоксин 0,25 мг на добу. ЕКГ виявила хронічну картину фібриляції передсердь, а 2D-ехокардіографія виявила ФВ 45%, ЛШДД ІІІ ступеня, помірну трикуспідальну регургітацію та РВСП 40 мм рт. Ст. (Рис. 3).
Їй перелили дві пінти еритроцитів, на яких її вміст Hb покращився до 8,8 мг/дл, а об'єм упакованих клітин (PCV) - до 24%. Її сечовина в крові становила 28 мг/дл, сироватковий креатинін 0,8 мг/дл. Вона була гіпонатріємічною з вмістом Na в сироватці 120 мг-екв/л при надходженні та гіпохлоремічною з концентрацією Cl в сироватці 87 мг-екв/л. Це було виправлено протягом 3 днів прийому 1000 мл NaCl щодня. Її про-мозковий натрійуретичний пептид знаходився на вищій стороні (583 пг/мл - норма 125 пг/мл), а показник anINR був у межах норми (1,15). Права променева артерія була канюльована для постійного контролю артеріального тиску. Пацієнт знаходився у правому боковому положенні. Була проведена нейростимуляція LSPB. Вводили LSPB, керований нейростимуляцією. Загальний обсяг блоку поперекового сплетення - 12 мл 0,5% бупівакаїну Загальний об’єм блоку крижового сплетення - 8 мл 0,5% бупівакаїну Її перевели з відділення після анестезії через 2 години уважного спостереження до хірургічного відділення інтенсивної терапії на 48 годин спостереження. Після операції у неї був епізод суправентрикулярної тахікардії, який контролювався болюсом аміодарону, після чого 2 дні інфузії аміодарону (рис. 4). Її виписали з хірургічного відділення інтенсивної терапії (SICU) на 4-й післяопераційний день із синусовим ритмом та відмовою від ліків (рис. 4).
Техніка ЛСПБ
Позиціонування пацієнта
До позиціонування вводять титрувані дози внутрішньовенно 1 мг мідазоламу та фентанілу 25–50 мкг, щоб забезпечити свідому седацію. В якості альтернативи блоку стегнового нерва з 1% ксилокаїном 10 мл вводять у положенні лежачи на спині. Пацієнти розташовані в боці операційною стороною вгору. Інтрамедулярний цвях для всіх переломів перекладачів виконують у бічному положенні наші хірурги. Зверніть увагу, що пацієнт стабілізований задньою та передньою опорою. Стегно без перелому згинається, перелом кінцівки тримається рівно і підтримується подушкою знизу. До позиціонування вводять титрувані дози внутрішньовенно 1 мг мідазоламу та фентанілу 25–50 мкг, щоб забезпечити свідому седацію. Для всіх LSPB обраний спосіб нейростимуляції. Блоки сплетення виконуються за допомогою 100-міліметрової ізольованої голки
Попереково-крижова лінія (рис. 5)
Попереково-крижова лінія (рис. 5)
Поперековий сплетення анатомічний орієнтир
Проведена міжкристальна лінія. Проводиться лінія cephalad від заднього верхнього клубового відділу хребта (PSIS). Ці лінії перетинаються в одній точці, яка є точкою введення голки для LPB.
Анатомічний орієнтир сакрального сплетення
Проведена лінія від PSIS до бульбоподібної зони (IsT). Це поділено на три частини. Точка вибирається проксимально на третину на цій лінії і є точкою введення голки для SPB. У літературі не згадується своєрідна «попереково-крижова лінія». Як показано на малюнку, точки введення голки для LPB (темно-синя стрілка) і SPB (темно-жовта стрілка) лежать на одній лінії.
PSIS: задній верхній клубовий відділ хребта.
Синя стрілка - введення голки для блоку поперекового сплетення.
Темно-жовтий - вставка голкою для блоку крижового сплетення.
Прийоми
LPB (рис. 6)
У згаданій точці вводиться 100-міліметрова стимулююча голка (перетин антікристальної лінії та лінії, проведеної через ПСІС). Голка пробивається крізь м’язи спини, поки не зустріне поперечний відросток (цей кістковий контакт має величезне значення) Наконечник голки вставляється не більше ніж на 1,5-2 см після поперечного відростка. Викликана м’язова реакція під час ЛПБ - це скорочення чотириголового м’яза при 0,4 мА. Об’єм введеного місцевого анестетика становить 20–25 мл 0,5% бупівакаїну.
Контрастне дослідження LPB (рис. 7)
Контрастне дослідження, проведене під час LSPB, коли рівень креатиніну в сироватці крові становив нижче 0,5 мг%. Контрастне поширення виявляє поширення поперекового сплетення і різко окреслює відділ, де знаходиться поперекове сплетення. У цьому контрастному дослідженні відповідь квадрицепса була отримана при 0,4 млн. Років. Контраст поширюється цефалад до рівня L2 в заочеревинній ділянці походження псоаса та початку елементів поперекового сплетення. Це близько до нейраксису. Дистально спостерігається внутрішньо-тазове поширення до нижньої межі L5. Поширення підтверджує блокаду стегнового та бічного стегнового шкірного нерва (LFCN), але блокада обтуратора сумнівна, оскільки розташування цього нерва є більш медіальним. Запропонована точка введення голки (Вінні) лежить лише поперек бічного краю контрасту. Це свідчить про необхідність невеликого медіального відхилення кінчика голки.
SPB (рис. 8)
Анатомічний орієнтир введення голки (лінія, що з’єднує PSIS та IsT, розділений на три частини, введення голки - це точка проксимальної третини і дистальних двох третин на цій лінії). Стимулююча голка вводиться перпендикулярно сідничним м’язам, і при попаданні на крижову пластинку кінчик голки не повинен знаходитися на відстані більше 1,5–2 см за крижовою пластинкою. Викликані м’язові реакції - це або підошовне згинання, або тильне згинання стопи при 0,4 мА. Об’єм введеного місцевого анестетика становить 0,5% бупівакаїну.
Контрастне дослідження SPB (рис. 9)
Контрастне дослідження, проведене під час SPB, ідентифікує внутрішньо- та поза-тазове поширення місцевого анестетика. Внутрішньо-тазове поширення блокує сідничний і пудендальний нерви, а дистальне сідничне поширення блокує задній шкірний нерв стегна і головний сідничний нерв.
Оцінку сенсорних та рухових функцій проводили, оцінюючи ділянку розрізу холодною губкою, обережним защемленням відповідної ділянки та обережним рухом переломованої кінцівки. Більше 50% спостерігалося пощадження ділянки порізу, що є предметом найбільшого занепокоєння. Пацієнти змогли рухати контралатеральну ніжку і скаржились на те, що вона холодна. Усі пацієнти були гемодинамічно стабільними при незначному падінні артеріального тиску АТ (8–10 мм рт. Ст.). У трьох пацієнтів падіння АПБ було значним (> 30 мм рт. Ст.). Це, ймовірно, передбачало епідуральне поширення і було оцінено в післяопераційному періоді. Контралатеральне розгинання кінцівок було мінімально обмеженим і підтверджувало можливе епідуральне поширення.
Обговорення
Темно-червоні стрілки - нижні полюси нирок при L2-3, але можуть поширюватися до L3-4.
Помаранчева лінія - відстань поперек остистого відростка.
Синя лінія - відстань від шкіри до поперекового сплетення.
Біла дужка - відстань від Т П до поперекового сплетення.
Зелена стрілка - вірогідне медіальне поширення в нейраксисі.
Регіональна анестезія залишається наркозом на вибір для літніх та хворих пацієнтів [57]. Таким чином, режим анестезії спеціально адаптується відповідно до вимог пацієнта на розсуд анестезіолога. Регіональна анестезія пов'язана з меншими шансами стаціонарної смертності та легеневих ускладнень серед усіх пацієнтів із переломами стегна у порівнянні із загальною анестезією. Цей висновок може бути зумовлений тенденцією до поліпшення результатів при регіональній анестезії серед пацієнтів із міжчеревними переломами [58]. Згідно з цим автором, LSPB забезпечує унікальну, односторонню та неускладнену регіонарну анестезію для пацієнтів геріатричного типу з високим ризиком, що перебувають на операціях на тазостегнових суглобах. Слід враховувати роль КЛЛ під контролем ультразвуку при болі в розрізі. Цей автор хотів би застерегти, що LPB є помірно складним у виконанні, вимагає дуже високої пильності під час введення місцевого анестезуючого засобу та суворого гемодинамічного контролю протягом хірургічного періоду. Ці автори рекомендують блок попереково-крижового сплетення як альтернативу нейраксіальним блокам при ранньому хірургічному відновленні (
- Зміни імунної системи у пацієнтів з коронавірусною хворобою-19 (CoViD-19), спричинені
- Залучення пацієнтів до харчової терапії Інститут функціональної медицини
- Вправи на захворювання коронарних артерій для здорових серцевих хворих; Сім'ї
- Чи худнуть пацієнти після тотальної ендопротезування кульшового суглоба
- Хімічний пілінг від мелазми у темношкірих пацієнтів