Фармакологічні стратегії детоксикації
Анотація
Детоксикація відноситься до безпечного припинення прийому речовини, яка перебуває в залежності, і відрізняється від профілактики рецидивів. Зазвичай дезінтоксикація триває від кількох днів до кількох тижнів, залежно від речовини, яка зловживається, тяжкості залежності та підтримки, доступної користувачеві. Психосоціальна терапія поряд із фармакологічними методами лікування є важливими для поліпшення результату. Залежності, розглянуті в цьому огляді, це детоксикація від опіоїдів (метадоном, бупренорфіном, агоністами α2-адренорецепторів та допоміжними препаратами), алкоголем (з бензодіазепінами, антиглутаматергіками та γ-аміномасляною кислотою (ГАМК) -ергічними препаратами), стимуляторами та каннабісом ( без чітких рекомендованих фармакологічних методів лікування), бензодіазепіни (із зменшенням дози) та нікотин (із замісною терапією нікотином, антидепресантами та частковими агоністами). Докази обмежені відсутністю контрольованих випробувань, достатньо надійних для оглядових органів, і потрібні додаткові дослідження оптимальних доз та режимів лікування, як окремо, так і в поєднанні.
Вступ
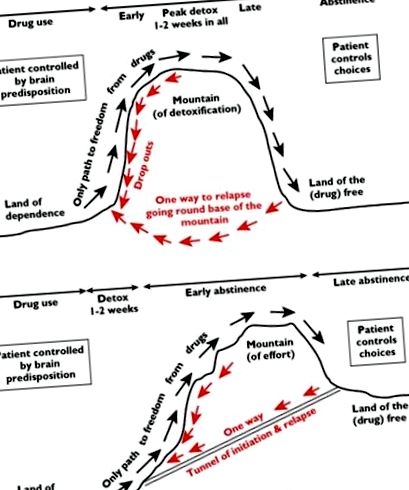
Сприйняття - це проблема. Пацієнти, їхні сім'ї та персонал часто вважають, що детоксикація є ключовим питанням, тоді як насправді це невелика частина набагато довшого шляху до утримання. Цифра складається з двох частин, підзаголовки для кожної: (А) Фантазія: Як пацієнти (та персонал) сприймають прогрес у лікуванні наркоманії. (Б) Реальність: шлях до утримання
Вибір стратегії детоксикації може залежати від багатьох факторів, включаючи клінічне судження, особисті переваги та обставини користувача, спосіб життя та очікування, ступінь залежності та супутні проблеми зі здоров’ям. Клініцистам може знадобитися пристосувати фармакологічні методи лікування, наприклад, стосовно ризику передозування, якщо дезінтоксикаційне лікування можна перенаправити на ін’єкцію, або якщо існує ризик для дітей, які проживають разом із користувачем, якщо лікування можна взяти додому. Для отримання ефективних планів лікування користувачі повинні брати участь у виборі лікування, а також, з дозволу користувача, також сім'я або опікуни.
Детоксикація від опіоїдів
Більшість користувачів повідомляють про вживання опіоїдних препаратів (в першу чергу героїну), а тих, кого вважають залежним, зазвичай переносять на заміну опіоїдів, таких як метадон або бупренорфін, щоб забезпечити стабілізацію контрольованого препарату, дози та режиму [8]. Деякі користувачі стабілізуються на діаморфіні (героїні) шляхом ін’єкцій або інтраназальної доставки. Інші опіоїди також іноді використовують, особливо модифіковані форми вивільнення морфіну, дигідрокодеїну та трамадолу. Рекомендується розпочинати дезінтоксикацію з використанням того самого препарату, що використовується для підтримання [3].
Детоксикація визначається як процес, який завершується протягом 28 днів як стаціонар, або до 12 тижнів у громаді. Деякі клініцисти повідомляють про зменшення доз протягом місяців або років, хоча це не вважається детоксикацією як такою. Calsyn та співавт. [9] виявили невеликий успіх у цьому методі, але це може бути корисним кроком на шляху до офіційної процедури детоксикації, оскільки надає користувачам певної впевненості, що вони можуть вживати менші дози свого підтримуючого препарату. Користувачів, яким не вдалося здійснити спробу детоксикації, можна знову ввести до підтримуючої терапії.
Метадон
Бупренорфін
Сублінгвальна таблетка під назвою Suboxone, затверджена в Європейському Союзі в 2006 році, являє собою комбінацію бупренорфіну та налоксону у співвідношенні 4: 1 (наприклад, 8 мг: 2 мг). При прийманні сублінгвально налоксон має низьку біодоступність і тому не має антагоністичних ефектів опіоїдів. Однак, якщо таблетку подрібнити, вколоти або пронюхати, біодоступність стає високою, а препарат вступає в дію, що призводить до симптомів відміни, які для деяких можуть перешкоджати неправильному використанню [22].
Інші опіоїди для детоксикації
Оральний морфін з повільним вивільненням (SROM) не рекомендується застосовувати як дезінтоксикаційну терапію, оскільки дослідження цієї стратегії обмежені [3]. Однак Madlung-Kratzer et al. [23] показали, що він має подібну ефективність до метадону в подвійному сліпому паралельному груповому дослідженні, що звужується протягом 16 днів, висновок, також підтверджений нещодавнім систематичним оглядом [24]. Він може підходити для користувачів, які не хочуть або не можуть переносити метадон або бупренорфін.
Лево-α-ацетилметадол (LAAM) - це синтетичний опіоїд, подібний за структурою до метадону, і може використовуватися для детоксикації подібним чином до метадону із схожими результатами [25]. Однак він також має кардіотоксичну дію, як метадон, і особливо подовжений інтервал QT [26], і мало використовується. Як і SROM, його застосовували як лікування другої лінії для користувачів, які не реагували на метадон або бупренорфін. Як і бупренорфін, період його напіввиведення досить довгий, щоб забезпечити дозування два-три рази на тиждень, а не щодня [27].
Трамадол є знеболюючим засобом з інтенсивністю морфіну в одну десяту [28] та більш сприятливим профілем побічних ефектів у порівнянні з метадоном. Він має часткову спорідненість до μ-опіоїдного рецептора, а також є інгібітором зворотного захоплення серотоніну та норадреналіну. Встановлено, що доза 600 мг на добу -1 є такою ж ефективною для обмеження симптомів відміни опіоїдів, як метадон 60 мг на добу -1, [29], і було відзначено мало клінічних відмінностей між використанням трамадолу та бупренорфіну в нещодавній ретроспективно підібраній когорті, контрольованій дослідження [30].
агоністи α2-адренорецепторів
Опіоїди пригнічують вивільнення норадреналіну, а детоксикація від опіоїдів може спричинити відскок норадреналіну. Агоністи α2-адренорецепторів, такі як лофексидин, можуть бути використані як допоміжна терапія, щоб допомогти обмежити цю «нордренергічну детоксикаційну« бурю ». Потрібне клінічне судження та ретельний моніторинг, щоб пікові ефекти агоністів α2-адренорецепторів збігалися з піковими ефектами відміни. Агоністи α2-адренорецепторів можна використовувати поряд з метадоном та бупренорфіном, але їх можна використовувати окремо для детоксикації, якщо підтримуюча терапія не потрібна, якщо користувач звернувся з проханням про детоксикацію протягом короткого періоду часу або якщо користувач має легку або невизначену залежність. Результати подібні до використання конічного метадону для детоксикації, хоча в цій групі детоксикація за допомогою агоніста α2-адренорецепторів не є такою ефективною, як детоксикація бупренорфіном [19]. Однак мета-аналіз Мідера [21] виявив, що показники завершення були подібними до бупренорфіну. Окерт та ін. [31], у дослідженні 223 користувачів, які детоксикуються від героїну, було виявлено, що агоністи α2-адренорецепторів з допоміжним речовиною трамадолом та стимулятором забезпечували кращі показники затримки в лікуванні, ніж детоксикація опіоїдами.
Лофексидин є неопіоїдним агоністом α2-адренорецепторів, ефективним для зменшення симптомів абстиненції [32], і прийом частини добової дози перед сном може бути ефективним при безсонні, пов’язаному з абстиненцією. Це ефективно для користувачів, де залежність невизначена, для молодих людей або для тих, хто має менший анамнез наркотиків. Його можна застосовувати протягом перших 7–10 днів детоксикації з початковою дозою 800 мкг на день -1 (зазвичай чотирма розділеними дозами через короткий період напіввиведення), що зростає до 2,4 мг на добу -1, а потім знову зменшується до нуль. Сам по собі він має кілька побічних ефектів, таких як сухість у роті та легка сонливість, що може призвести до седації при застосуванні з алкоголем або іншими депресантами центральної нервової системи. Були випадкові повідомлення про клінічно значущу гіпотензію та брадикардію [33] та симптоми відміни опіоїдів при зменшенні дози, які можуть бути обмежені зменшенням доз, але рекомендується щоденний моніторинг для оцінки симптомів відміни та вимірювання пульсу та артеріального тиску.
Клонідин також є агоністом α2-адренорецепторів, який застосовується з кінця 1970-х років для сприяння відмові від опіоїдів і може зменшити багато симптомів [34]. Однак такі симптоми, як тривога, неспокій, безсоння, м’язовий біль і тяга, можуть не реагувати, і це може спричинити седацію та безсоння [35]. Його зазвичай не рекомендують застосовувати NICE [3] через його наслідки гіпотонії та брадикардії, які набагато більш виражені, ніж лофексидин. Через ці проблеми його рідко рекомендують використовувати в амбулаторних умовах.
Інші допоміжні методи лікування
Налтрексон/налоксон та швидка, надшвидка та прискорена детоксикація
Детоксикація від алкоголю
Відмова від алкоголю може не вимагати фармакологічного втручання, якщо тяжкість залежності та симптоми абстиненції цього не вимагають. Однак добавки тіаміну можуть бути необхідними, щоб уникнути синдрому Верніке – Корсакова [48]. Люди з алкогольною залежністю, як правило, мають знижений рівень тіаміну у своєму раціоні, а етанол може порушити зберігання і використання тіаміну [49,50]. На додаток до методів лікування, описаних нижче, можна стверджувати, що інші препарати відіграють роль у детоксикації, такі як налтрексон, налмефен, акампросат, баклофен та дисульфірам, хоча вони більше підходять для профілактики рецидивів. Іншим методом лікування, який має потенційну роль у детоксикації алкоголю, є психотропний знеболюючий закис азоту (ПАН), який був визначений Кокрановським оглядом щодо легкої та помірної відмови від алкоголю [51]. Це може мати швидкий терапевтичний ефект при мінімальній седації.
Бензодіазепіни
Усі рекомендації, включаючи NICE [52] та два огляди Кокрана [53,54], підтримують використання бензодіазепінів, таких як хлордіазепоксид, при детоксикації від алкоголю, і це добре встановлене лікування, що зменшує тяжкість абстиненції та ризик судом та делірію. [55]. Діазепам, зокрема, може бути корисним для зменшення судом de novo, а інші корисні бензодіазепіни включають оксазепам та лоразепам. Однак бензодіазепіни можуть бути непридатними для тривалого лікування утримання через ризик їх поєднання з алкоголем. Керівні принципи Британської асоціації з психофармакології [55] попереджають, що використання селективних інгібіторів зворотного захоплення серотоніну (СІЗЗС) не рекомендується, якщо користувач також не в депресії, і його слід уникати або застосовувати з обережністю у алкоголіків типу 2 (раннє настання, позитивні сім'ї історія, імпульсивні/асоціальні риси особистості), оскільки вони можуть погіршити результати. В недавньому огляді Музик та співавт. [56] дійшов висновку, що клонідин та дексмедетомідин можуть бути корисними як допоміжна терапія до бензодіазепінів.
Антиконвульсанти/антиглутаматергіки
Акампрозат
Баклофен
Баклофен - це агоніст ГАМК, який використовується для контролю м’язових спазмів при детоксикації, оскільки ГАМК-рецептори є модуляторами дофамінергічного випалення нейронів. Показано, що він пригнічує симптоми абстиненції та тягу з ефективністю та безпекою при утриманні [74]. Він добре переноситься і може бути призначений пацієнтам із порушеннями функції печінки (отже, його застосування в печінкових центрах), де клінічно достатньо низької дози, хоча більш високі дози (наприклад, 20–30 мг тричі на день) можуть бути ефективнішими, ніж менші дози. (10 мг тричі на день). Однак деякі дослідження не виявили переваги порівняно з плацебо [75], і нещодавній огляд Кокрана поставив під сумнів його використання без подальших досліджень [76].
γ-гідроксимасляна кислота (GHB)
GHB діє на рецептори GHB і має однаковий механізм дії та подібні ефекти з баклофеном. Було показано, що він має ефективність як у відмові від алкоголю, так і у профілактиці рецидивів [77]. Зокрема, дозування у дозі 50 мг зменшує тягу ефективніше, ніж плацебо та дисульфірам, але не виявлено, що ГРБ перевершує бензодіазепіни [78]. GHB має ліцензію в деяких європейських країнах, але, на відміну від баклофену, він зростає у популярності як заборонений рекреаційний наркотик, і побоювання з приводу можливого зловживання обмежили його використання у Великобританії [78]. Наявність у твердому складі (Alcover) може зменшити проблему.
Детоксикація від стимуляторів та конопель
Досі не існує рекомендованих фармакологічних методів детоксикації від стимуляторів та конопель, незважаючи на великі дослідження. Наприклад, для лікування кокаїнової залежності обстежено понад 60 ліків [79]. Часто буває так, що досліджувані з цією метою ліки виявляються неефективними або дослідження мають неоднозначні результати.
При детоксикації конопель протисудомні засоби, такі як напівнатрієвий вальпроат [96], та антидепресанти, такі як бупропіон, флуоксетин, міртазепін та нефазадон, показали незначну користь [97–100]. Тяга зменшується, але дратівливість, тривожність і втома підвищуються. Головною проблемою відміни канабісу є труднощі зі сном, а також дослідження Вандрі та співавт. [101] показав, що це може полегшити золпідем. Дослідження римонабанту, антагоніста канабіноїдних рецепторів, було припинено через нестерпні побічні ефекти [102]. Деякі обіцянки щодо детоксикації конопель показали пероральний тетрагідроканабінол (ТГК або дронабінол) та карбонат літію. Показано, що доза 30–90 мг на день ТГК, особливо у поєднанні з лофексидином, зменшує симптоми абстиненції, проблеми зі сном, тривогу, тягу та симптоми депресії [96, 103]. Дронабінол (δ-9-тетрагідроканабінол) та карбонат літію виявилися корисними для полегшення абстиненції [104–106].
Однак щодо незаконних наркотиків, включаючи стимулятори, конопель та екстазі (МДМА), психосоціальна терапія, така як робота з ключами та управління непередбаченими ситуаціями, залишається рекомендованим лікуванням [3]. Клініцист все ще відіграє роль у моніторингу та лікуванні будь-яких проблем психічного здоров’я, включаючи психоз, депресію чи ризик самогубства. Симптоми відміни від GHB та його попередників (γ-бутиролактон, GBL та 1,4-бутандіол, 1,4-CB) можуть включати серйозні нервово-психічні проблеми та вегетативну нестабільність, що може загрожувати життю та вимагати інтенсивної терапії. Менш важкі, але постійні побічні ефекти включають безсоння, тривогу та депресію. Bell & Collins [107] повідомляють, що фармакологічні методи лікування включають використання бензодіазепінів у високих дозах (наприклад, 40–120 мг діазепаму), можливо, у поєднанні з баклофеном або іншими заспокійливими засобами, такими як пентобарбітал, якщо немає відповіді на бензодіазепіни. СІЗЗС в ідеалі слід уникати у споживачів кокаїну та амфетаміну через можливий серотоніновий синдром, хоча вони зазвичай використовуються.
Детоксикація з бензодіазепінів
Детоксикація від нікотину
Залежність від нікотину часто залишається поза увагою при детоксикації, незважаючи на те, що більшість пацієнтів палять. Послуги з лікування наркотиків не часто пропонують поради щодо відмови від куріння, можливо, через те, що вони вважають це неважливим, або, можливо, через те, що клініцисти не мають достатнього досвіду або мають побоювання, що детоксикація від куріння може перешкоджати іншим методам детоксикації. Відмова від куріння важливий з ряду причин, крім користі для здоров'я. Сигарети можуть служити підказкою для споживання інших наркотиків курінням, а відмова може допомогти в результатах лікування наркотиків, таких як подолання тяги та запобігання рецидивам. Основні методи детоксикації нікотину розглянуті нижче, але крім того, клонідин можна розглядати як лікування другого ряду. В ході досліджень було показано, що тіагабін, баклофен, габапентин, варенклін, мекаміламін (неселективний антагоніст рецепторів NAch) та топірамат мають позитивний вплив на припинення лікування. Однак налтрексон мало обіцяє [116].
Замісна терапія нікотином (NRT)
Антидепресанти
Відмова від нікотину може викликати депресивні симптоми, можливо тому, що сам нікотин може бути антидепресантом [121]. Нортриптилін, СІЗЗС (флуоксетин, пароксетин, сертралін), МАО-інгібітори, венлафаксин та звіробій - лікування другого ряду, яке може бути корисним при проблемах настрою після відмови від куріння [55]. Деякі антидепресанти можуть бути корисними через шлях їх дії, незалежно від їх антидепресантних властивостей. Наприклад, бупропіон - це нетиповий антидепресант з дофамінергічною та адренергічною дією, який також зв’язується з рецепторами NAch. Бупропіон покращує рівень відмови у порівнянні з плацебо, і було встановлено, що він зменшує тягу та задоволення від куріння [122]. Це може бути корисно для користувачів, яких турбує збільшення ваги після відмови від куріння [123]. Лікування починають за 1 тиждень до спроби припинення, починаючи з 150 мг на добу -1 протягом 3–5 днів, збільшуючи до 150 мг двічі на день, що триває протягом 7–12 тижнів. Застосування супутнього НЗТ з бупропіоном може подвоїти швидкість припинення, і це може бути розглянуто для користувачів, які намагаються вийти з НРТ самостійно [124].
Часткові агоністи нікотинових рецепторів
Часткові агоністи нікотинових рецепторів протидіють симптомам відміни нікотину (діючи як агоніст) та зменшуючи задоволення від куріння (діючи як антагоніст), і можуть бути корисними для поліпшення довгострокового припинення лікування. Вареніклін є селективним частковим агоністом для рецептора a4-b2-NAch з помірною спорідненістю до рецептора 5-гідрокситриптаміну-3. Кейхілл та ін. [125] показав, що варениклін покращує тривале припинення в 2–3 рази порівняно з плацебо або бупропіоном, і все ще був ефективним при менших дозах, що також зменшувало побічні ефекти препарату (наприклад, нудоту). Рекомендована доза становить 1 мг двічі на день протягом 12 тижнів, що досягається шляхом поступового збільшення дози з 0,5 мг один раз на день протягом тижня до початку відмови від куріння. Ще 12 тижнів дозування можна використовувати як профілактику рецидивів. Неясно, чи ці способи лікування перевершують НЗТ і чи існують необґрунтовані зв'язки між цими препаратами та депресією із суїцидальними намірами [55]. Потрібні додаткові дослідження.
Висновок
- Сік петрушки для детоксикації печінки; Очищення нирок
- Пан та пані Дієтичне харчування 6 Стратегії покупок продуктів; Поїзд
- RAFT Стратегії в класі для читання ракет
- Фармакологічне лікування розладів харчування
- ОЧИЩЕННЯ І ДЕТОКСИФІКАЦІЯ ВЕСНИ - І ПІДГОТОВКА ДО ЛІТНЬОГРЕЦЬКОЇ МЕДИЦИНИ; S БЛОГ