Дієти з виведення їжі ефективні для тривалого лікування дорослих з еозинофільним езофагітом
Резюме
Передумови
Обмежені дані описують довгострокову ефективність дієтичного виведення при еозинофільному езофагіті (EoE).
Ми оцінили довгострокові результати дієт для виведення їжі (FED) для лікування дорослих з EoE.
Методи
Ми провели ретроспективне когортне дослідження в нашому центрі, проаналізувавши всіх пацієнтів з ЕоЕ, які отримували ФЕД без супутніх стероїдів. Базові дані були зведені за допомогою стандартизованих форм збору. Дані подальшого спостереження середнього 24,9-місячного періоду були зібрані для пацієнтів з гістологічною реакцією на ФЕД під час та після повторного введення їжі. Основними результатами були симптоматичні, ендоскопічні та гістологічні відповіді.
Результати
З 52 пацієнтів 18 отримували 6FED, 32 отримували цільову дієту, а 2 отримували 6FED з цілеспрямованою елімінацією. Було 21 (40%) пацієнтів з початковою гістологічною відповіддю. Респонденти повідомили про меншу дисфагію після лікування (95% вихідного рівня проти 11%; p = 0,001) та наприкінці спостереження (95% базового рівня проти 33%; p = 0,008). Одночасно були зафіксовані значні та довговічні ендоскопічні покращення: Ендоскопічний контрольний бал: 3,2 проти 0,7; р = 0,001; та 3,2 проти 1,7; р = 0,06. Гістологічні результати покращились після найбільш обмежувальної дієти у тих, хто реагував (49,8 проти 4,1 еос/hpf; р = 0,001) і залишалися пригніченими у 10 первинних респондентів, які підтримували відповідність у кінці спостереження (5,2 еос/hpf).
Висновки
Серед пацієнтів з EoE, які реагували на FED та залишалися прихильниками, підтримуюча дієтична терапія давала тривалий довготривалий симптоматичний, ендоскопічний та гістологічний контроль захворювання. Ці довгострокові дані підтверджують, що FED є ефективним варіантом підтримуючого лікування у деяких дорослих з EoE.
Вступ
Еозинофільний езофагіт (ЕоЕ) - це хронічний імуно/опосередкований антигеном клініко-патологічний розлад, який гістологічно визначається переважаючим еозинофільним запаленням стравоходу та клінічно дисфункцією стравоходу. Діагностується, коли на біопсії стравоходу припадає щонайменше 15 еозинофілів на поле потужної потужності (eos/hpf) та після виключення альтернативної етіології еозинофілії. 1,2 ЕоЕ є основною причиною захворюваності стравоходу. 3–5 Патогенез ЕоЕ є багатофакторним, але клінічне, гістологічне та ендоскопічне покращення за допомогою дієтичних стратегій елімінації підтримує роль сенсибілізації харчового антигену в етіології розладу. 6–17
У той час як кортикостероїди покращують як клінічні, так і гістологічні особливості ЕоЕ, 18,19 є помітні показники відсутності відповіді на стероїди, можливі 20,21 побічні ефекти, 22-27 і активність захворювання ЕоЕ повторюється після відміни цих препаратів. 28,29 Навпаки, дієти для виведення їжі вирішують етіологічні фактори EoE, не мають побічних побічних ефектів, пов’язаних з прийомом ліків, і можуть призвести до тривалої ремісії. Це робить дієтичну елімінацію привабливим варіантом лікування. Однак, порівняно з дітьми, мало відомо про довгострокову ефективність цієї стратегії лікування у дорослих. 6–17
Отже, це дослідження мало на меті оцінити загальну довгострокову ефективність дієт для виведення їжі у дорослих для лікування EoE. Ми також мали на меті оцінити ефективність дієти з виведення їжі у пацієнтів, які раніше отримували лікування ЕоЕ місцевими стероїдами.
Матеріали і методи
Ми провели ретроспективне когортне дослідження в лікарнях Університету Північної Кароліни (UNC) з 2008 по 2017 рр. Інституційна оглядова комісія UNC схвалила це дослідження. Випадки EoE були діагностовані відповідно до принципів консенсусу 1,2 та визначені з бази даних клінічної патології UNC EoE. Клінікопатологічна база даних UNC EoE була раніше описана. 30 Хворих на ЕоЕ, які були включені, на момент початку дієти для виведення їжі не було 18 років, вони не застосовували одночасно специфічні для ЕоЕ препарати або протягом 6 тижнів після дієти для виведення їжі, а також мали подальші спостереження в УНК, включаючи ендоскопію з біопсією. Пацієнти з еозинофільною інфільтрацією додаткових сегментів шлунково-кишкового тракту також були виключені з цього дослідження.
Щоб допомогти виділити ефект дієти для виведення їжі, дані були абстраговані з періодів лікування, коли пацієнти отримували дієту з виведення їжі без супутніх стероїдів або терапії EoE другої лінії. Однак пацієнти, які раніше отримували кортикостероїди або терапію другої лінії, не були виключені з аналізу. Стандартна практика в UNC дозволяє щонайменше чотири тижні перервати стероїди до початку дієти для виведення їжі. Крім того, щоб мінімізувати помилкову класифікацію та упередження вимірювань, ми не аналізували інтервали лікування, коли пацієнти втрачали можливість подальшого спостереження.
Дієта для виведення їжі у меншості пацієнтів була змінена або змінена, оскільки дієта не давала гістологічної відповіді на першій ендоскопії після лікування (наприклад, додаткове цілеспрямоване усунення підозр на активацію їжі, додане до 6FED). Для цілей даної статті, у цих конкретних пацієнтів вихідні симптоматичні, ендоскопічні та гістологічні дані посилаються на дані до початку будь-якої дієти з виведення їжі. Відповіді на лікування абстрагувались після початку другої/модифікованої (або найбільш обмежувальної) дієтичної елімінаційної стратегії.
Результати
Базові характеристики
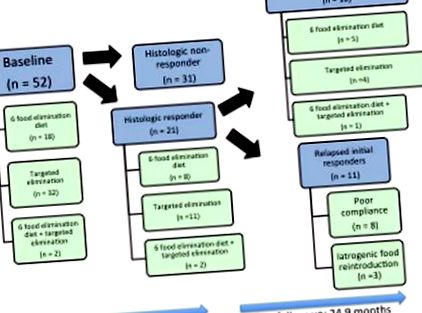
Загалом 52 пацієнти, які отримували дієту для виключення їжі, відповідали критеріям включення для аналізу в цьому дослідженні. Серед цих 52 пацієнтів 16 були включені в попередню публікацію, де детально описувались короткочасні результати дієти з виведення їжі (рис. 1). 14 Протягом усього періоду дослідження було 3 відсутні значення (відсутні 2%) для гістологічних результатів та 10 відсутніх значень (15% відсутні) для симптоматичної глобальної реакції. Приблизно у половини пацієнтів не було оцінки EREFS, розрахованої на момент початкового рівня та початкової ендоскопії після лікування. Однак лише 4 спостереження (3% відсутні) бракували для загальних ендоскопічних висновків на початковій або подальшій оцінках.
Зображення потоку пацієнтів протягом усього періоду лікування.
Середній вік на початку елімінації був 38,5 років, і більшість пацієнтів були жінки (60%) та білі (92%) (табл. 1). Офіційне тестування на харчові алергени, будь то пластир, укол або радіоалергосорбент, було проведено у 63% пацієнтів. З них 79% мали принаймні одну харчову чутливість, виявлену під час тестування. При базовій ендоскопії кільця та борозни були найпоширенішими ознаками, а середній загальний бал EREFS становив 4,1. Середній пік кількості еозинофілів до лікування дієтою, що виключає їжу, становив 60,3 еос/к.с. (табл. 1). До початку дієти з виведення їжі було 42 (81%) пацієнти, які раніше отримували кортикостероїди, які припиняли через первинну відсутність відповіді або втрату відповіді у 15 (36%), а в решті - за перевагою пацієнта (табл. 2 ). Протягом періоду спостереження пацієнти переважно продемонстрували часткове або хороше дотримання дієти з виведення їжі (94%).
Таблиця 1
Базові характеристики та клінічні дані (число = 52)
- Харчова чутливість збила вас з місця все, що вам потрібно знати про елімінаційні дієти Їжа; Вино
- Вплив форми їжі та строків прийому їжі на апетит та споживання енергії у худих молодих людей та
- Ефективне лікування; Оздоровлення для Парво у собак; Охорона здоров’я та харчування; Зневоднена собака
- Елімінаційні дієти
- Інструкції щодо елімінаційної дієти Харчова алергія та непереносимість, як робити елімінаційну дієту