JOP. Журнал підшлункової залози
Shafiq Rehman 1, Bryon C Jaques 2 *
1 Відділення гепатобіліарної та трансплантаційної хірургії, лікарня Фрімена, Ньюкасл-апон-Тайн, лікарні NHS Trust, Великобританія NE7 7DN
2 Відділення гепатобіліарної та трансплантаційної хірургії лікарні сера Чарльза Гарднера, Недлендс, Вашингтон, Австралія 6009
* Автор-кореспондент: Bryon C Jaques
Відділення гепатобіліарної та трансплантаційної хірургії
Лікарня сера Чарльза Гарднера, Недландс
WA Австралія 6009
Телефон: +61 8 9346 4055
Електронна пошта: [електронна пошта захищена]
Отримано 01 жовтня 2015 р - Прийнято 10 листопада 2015 р
Анотація
Ключові слова
Клей для фібринових тканин; Панкреатодуоденектомія
Абревіатура
Оцінка ризику свищів FRS; LOS тривалість перебування; PD панкреатодуоденектомія; Післяопераційні свищі підшлункової залози POPF; НГ ніякого клею
ВСТУП
Панкреатикодуоденектомія (ПД) - це часто виконувана хірургічна процедура при різних злоякісних та доброякісних захворюваннях підшлункової залози та периампулярної області [1]. Частота основних післяопераційних ускладнень, що повідомляються, після ПД становить від 40% до 50% [2-5]. Поганий передопераційний серцевий резерв є предиктором для тих пацієнтів, які найбільш сприйнятливі до розвитку ускладнень після БД [6]. Витік анастомозу підшлункової залози з післяопераційною фістулою підшлункової залози (POPF) є найпоширенішим ускладненням після ПД [1, 7, 8], із повідомленнями про частоту захворювання від 2% до 28% [2, 9-13]. Витоки можуть призвести до затримки спорожнення шлунка, зараження рани, панкреатиту, кровотечі, перитоніту та/або сепсису [1, 7] та смерті. За останнє десятиліття переопераційна смертність у великих спеціалізованих центрах, що виконують ПД, зросла до 0-3% [14, 15]. Огляд понад 500 пацієнтів, які перенесли ПД на злоякісні захворювання у нашому центрі, показав, що витоки підшлункової залози сприяли перипераційній смертності на 2%, але не впливали на довготривале виживання [16]. Однак, незважаючи на поліпшення смертності, при такій високій зафіксованій періопераційній захворюваності 30% - 50% [2, 9, 10], зменшення витоків підшлункової залози та свищів повинно бути важливою метою кожного хірурга підшлункової залози при виконанні PD.
Використання EVICEL ® для зменшення частоти витоків шлунково-кишкового анастомозу у великих вісцеральних хірургічних втручаннях було випробувано в нерандомізованих дослідженнях, деякі з яких мали позитивні результати [38].
Однак не існує рандомізованих досліджень з використанням EVICEL ® або інших продуктів фібринового клею як плівки між двошаровим панкреатико-ієюностомічним анастомозом після PD. Тому ми оцінили вплив місцевого фібринового клею, застосованого таким чином після панкреатикодуоденектомії, на післяопераційний свищ підшлункової залози, загальний рівень ускладнень та тривалість перебування в лікарні (LOS).
МЕТОДИ
Хірургічна техніка та післяопераційне управління
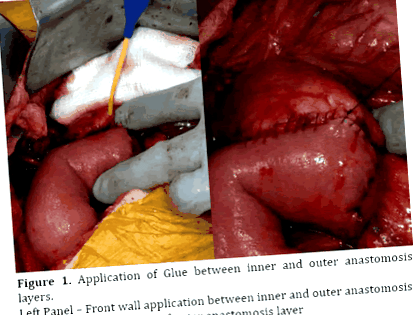
Фігура 1. Нанесення клею між внутрішнім і зовнішнім шарами анастомозу.
Ліва панель - Застосування передньої стінки між внутрішнім та зовнішнім анастомозом
Права панель - Завершення зовнішнього шару анастомозу
Усі пацієнти були схвалені амбулаторними хворими до операції. Під час кожної PD інші пацієнти отримували фібриновий клейовий герметик (EVICEL ®) зі своїм анастомозом. Пацієнтам, які отримували фібриновий клейовий герметик, місцево застосовували EVICEL ® через двоствольний шприц, підключений до Y-подібного катетера, накладеного по окружності між слизовим і серозно-м’язовим шаром тонким шаром (загалом потрібно 4-10 мл). EVICEL ® не застосовували у протоці підшлункової залози.
Три великі стовбурові хірургічні дренажі 19-Fr Blake були розміщені точно так само у кожного пацієнта. Двох розташовували так, щоб сидіти ззаду підшлунково-порожниного анастомозу, а одного - спереду від нього. Стіки з кожного стоку аналізували біохімічно на наявність амілази рідини до видалення.
Назогастральний та внутрішньошлунковий зонди видаляли, коли пацієнти переносили пероральну дієту.
Збір даних та вимірювання результатів
Всі дані були зібрані перспективно. Первинними кінцевими точками були післяопераційні фістули підшлункової залози (POPF), будь-яке ускладнення та тривалість перебування в лікарні. Післяопераційні ускладнення реєстрували відповідно до модифікованої класифікації Клавієна-Діндо, адаптованої для панкреатикодуоденектомії [23]. Фістули підшлункової залози були визначені відповідно до рекомендацій Міжнародної дослідницької групи з питань фістули підшлункової залози (ISGPF) [21] як будь-який вимірюваний об’єм рідини, що виділяється з будь-якого дренажу в післяопераційний день або після нього, коли рівень амілази втричі перевищував рівень сироватки (> 300 Од/л). Наявність збору навколошлункової залози при осьовій візуалізації з клінічною підозрою на свищ була включена в аналіз у пацієнтів, у яких були видалені дренажі. Каналізація з рідинним стоком будь-якого об'єму з високими записами амілази залишалася in-situ до тих пір, поки зареєстрований обсяг не дорівнював нулю протягом двох днів поспіль, це одного разу вимагало виписки пацієнта з амбулаторним лікуванням стоків медсестрою районної громади.
Оцінка ризику фістули
FRS, як визначено Калері та ін. [24], було незначно змінено для цього дослідження. Оцінка текстури підшлункової залози, патології та інтраопераційної крововтрати не змінювалася, проте діаметр протоки підшлункової залози, виміряний під час операції, вимірювали в 3, а не в 5 категоріях. Вважалося, що це занадто суб'єктивно, щоб диференціювати повітроводи меншого діаметру, які легко розширюються при проходженні вимірювального мікрометра. Проводи вимірювали за допомогою однієї стандартної 4-міліметрової канюлі в якості вимірювача і групували, коли вона не відповідала 5 мм (0 балів). Цей модифікований FRS визначений у Таблиця 1.
Слідувати
Після первинного спостереження між 4-6 тижнями всі пацієнти регулярно проходили належний огляд залежно від їх основного патологічного стану. Жоден пацієнт не був втрачений для подальшого спостереження.
Статистичний аналіз
Усі результати виражаються як медіана та значення діапазону. Безперервні змінні аналізували за допомогою U-критерію Манна-Уітні, тоді як категоріальні змінні аналізували за допомогою хі-квадрата та/або точного тесту Фішера. Весь статистичний аналіз проводився за допомогою програмного забезпечення SPSS для Windows (версія 21; SPSS, Inc, Чикаго, Іллінойс).
РЕЗУЛЬТАТИ
Характеристика пацієнтів
Демографічні показники пацієнтів зведені в Таблиця 2. Були проаналізовані результати 100 послідовних пацієнтів, які перенесли PD Уіппла на злоякісні та доброякісні ураження підшлункової залози з листопада 2008 по 2014 рік. П'ятдесяти пацієнтам застосовували клей EVICEL ® ((G)) між двошаровим панкреатико-ієюностомічним анастомозом і 50 - стандартний анастомоз без шару клею, без клею ((NG) група). Ці дві групи були зіставлені за віком [медіана G = 68 років (діапазон 44-84 роки) проти NG медіа N = 66, (діапазон 38-82 роки), P = 0,19] і стать [G Чоловік: Жінка 25: 25 проти НГ Чоловік: Жінка 26:24, Р = 0,84].
Післяопераційні ускладнення
Жодної групи смертності не було. Частота післяопераційних ускладнень наведена у Таблиці 3, 4. Загальні ускладнення становили N = 12 (24%) у кожній групі (P = 0,22). Значний рівень ускладнень (ступінь Клавієна 3 і вище) [G N = 4 (8%) проти NG N = 2 (4%), P = 0,40] також був подібним між двома групами. Найбільш частим післяопераційним ускладненням була післяопераційна фістула підшлункової залози [GN = 7 (14%) проти NG N = 11 (22%), P = 0,42], більшість з яких у кожній групі були біохімічними витоками підшлункової залози, які незначна і не вимагала втручання (див. нижче). Післяопераційна тривалість перебування (LOS) також була подібною [медіана G 13 днів (діапазон 11-21 день) проти медіани NG 14 днів (діапазон 9-22 дні), P = 0,90].
Важливо зазначити, що перипераційні висновки м’якої підшлункової залози у N = 32 (32%) пацієнтів (P = 0,17) або малого діаметра підшлункової залози у N = 57 (57%) пацієнтів (P = 0,92) та/або передопераційне встановлення біліарного стенту у N = 72 (72%) пацієнтів (P = 0,15) не відрізнялося між групами та не передбачало збільшення кількості післяопераційних витоків або ускладнень самостійно.
Післяопераційний підшлунковий свищ
Коли POPF траплявся в цій серії, вони були розділені на дві широкі категорії: клінічно значущі або суто біохімічні нориці та класифіковані A, B або C, як визначено ISPGF [21]. Клінічно значущі свищі визначали як витоки, при яких об’єм стоку свища перевищував 50 мл/добу та/або пацієнт мав будь-який із наступних ознак або симптомів системного розладу, таких як пірексія, підвищений вміст білих клітин, великий об’єм носогастрального стоку або біль у животі. Біохімічні нориці (ступінь А) були тимчасовими та безсимптомними, характеризувалися лише підвищеним рівнем дренажної амілази та не мали значних клінічних наслідків [21, 22]. На відміну від цього, клінічно значущі POPF (ступінь B і C) були більш хворобливими і вимагали будь-яких відхилень від нормального клінічного ведення. Свищі ступеня В включають терапевтичне лікування за допомогою антибіотиків або інфузію октреотиду із загальним парентеральним харчуванням (TPN). Свищі ступеня С визначаються як такі, що вимагають більш інвазивного втручання у вигляді оперативного втручання під загальним наркозом, черезшкірне рентгенологічне введення дренажу з поверненням до відділення інтенсивної терапії для інтенсивного лікування. Ці особливо важкі нориці в деяких випадках можуть також призвести до сепсису, недостатності органів або смерті [21].
У цьому дослідженні загальна загальна частота розвитку фістули підшлункової залози в обох групах (клей і без клею) разом становила N = 18 (18%), з них 61% (N = 11 з 18) були біохімічними витоками ступеня А ISPGF, які не потребували медичне або хірургічне лікування. Таблиця 5 узагальнює всі підшлункові свищі. Незважаючи на те, що спостерігалася тенденція до меншої кількості підшлункової залози у пацієнтів, які отримували клей EVICEL ®, післяопераційний рівень підшлункової залози не суттєво відрізнявся між групами [GN = 7 (14%) проти NG N = 11 (22%), Р = 0,42]. Використовуючи класифікацію ISPGF за ступенем тяжкості фістули підшлункової залози, у 5 пацієнтів групи G спостерігалася фістула ступеня A порівняно з 6 пацієнтами групи NG, [GN = 5 (10%) проти NG N = 6 (12%), P = 0,50 ]. Двом пацієнтам у групі G та 4 пацієнтам у групі NG потрібен Октреотид у вигляді безперервної внутрішньовенної інфузії у дозі 200 мкг/годину та TPN, призначений для контролю великих обсягів підшлункової залози підшлункової залози ISPGF ступеня B [GN = 2 (4%) проти NG N = 4 (8%), P = NS]. Одному пацієнту в групі NG потрібна була рентгенологічна вставка дренажу з поверненням до інтенсивної терапії для внутрішньочеревного збору, пов’язаного із свищем підшлункової залози ISPGF, ступінь C [GN = 0 (0%) (N = 0) проти NG N = 1 (2%), P = NS].
Коли POPF досліджували в контексті модифікованого показника ризику фістули (FRS) Таблиця 1, [24] ми виявили, що у пацієнтів з високим FRS, яким застосовували клей, спостерігалося значно менше POPF, ніж у пацієнтів групи, що не клеїть [CRF-POPF 7 балів: POPF GN = 4 з 13 (31%) проти POPF NG N = 9 з 18 (50%), P = 0,03] (Малюнок 2).
Малюнок 2. Модифікований показник ризику фістули (FRS); Фактичний відсоток POPF ставить клей проти відсутності клею. (Різниця FRS = 7 p = 0,030)
ОБГОВОРЕННЯ
Цей одноцентровий аудит був проведений для оцінки ролі клею EVICEL ® у запобіганні післяопераційним ускладненням після панкреатикодуоденектомії (PD). Було включено 100 послідовних пацієнтів, які проходили процедуру Уіппла щодо злоякісних та доброякісних уражень підшлункової залози. П’ятдесят пацієнтів, які чергувались, отримували фібриновий клей, нанесений між анастомотичними шарами у вигляді тонкої плівки під час панкреатикодуоденектомії, і порівнювали з 50 одночасними пацієнтами, яким не застосовували клей. Результати цього дослідження є сильнішими, ніж попередні аналогічні публікації, оскільки всі процедури проводились у центрі великого обсягу одним хірургом, використовуючи ту саму техніку для анастомозу, встановлення дренажу та виявлення свищів. Дві групи відповідали за віком, статтю та консистенцією підшлункової залози, і єдиною відмінністю між групами був шар фібринового клею між анастомозними шарами у половини пацієнтів. Не було виявлено суттєвої різниці між двома групами щодо загальної кількості післяопераційних витоків підшлункової залози [GN = 7 (14%) проти NG N = 11 (22%), P = 0,42] або значних показників ускладнень [GN = 2 (4%) проти NG N = 4 (8%), P = 0,40].
Слабкістю цього дослідження був метод рандомізації та малий обсяг вибірки. Оскільки ці дві групи добре узгоджувались за віком пацієнта, статтю, консистенцією текстури підшлункової залози, наявністю жовчного стенту під час операції та малим розміром протоки підшлункової залози, аудит виявив надзвичайно подібні когорти для порівняння. Це дослідження виявляється недостатньо потужним для того, щоб показати статистичні відмінності між групами в загальному ускладненні та частоті фістули підшлункової залози, що, на нашу думку, пояснюється низьким значним ускладненням та серйозними показниками свищів підшлункової залози в обох когортах. Щоб досягти статистичної значущості для загального показника POPF та рівня ускладнень, майбутні дослідження потребували б отримання даних від кількох осіб у великому підрозділі або охоплення кількох центрів, і їм потрібно було б жорстко контролювати стандартизацію роботи, розміщення стоків та виявлення фістули на посаді -операційний період, який контролювався в цьому дослідженні. Коли ризик POPF був стратифікований з використанням FRS, дослідження було достатньо потужним, показуючи перевагу клею у тих, хто має високий FRS.
Техніка нанесення фібринового клею між шарами анастомозів PD є унікальною для цього дослідження і виконується для посилення ущільнення зовнішніх анастомозів шляхом утворення міцного зв’язку фібрину між підшлунковою залозою та тонкою кишкою. Фібриновий клей не асоціювався з будь-якими несприятливими явищами у 50 пацієнтів, які його застосовували.
Оскільки більшість пацієнтів мали безперебійні операції, а ті, у кого була POPF, в основному мали місце клінічно незначні витоки, не дивно, що тривалість перебування в лікарні була майже однаковою в обох групах, і навряд чи більший обсяг дослідження виявив би відмінності в цьому результаті одноразове випробування.
ВИСНОВОК
Застосування клейового герметика було безпечним, без негативних наслідків. Ми рекомендуємо розглядати фібриновий клей у тих випадках, коли прогнозується високий рівень FRS, оскільки клей суттєво знижує рівень POPF у пацієнтів, які найбільш схильні до розвитку CR-POPF.
Конфлікт інтересів
Автори заявляють, що у цій статті немає конфлікту інтересів.
- Чи зменшує маркування дошок меню ресторанів швидкого харчування інформацією про калорії зменшення кількості придбаних калорій
- Чи зменшує передопераційне ентеральне харчування частоту хірургічних ускладнень у хворих на
- Чи зменшує молоко харчову цінність зеленого чаю за допомогою матового харбового середнього
- Чи зменшує дотримання середземноморської дієти ризик розвитку хвороби Паркінсона MDedge Neurology
- Вживання 3 плиток шоколаду на місяць може зменшити ризик серцевих захворювань - Business Insider