Асоціація режимів харчування з фосфором у сироватці крові у хворих на підтримуючий гемодіаліз: дослідження поперечного перерізу
Предмети
Анотація
Джерела дієтичного фосфату по-різному сприяють гіперфосфатемії у хворих на підтримуючому гемодіалізі (МГД). Це поперечне дослідження в Малайзії досліджувало зв'язок між режимами харчування та фосфором у сироватці крові у хворих на МГБ. Дієтичні схеми були отримані шляхом аналізу основних компонентів на основі 27 груп продуктів, що потрапили до списку 3-денних відкликань дієти 435 пацієнтів із СГД. Асоціації сироваткового фосфору досліджували з визначеними режимами харчування. Виникло три режими харчування: Домашні продукти (HFdp), Напої, підсолоджені цукром (SSBdp) та Їдять локшину (EO-Ndp). Найвищий рівень хворих у пацієнтів із СН (T3-HFdp), суттєво пов'язаний із більшим споживанням загального білка (стор = 0,002), тваринного білка (стор = 0,001) та органічного фосфату на тваринній основі (стор 2,00 ммоль/л було значно в 2,35 рази вище (стор = 0,005) з T3-SSBdp. SSBdp був пов'язаний з більшим споживанням неорганічного фосфату та вищими рівнями фосфору в сироватці крові.
Вступ
Гіперфосфатемія пов'язана зі збільшенням смертності та захворюваності хворих на підтримуючому гемодіалізі (МГД) 1,2. Висока частота гіперфосфатемії у хворих на МГД пояснюється дисбалансом між споживанням фосфату та кліренсом, оскільки діаліз залишається основним шляхом для виведення надмірного фосфату у пацієнтів з мінімальною функцією нирок 3. Тому обмеження дієтичного споживання фосфату разом із використанням фосфатних зв’язуючих є важливим аспектом терапії гіперфосфатемії 4. Однак обмеження дієтичного фосфату часто призводить до одночасного зменшення споживання продуктів, багатих білком, що ненавмисно порушує адекватність дієтичного білка, збільшуючи, таким чином, ризик втрати енергії білка 5 .
Зростає обізнаність щодо мінливості біодоступності фосфатів у раціоні як за джерелами (рослини чи тварини), так і за типом (органічні чи неорганічні). Таким чином, біодоступність є найнижчою для фосфатів, отриманих з рослин (10–30%), за ними - фосфатів, отриманих від тварин (40–60%), тоді як найвища (100%) для неорганічних фосфатів, що містяться в харчових добавках 6. Фосфат, отриманий з рослин, не легко засвоюється і не засвоюється, оскільки людині бракує необхідного ферменту фітази, щоб гідролізувати фітат для виділення фосфату. З іншого боку, неорганічні фосфати - це солі, які легко відключаються в шлунку, і в результаті> 90% поглинається 7. Виходячи з цього розуміння, сучасний підхід у навчанні пацієнтів повинен зосередитись на виборі свіжої їжі, що містить фосфати з нижчою біодоступністю, тоді як уникати харчових продуктів з фосфатсодержащими добавками 4,8. Також відомо, що потенційна взаємодія поживних речовин у травному тракті може впливати на біодоступність фосфатів у їжі 9 .
Дієтичний режим визначається кількістю, різноманітністю чи комбінацією різних продуктів харчування та напоїв у раціоні та частотою їх звичного споживання 10. Аналіз дієтичного харчування виявився цінним підходом для дослідження зв'язків між загальним харчуванням та результатами здоров'я у дослідженнях харчування людини. На відміну від підходу, що ґрунтується на поживних речовинах та продуктах харчування, підхід на основі дієти враховує, що споживання їжі людиною впадає у схеми, що відображають складну комбінацію дієтичних компонентів та поживних речовин, які можуть мати синергетичну та конкурентну взаємодію 11 .
Існує два підходи до аналізу дієтичної структури, а саме апріорі і à posteriori. Ан апріорі підхід оцінює загальну якість дієти з використанням балів або показників, заснованих на рекомендаціях щодо здорового харчування або дієт, які, як відомо, приносять користь для здоров'я, тоді як à posteriori підхід використовує статистичні методи для виявлення існуючих режимів харчування у досліджуваній популяції 12. à posteriori підхід генерує інформацію про специфічні для населення схеми харчування, що сприяє кращому розумінню результатів здоров’я, пов’язаних із місцевими релевантними режимами харчування, та розробці культурно-адаптованого втручання в харчування. Відповідно, деякі дослідження досліджували зв'язок між à posteriori отримані схеми харчування та результати, пов’язані зі здоров’ям, у пацієнтів із СХВ, такі як харчовий ризик 14 та смертність 15,16. Дослідження контрольованого годування серед популяції нехронічних захворювань нирок (ХХН) також повідомило, що біодоступність фосфатів у їжі, оцінена за допомогою екскреції фосфату з сечею, варіюється залежно від режиму харчування 17 .
Зрозуміло, що можливий зв’язок між режимами харчування та рівнем фосфору в сироватці крові у пацієнтів із МГБ залишається невідомим. Тому це дослідження мало на меті дослідити зв'язок між à posteriori похідна дієта та рівень фосфору в сироватці крові у хворих на МГБ.
Методи
Дизайн дослідження та сукупність
Це було поперечне дослідження, в якому використовувались дані, зібрані в період з жовтня 2015 р. По листопад 2018 р. Під час скринінгу пацієнтів із СХВ для рекрутингу у пальмові токотрієноли у дослідженні хронічного гемодіалізу, як описано в інших місцях 14,18. Пацієнтів набирали з 14 центрів діалізу в міській зоні долини Кланг, Малайзія. Критеріями включення були пацієнти із СХВ у віці щонайменше 18 років та діалізовані щонайменше 3 місяці. Критеріями виключення були пацієнти з поганою прихильністю до лікування гемодіалізом, непридатними для оцінки через фізичні або психічні вади, або з невиліковною хворобою, такою як ВІЛ/СНІД або злоякісна пухлина. Етичне схвалення було отримано від Комітету з медичних досліджень та етики Міністерства охорони здоров’я Малайзії (довідковий номер: NMRR-15-865-25260). Усі пацієнти, які відповідають вимогам, дали письмову інформовану згоду, і всі дослідницькі процедури проводились відповідно до відповідних рекомендацій та норм.
Змінні та збір даних
Соціально-демографічні дані пацієнтів, історія хвороби та останні рецепти ліків були отримані з медичної документації. Дотримання пацієнтами відповідності виписаним фосфатним в’яжучим речовин оцінювали за допомогою особистих інтерв’ю. Біохімічні результати були витягнуті з лабораторних звітів пацієнтів у центрі, що мали значення протягом 2 тижнів після збору інформації про дієту. Всі аналізи проводились акредитованими лабораторіями 19 відповідно до робочих процедур, передбачених Міністерством охорони здоров'я, Малайзія.
Дієтичну оцінку проводили дослідники-дієтологи з використанням методу 3-денного відкликання дієти (3-DDR), який включав день діалізу, день недіалізу та день вихідних 20. Для оптимізації оцінки розміру порції використовували звичайні побутові вимірювальні інструменти (миски, ложки та склянки). Крім того, пацієнтів запитували про їхню щотижневу частоту прийому їжі на вулиці. Їжа та напої, що споживаються в побутових одиницях, перетворювались на абсолютну масу (г) та об’єм (мл) перед аналізом складу поживних речовин за допомогою програмного забезпечення Nutritionist Pro (First DataBank Inc., США), яке посилається на Малайзійський харчовий склад 21 та Сінгапурський харчовий склад 22 бази даних. Індекс Гольдберга був використаний для ідентифікації 3DDR прийнятних репортерів для забезпечення якості дієтичних даних. Коротше кажучи, базальний рівень метаболізму (BMR) пацієнтів оцінювали за допомогою рівняння Гарріса-Бенедикта 23. Виходячи з повідомленого споживання енергії (EI), співвідношення EI: BMR 2,4 вважалося недооцінками, прийнятними та надмірними звітами 3DDR відповідно 24 .
Продукти харчування з 3DDR класифікувались за категоріями білків тваринного або рослинного походження 25. Групу тваринних білків складали такі продукти харчування: риба, молюски, яйця, птиця, червоне м’ясо, молоко, молочні продукти, м’ясо, оброблене або консервоване, морепродукти та яйця. Джерелами їжі рослинної білкової групи були рис, крупи, боби, бобові, фрукти, листові овочі та крохмалисті овочі. Окремий продукт харчування був безпосередньо віднесений до відповідної групи продуктів харчування. Для приготованих страв із сумішшю інгредієнтів, що складаються з білків тваринного та рослинного походження, посилання на рецепти Малайзійської харчової композиції 21 визначали вміст білка в кожному інгредієнті, який потім було віднесено до відповідної білкової групи.
Оскільки метод 3DDR був обраний для оцінки споживання дієти замість опитувальника частоти їжі, спочатку агрегування продуктів харчування за групами продуктів харчування було здійснено, як було описано раніше 14, перед проведенням аналізу дієтичної структури. Усі продукти харчування з 3DDR були вилучені та відсортовані за алфавітом. Потім дублікати видаляли, а продукти харчування групували на основі подібності, способу приготування їжі та вмісту поживних речовин. Спочатку було розроблено 47 груп продуктів, а потім, виходячи із споживання кожної групи продуктів, групи продуктів, які споживали менше 5% пацієнтів, або були виключені, або згорнуті з подібними групами продуктів харчування. Це сузило остаточний перелік продуктів харчування до 27 груп продуктів.
Індекс дієтологічної одноманітності (DMI) розраховували, як описано Zimmerer et al. 27 для оцінки різноманітності продуктів харчування. З розробленого списку груп з 27 продуктів харчування загальна кількість кожної спожитої групи продуктів харчування була перетворена на порції відповідно до Малайзійських дієтичних рекомендацій 2010 28. Дієта, що споживається з різноманітними групами продуктів харчування, призвела до менших пропорцій загальної порції для кожної групи продуктів, і було отримано менше значення індексу, або навпаки.
Статистичний аналіз
Односторонній ANOVA був використаний для порівняння споживання поживних речовин у тертилів ідентифікованих режимів харчування, з тестом Бонферроні на post hoc аналізи. Крускал – Уолліс з Данном post hoc тест був використаний для порівняння ненормально розподілених змінних. Односторонній аналіз коваріації, скоригований для коваріатів, використовували для порівняння фосфору в сироватці крові по третинам кожного режиму харчування, а тест Бонферроні використовували для множинних порівнянь. Для оцінки коефіцієнтів шансів (ОР) гіперфосфатемії (фосфор у сироватці крові вище 1,78 ммоль/л та 2,00 ммоль/л), пов'язаних із Т3, використовувались численні логістичні регресії. Дані про відсутність коваріантних даних (менше 2%) були зараховані з використанням середнього значення існуючого значення всіх пацієнтів. Всі аналізи були обчислені за допомогою SPSS версії 25 (IBM, Чикаго, Іллінойс, США). Статистичне значення було встановлене стор-значення
Результати
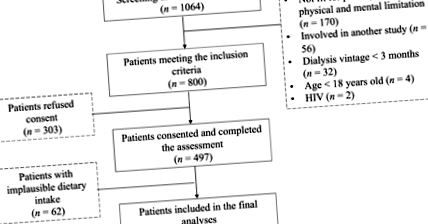
Вивчіть блок-схему набору пацієнтів.
Виникло три режими харчування з 27 групами продуктів харчування, що застосовували PCA (табл. 2). Значення PCA Кайзера – Мейєра – Олкіна становило 0,538, що вказує на прийнятну достатність вибірки для факторного аналізу. Перший режим харчування був позначений як “Home FoodDP”, оскільки він представляв велике споживання білого рису, некрохмалистих овочів, риби та молюсків, птиці, свинини, рафінованого хліба, булочки, булочки та бісквітів, свіжих та сухофруктів та соєвий сир та бобові, разом із низьким споживанням смаженого рису та кокосового молока (рис. 2). Другий режим харчування був позначений як “Локшина, що їсть їжу”, оскільки він відображав велике споживання смажених страв з локшини, пау, неясна сума і Йонг Тау Фу, і перероблених рибних продуктів, разом з низьким споживанням смаженого рису та насі лемак. Третій режим харчування характеризувався високим споживанням підсолоджуваних цукром напоїв, разом із цукерками та чіпсами, яловичиною, вишуканою традиційною крупою, птицею, рафінованим хлібом, булочкою, булочкою та бісквітом, смаженим рисом та насі лемак. Цей шаблон був позначений як “Підсолоджені цукром напоїDP (SSBDP)”. Ці три режими харчування пояснювали 72,1% від загальної дисперсії серед 27 груп продуктів, причому найвищі відхилення становили SSBDP (45,3%), за ними йшли Food FoodDP (13,8%) та моделі з їжею локшиниDP (13,0%).
Групи продуктів з коефіцієнтом навантаження в межах кожного режиму харчування. Коефіцієнт навантаження вказує на кореляцію групи продуктів харчування з дієтою. Місцеві назви продуктів харчування на етнічній основі Куїх- місцеві солодкі або солоні закуски на розмір; Пау—Наповнений паровий булочка; Невиразна сума— Вареник розміром з укус, наповнений м’ясом або морепродуктами; Йонг Тау Ху—Соєвий сир або овочі, наповнені рибною пастою або меленим м’ясом; Насі Лемак—рис, зварений на кокосовому молоці.
Лінійний регресійний аналіз сироваткового фосфору наведено в таблиці 3. У моделі, що враховує всі змінні, адекватність діалізу (Kt/V, β = - 0,223, стор = 0,001), прилипання до фосфатних сполучних (β = - 0,184, стор Таблиця 3 Фактори, пов'язані з рівнем фосфатів у сироватці крові за допомогою лінійного регресійного аналізу.
Профілі поживних речовин трьох ідентифікованих режимів харчування представлені в таблиці 4. Верхній терцій (Т3) Home FoodDP вказував на значно більший прийом загального білка (стор = 0,002), тваринного білка (стор = 0,001), органічний фосфат на тваринній основі (стор Таблиця 4 Порівняння дієтичних показників між третинами для кожного режиму харчування.
Рівень фосфору в сироватці крові по тертилам для кожної дієтичної схеми представлений у таблиці 5. Після коригування конфігураторів, рівень фосфору в сироватці крові виявився значно вищим для Т3 проти Т1 ССДПП (стор = 0,006). Хоча жоден Т3 будь-якої дієтичної картини суттєво не асоціювався з вищим АБО для рівня фосфору в сироватці> 1,78 ммоль/л (стор > 0,05), все ще незначна тенденція (стор = 0,067) спостерігався при SSBDP (АБО = 1,64; 95% ДІ 0,97, 2,79), що можна вважати значущим для стор значення 2,00 ммоль/л, поріг, який є клінічно значущим, значно збільшився у 2,35 рази (95% ДІ 1,30, 4,28, стор = 0,005) з Т3 SSBDP. Кава або чай, доданий з цукром, був найпоширенішим SSB (39,0%), який споживають пацієнти при Т3 SSBDP, потім кава або чай, додані зі згущеним молоком або випареним молоком (24,3%), і сироп, або напої з сердечного або тетрапаку (13,3 %) (Рис. 3).
Види напоїв, які вживають 3 пацієнти (2)n = 145) в межах дієтичного режиму цукрових підсолоджуваних напоїв.
Всього було виявлено 105 пацієнтів з Т3 Home FoodDP та 101 пацієнт з Т3 SSBDP та проведено порівняння між цими двома групами (табл. 6). Пацієнти Т3 з ПСДП були молодшими (стор = 0,001); переважно чоловіки (стор = 0,037) та ймовірних малайських пацієнтів (стор Таблиця 6 Порівняння характеристик дієтичних показників між пацієнтами 3-ї категорії домашньої їжі та напоями, підсолодженими цукром.
Обговорення
У цьому дослідженні висвітлено потенційне застосування підходу до дієтичного режиму в дієтологічних втручаннях для пацієнтів із СХВ. Дієтичний підхід враховує багатовимірну експозицію та взаємодії, що існують у складних комбінаціях дієтичних компонентів та поживних речовин з харчових продуктів 12. Оскільки люди споживають їжу замість поживних речовин окремо, дієтичні схеми можна легко перетворити на практичні дієтичні поради. Тим не менше, ми не можемо спростувати важливість визнання та обмеження споживання неорганічних фосфатів. Ми чітко показали, що режим харчування, що містить напої, багаті неорганічним фосфатом, асоціювався з гіперфосфатемією у цієї популяції в Малайзії, і цей аспект слід враховувати в навчанні пацієнтів, а також включати до місцевих рекомендацій клінічної практики 8. У той же час критично важливо також підкреслити для пацієнтів цінність збалансованого харчування.
На закінчення слід зазначити, що SSBDP асоціюється з більш високими концентраціями фосфору в сироватці крові у пацієнтів з МГБ, можливо, через більший прийом неорганічного фосфату. Home FoodDP асоціювався з більшою кількістю споживання білка, але не був пов’язаний з рівнем фосфору в сироватці крові. Отже, оцінка звичного режиму харчування може надати цінну інформацію щодо дієтичного лікування гіперфосфатемії у хворих на МГД. Майбутні дослідження, що вивчають ефективність дієтичного втручання при гіперфосфатемії у хворих на МГБ, є виправданими.
- Оцінка впливу підвищеного споживання харчових волокон на функцію кишечника у хворих на
- Асоціація вживання алкоголю з поширеністю жирової печінки після адаптації до дієти
- Асоціація ожиріння з хронічними захворюваннями нирок у пацієнтів літнього віку з неалкогольною жировою кліткою
- Споживання алкоголю та дієтичні схеми Дослідження FinDrink
- Зміни специфічних для їжі титрів сироватки IgG4 до загальних харчових антигенів у пацієнтів із дратівливою реакцією