Ароматаза, рак молочної залози та ожиріння: складна взаємодія
Анотація
Ожиріння асоціюється з аномально високою експресією ферменту ароматази в молочній залозі, збільшенням місцевого вироблення естрогену та схильністю до гіперплазії молочної залози та раку. Підвищене ожиріння у жінок у постменопаузі може спричинити сигнальні шляхи, що індукують експресію ароматази. У жирових фібробластах молочної залози підвищена продукція TNF може індукувати дистальний промотор ароматази, тоді як посилена локальна продукція PGE2 може викликати проксимальну промоторну область. Тут ми розглядаємо механізми, які контролюють експресію гена ароматази в жировій тканині молочної залози, і паракринні взаємодії між злоякісними клітинами епітелію молочної залози та оточуючими жировими фібробластами. Систематична характеристика цих сигнальних шляхів полегшить ідентифікацію потенційних цілей лікарського засобу для вибіркового зменшення експресії ароматази та надмірного вироблення естрогену з терапевтичною перевагою.
Взаємозв’язок ожиріння та естрогену
У грудній клітці доброякісні або злоякісні епітеліальні клітини контактують з вистиланими клітинами ендотелію капілярами, недиференційованими жировими фібробластами, які також відомі як преадипоцити, та наповненими ліпідами зрілими адипоцитами [17]. Ароматаза, яка є членом надродини цитохрому Р450, є ферментом, відповідальним за ключові етапи синтезу естрогенів [9]. Ароматаза експресується в декількох тканинах, включаючи недиференційовані жирові фібробласти та пухлини молочної залози, але не експресується у зрілих адипоцитах [9,18]. Значно збільшена маса жирової тканини молочної залози у жінок з ожирінням може локально збільшити вироблення естрогену в грудях просто через більшу кількість фібробластів, що експресують аромат-тазу [9]. На додаток до цього ефекту маси, експресія ароматази на одиницю жирової тканини або клітини може також збільшуватися із збільшенням ваги.
Естроген, продукт ферменту ароматази в жировій тканині, давно підозрювали як гормон, відповідальний за збільшення ризику раку молочної залози у жінок із ожирінням у постменопаузі. Насправді, найефективнішим гормональним лікуванням раку молочної залози в постменопаузі було використання інгібіторів арома-тази, які блокують активність ароматази в молочній залозі та на периферії, тим самим зменшуючи кількість місцевого вироблення естрогену - що, в свою чергу, допомагає придушити рецидив захворювання. тканини пухлини молочної залози [19]. Ключовим та невирішеним питанням був відносний внесок жирової тканини молочної залози порівняно з підшкірною жировою клітковиною в інших ділянках тіла в утворення естрогену, який сприяє збільшенню ризику та росту раку молочної залози. Епідеміологічні дослідження показали, що незначно підвищений рівень естрогену у венозній крові може пояснювати частину зв'язку між ожирінням та частотою раку молочної залози [20]. Однак нещодавно проведене рандомізоване дослідження "Жіноче здоров'я", яке продемонструвало можливе зниження ризику раку молочної залози у жінок в постменопаузі, яким вводили естроген-замінюючий гормон, поставило під сумнів роль м'яко підвищеного рівня циркулюючого естрогену у ризику раку молочної залози [15,16].
Механізми надмірної експресії ароматази при естроген-реагуючому раку молочної залози
Окремий ген кодує ароматазу, ключовий фермент для біосинтезу естрогену, пригнічення якого ефективно виключає вироблення естрогену. Сьогодні інгібітори ароматази є найефективнішими ендокринними методами лікування раку молочної залози, що реагує на естро-ксген [28]. Кілька випадкових рандомізованих клінічних досліджень, опублікованих з 2000 р., Продемонстрували перевагу інгібіторів ароматази над антагоністом естрадіолу тамоксифеном у лікуванні раку молочної залози [19,29–35]. Таким чином, пригнічення утворення естрогену терапевтично ефективніше, ніж блокування його дії. Яєчники, яєчка, жирова тканина, шкіра, гіпоталамус і плацента - все це виражає ароматазу, фізіологічно [36]. На відміну від цього, жирова тканина молочної залози, що має пухлину, надмірно експресує ароматазу, що призводить до місцевого перевиробництва естрогену, який надає паракринну та внутрішньокринну пухлинні ефекти [36]. Хоча подібні промоторні ділянки ароматази можуть активуватися в нормальних та патологічних тканинах, клітинні та транскрипційні регуляторні механізми надзвичайно різноманітні та специфічні для клітин [9,37]. Це призвело до детального дослідження механізмів, що зумовлюють надмірну експресію ароматази в кожній тканині, намагаючись визначити конкретні молекулярні мішені для розробки нових терапевтичних засобів [9,38].
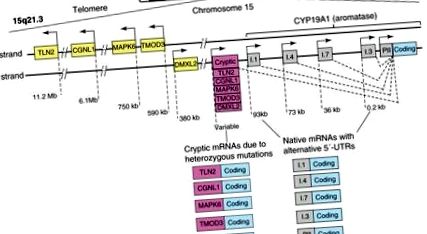
В якості альтернативи використовуються промотори, розподілені в межах 93 кб регуляторної області вище від загальної кодуючої області, по-різному контролюють експресію ароматази в гонадах, жировій тканині, кістках, мозку, шкірі, печінці плода та плаценті [39]. На даний момент у людини знайдено десять альтернативних промоторів, включаючи I.1, I.2 в плаценті, I.4 в жировій тканині та шкірі, I.5 в тканинах плода, якщо в мозку, I.7 в ендотеліальних клітинах, I.6 у кістці, I.3 у жировій тканині та PII у статевих залозах (рис. 1) [9]. Певний набір факторів транскрипції регулює кожен промотор в залежності від сигнального шляху та тканини.
Структура гена CYP19A1. Ген людини CYP19A1 (ароматаза) транскрибується у напрямку від теломери до центромери хромосоми 15 і містить приблизно 10 альтернативно використовуваних природних промоторів, які регулюють його експресію частково тканинно специфічно. Активація кожного промотору транскрибується на видах мРНК, що містить певну 5'-нетранслируемую область (5'-UTR), яка служить сигнатурою цього конкретного промотору. П'ять інших генів (TLN2, CGNL1, MAPK6, TMOD3 та DMXL2), згруповані в тандемі, лежать поруч з ароматазою в її теломерному аспекті. Гетерозиготні інверсії або делеції змінюють напрямок промоторів цих генів та їх 5′-UTR і переміщують їх вище за течією гена ароматази. Потім ці криптичні промотори неадекватно надмірно експресують ароматазу в багатьох тканинах людини і викликають надлишок естрогену. Найбільш поширеним проявом є жіноче розростання тканини молочної залози у хлопчиків (передпубертатна гінекомастія) (див. [40] для більш детальної інформації).
Фолікулостимулюючий гормон (FSH) індукує найбільш проксимальний промотор PII через cAMP-залежний шлях, що включає рекрутинг стероїдогенного фактора-1 та β-катеніну в клітинах гранульози яєчників людини [41]. Як буде детально описано пізніше, PGE2 через цАМФ координує індукцію проксимального кластеру промоторів PII та I.3, які лежать у межах приблизно 0,2 кб послідовності, шляхом рекрутингу CCAAT/енхансер-зв'язуючого білка-β (C/EBPβ), JunD та печінки рецепторний гомолог-1 (LRH-1) у жирових фібробластах молочної залози людини [9,42]. Навпаки, промотор I.4, який лежить приблизно на 73 кб вище від кодуючої області, індукується глюкокортикоїдами та цитокінами інтерлейкіну -6 або -11 та TNF. Це призводить до активації c-Jun N-кінцевої кінази (JNK), що активує кіназу-1 (Jak1), та до рекрутингу перетворювача сигналу та активатора транскрипції-3 (STAT3), до спільного з глюкокортикоїдним рецептором (GR), в жирові фібробласти людини [9]. У вільній від раку тканині молочної залози жирові фібро-бласти експресують низький рівень ароматази через промотор I.4, тоді як область промотора I.3/II, яка зайнята транскрипційними репресорами, залишається спокійною [43,44].
Різні клітинні та молекулярні механізми відповідають за експресію ароматази при раку молочної залози проти тканин молочної залози, що не містять захворювань [9]. По-перше, клітинний склад змінюється при раку молочної залози таким чином, що недиференційовані жирові фібробласти, що експресують ароматазу, накопичуються навколо злоякісних клітин епітелію. По-друге, молекулярні зміни в жирових стромальних клітинах сприяють зв’язуванню підсилювачів транскрипції проти інгібіторів із нормально спокійною промотором ароматази I.3/II. Робота кількох лабораторних лабораторій показала, що ці два механізми підтримують місцеву надлишкову експресію ароматази при раку молочної залози та кількість підрахунку більшості експресії ароматази при раку молочної залози [24,45,46]. Описано третій механізм, який включає підвищену активність дистальних промоторних областей, таких як I.4 та I.7, і це також сприяє надмірній експресії ароматази в пухлинах молочної залози (рис. 1) [47,48]. Нарешті, гетерозиготні мутації, які призводять до того, що область кодування ароматази лежить поруч з конститутивно активними криптичними промоторами, які зазвичай транскрибують інші гени, можуть враховувати надмірну експресію ароматази в грудях та інших тканинах та надмірне утворення естрогену (рис. 1) [49]. . Клінічне значення цього механізму у розвитку раку поки не відоме.
Утворення естрогену при раку молочної залози
Біологічно активним естрогеном є естрадіол. Ароматаза каталізує перетворення андростендіону в естрон або тестостерону в естрадіол. Оскільки основним циркулюючим стероїдом у жінок у постменопаузі є андростен-діон, для утворення естрадіолу необхідні відновлювальні ферменти. Ферменти 17β-гідроксистероїддегідрогенази типу 1 (HSD17B1) та альдо-кеторедуктази сімейства 1, член С3 (AKR1C3), які можуть перетворювати естрон у естрадіол, а ан-дростендіон у тестостерон, відповідно, присутні в різних типах клітин злоякісних та доброякісних тканини молочної залози та доповнюють активність ароматази для утворення естрадіолу з циркулюючого андростендіону (рис. 2) [58,59].
Клітинна локалізація ароматази при раку молочної залози
Приблизно 90% активності ферменту ароматази та мРНК у жировій тканині молочної залози виявляється в недиференційованих фібробластах, а не в зрілих адипоцитах [60] (рис. 2). Імунореактивна ароматаза локалізована як у злоякісних епітеліальних клітинах, так і в оточуючих фібробластах в тканинах пухлини молочної залози [61–63]. Проте біологічна значимість імунореактивної ароматази, виявленої різними антиболами, залишалася дискусійною [64]. Помітно високі рівні активності ферменту ароматази та експресії генів за допомогою активації промотору I.3/II постійно виявляються в жировій тканині молочної залози або фібробластах, щойно виділених із тканини молочної залози, з раком або без нього [24,60,65]. Активність ферменту ароматази в первинних злоякісних епітеліальних клітинах молочної залози або клітинних лініях, навпаки, була або не виявлена, або надзвичайно низька [66] (рис. 2).
Щільний шар недиференційованих жирових фібробластів (десмопластична реакція), що оточує злоякісні епітеліальні клітини, є важливим для структурної та біохімічної підтримки росту пухлини [67]. Злоякісні епітеліальні клітини секретують велику кількість антиадипогенних цитокінів TNF та IL-11, які пригнічують диференціювання фібробластів до зрілих адипоцитів, головним чином, шляхом придушення адипогенних факторів транскрипції C/EBPα та активованого рецептором-γ проліфератора пероксисоми (PPARγ ) (Малюнок 2). Таким чином, велика кількість жирових фібробластів, що продукують естроген, зберігається проксимально до злоякісних клітин [43,68] (рис. 2).
Сигнальні шляхи, що регулюють промоторну область I.3/II у фібробластах пухлини молочної залози
Для вивчення потенційних механізмів блокування активності ароматази та вироблення естрогену в жирових фібробластах молочної залози, що оточують злоякісні епітеліальні клітини, систематично досліджені нижчі ефекти ефекту шляху PGE2 – cAMP – PKA/PKC [27]. Ці зусилля допомогли визначити сигнальні компоненти, які зв'язують фактори транскрипції, пов'язані з туморогенним промотором I.3/II області гена ароматази. Дослідження жирових фібробластів вказували на залучення двох специфічних кінцевих MAP-кіназ: JNK та p38 (рис. 3) [27]. Детальна дисекція цього шляху показала, що лікування PGE2 жировими фібробластами молочної залози активувало як PKA, так і PKC та їхні ефективні ефекти, JNK та p38, які в сукупності були необхідними для продукування естрогенів, опосередкованого через промоторну область I.3/II гена ароматази. [27]. Ці дослідження підкреслили роль цих кінцевих MAP-кіназ у активації експресії гена арома-тази та вказали на можливість використання JNK та p38 як потенційних нових мішеней для лікарської тканини для специфічної абляції експресії ароматази тканин молочної залози.
Транскрипційні комплекси, які регулюють промоторну область I.3/II у фібробластах пухлини молочної залози
Промотори I.3 і II розташовані приблизно на відстані 0,2 кб один від одного і мають декілька цис-діючих елементів, необхідних для активації промоутера, включаючи напівмісце ядерного рецептора, сайти зв'язування C/EBPβ, сайти зв'язування AP-1 та cAMP- елементи відповіді (CRE) (Рисунок 3) [43,44]. Повідомляється про велику кількість факторів транскрипції, які потенційно можуть регулювати цю складну область. Однак дуже мало з них, як було продемонстровано, виконують функціональну роль у жирових фібробластах людини. У цьому огляді ми зосереджуємось на підсилювачах транскрипції, які були охарактеризовані за допомогою методів in situ, таких як імунопреципітаційна ПЛР хроматину, або було показано, що регулюють активність мРНК або ензиму ароматази за допомогою методів збиття на основі siRNA в первинних жирових фібробластах людини. Ці фактори обмежені C/EBPβ, CREB-зв’язуючим білком (CBP), печінковим рецептором-гомологом 1 (LRH-1), JunB та JunD [42,44,72–79].
Було показано, що інкубація жирових фібробластів молочної залози із середовищем, кондиційованим злоякісними епітеліальними клітинами, або з PGE2 призводить до рекрутування стимулюючого транскрипційного комплексу, що включає C/EBPβ, CBP, JunB, JunD та LRH-1, до промотора ароматази I. 3/II регіон [44,72–79] (Малюнок 3). Таким чином, у недиференційованих жирових фібробластів у пухлинах молочної залози проксимально скупчені промотори ароматази I.3/II координуються за допомогою механізмів, залежних від PKA- та PKC (рис. 3). Як зазначалося вище, ці промотори зазвичай перебувають у спокої у фібробластах нормальної тканини молочної залози через зв'язування інгібуючого транскрипційний комплекс. Однак у злоякісному середовищі молочної залози промоторна область I.3/II зайнята кількома підсилювачами транскрипції в результаті активації множинних сигнальних шляхів, які в кінцевому підсумку збільшують експресію аро-матази у фібробластах молочної залози [43,44] (Рисунок 3 ).
Орієнтація на промотор ароматази I.3/II як терапевтичну стратегію
Заключні зауваження
Подяка
Наша робота підтримується грантами Національного інституту раку (CA67167), Фонду Ейвона та Фонду Лінн Сейдж.
- Рак молочної залози вражає і чоловіків. Зверніть увагу на наявність будь-якої шишки в пахві, на шиї; люди з діабетом, ожирінням
- Рак молочної залози Ожиріння може перешкоджати деяким методам лікування
- Анотація P4-10-15 Ожиріння впливає на характер раку молочної залози у жінок в постменопаузі
- Акупунктура та психотерапія в комплексному лікуванні ожиріння Медична акупунктура
- AEG-1MTDHLYRIC - проміксуальний білковий партнер, критично важливий при раку, ожирінні та захворюваннях ЦНС - PubMed