Венозна тромбоемболія та гіпергомоцистеїнемія як перший прояв перніціозної анемії: серія випадків
Анотація
Передумови
Підозрюється, що гіпергомоцистеїнемія сприяє тромбозу. Декілька досліджень випадків контролю та навіть мета-аналіз підтвердили зв'язок між венозним тромбозом та гіпергомоцистеїнемією. Гомоцистеїн обумовлений генетичними та набутими факторами (погана дієта фолієвої кислоти та вітаміну В12, старший вік, порушення функції нирок, захворювання щитовидної залози та злоякісні пухлини), спричинені прийомом та концентрацією вітаміну В9 або В12 у більшості випадків.
Презентація справ
Ми повідомляємо про випадки чотирьох марокканських пацієнтів із гострим тромбозом вен на різних ділянках: 34-річного чоловіка, 60-річного чоловіка, 58-річного чоловіка та 47-річної жінки . У всіх пацієнтів був низький рівень кобаламіну з вираженою гіпергомоцистеїнемією з нормальним вмістом фолієвої кислоти в сироватці крові та червоних клітин. Венозний тромбоз виявив перніціозну анемію у всіх пацієнтів. Низький рівень кобаламіну, атрофічний гастрит та позитивні результати щодо антитіл до парієтальних клітин шлунка підтвердили діагноз перніціозної анемії. Не було жодних доказів іммобілізації, недавньої операції, злоякісної пухлини, антифосфоліпідних антитіл, мієлопроліферативного розладу або замісної гормональної терапії. Не виявлено дефіциту білка С та білка S; вони мали нормальну функцію антитромбіну III та фактор V Лейдена; мутацій генів протромбіну не виявлено. Лікування включало пероральну антикоагуляційну терапію та добавки кобаламіну. Результат був сприятливим у всіх випадках.
Висновки
Ці звіти демонструють, що пернициозна анемія сама по собі може призвести до гіпергомоцистеїнемії, яка є досить значною, щоб призвести до тромбозу. Розуміння молекулярного патогенезу розвитку тромбозів у пацієнтів з гіпергомоцистеїнемією, пов’язаною з хворобою Бірмера, допомогло б нам виявити пацієнтів із групи ризику та відповідно їх лікувати. Коротко оглядається література, що стосується взаємозв'язку між гомоцистеїном та венозним тромбозом.
Передумови
Гомоцистеїн - це амінокислота, що утворюється внаслідок внутрішньоклітинного деметилювання метіоніну. Гіпергомоцистеїнемія характеризується підвищенням рівня гомоцистеїну в сироватці крові. Вважається, що це модифікуваний фактор ризику інфаркту міокарда, тромбозу периферичних артерій, а також тромбозу глибоких вен та легеневої емболії [1,2,3]. Більшість повідомлень, пов’язаних із захворюваннями артерій, описують асоціацію із незначно підвищеним рівнем гомоцистеїну. Натомість існують обмежені та суперечливі публікації, пов’язані з тромбозом венозної системи, пов’язаним із рівнем гомоцистеїну [4,5,6,7,8].
Гіпергомоцистеїнемія може бути наслідком генетичних дефектів ферментів, що беруть участь в метаболізмі гомоцистеїну: цистатіонін-β-синтази (CBS), метіонін-синтази (MS) і N5, N10-метилентетрагідрофолат-редуктази (MTHFR) або дефіциту ферментів кофакторів (вітамін B6, вітамін В6, або косубстрат вітаміну В9) [5].
Однак найпоширенішою причиною дефіциту вітаміну В12 при гіпергомоцистеїнемії є пернициозна анемія. Пернициозна анемія зазвичай діагностується за наявності мегалобластної анемії, неврологічних симптомів або атрофічного гастриту. Повідомлялося, що тромботичні події є виявляючим симптомом [9,10,11,12,13,14,15,16]. Ми повідомили про чотири випадки венозного тромбозу, що виявляє згубну анемію.
Презентація справи
Випадок 1
Випадок 2
Раніше здоровий 60-річний марокканець без жодної історії хвороби звернувся до нашої лікарні з анемією та глибоким венозним тромбозом правої ноги. Фізичний огляд показав блідість і набряк правої ноги з ознаками флебіту. УЗД виявило тромбофлебіт правої клубово-стегнової та підколінної вен. Рівень його гемоглобіну становив 9,5 г/дл, а середній корпускулярний об’єм - 111 мкм 3. Рівень його гомоцистеїну в плазмі становив 125 мкмоль/л (норма 120). Рівень його фолієвої плазми знаходився в межах норми. Аспірація кісткового мозку при біопсії показала мегалобластоз. Антитіла до внутрішнього фактора були позитивними; ендоскопія виявила атрофічний гастрит. Жодної іншої аномалії на більш детальному екрані для виявлення новоутворень або хвороби Бехчета не виявлено. Антинуклеарне антитіло було негативним.
Його лікування включало внутрішньовенну антикоагулянтну терапію гепарином, яку згодом вводили перорально. Вітамін В12 давали у високій дозі внутрішньовенно. На 7 день його гемоглобін становив 11 г/дл.
Після 6-місячного періоду спостереження при застосуванні кобаламіну та перорально антикоагулянту рівень його гемоглобіну та гомоцистеїну в плазмі був у межах норми. Він залишався вільним від тромботичних явищ протягом 3 років після спостереження.
Випадок 3
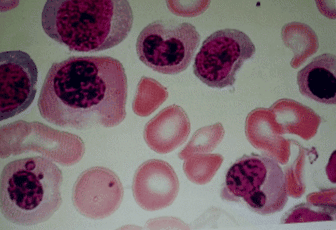
58-річний марокканець подав до нашої лікарні анемію та набряк правої ноги. Він не мав історії хвороби, а фізикальний огляд показав блідість та ознаки флебіту правої ноги. УЗД виявило тромбофлебіт правої стегнової та підколінної вен. Рівень його гемоглобіну становив 8,6 г/дл, а середній корпускулярний об’єм - 115 мкм 3. Рівень його гомоцистеїну в плазмі становив 200 мкмоль/л (норма 120), а рівень фолієвої кислоти в плазмі був нормальним. Аспірація кісткового мозку при біопсії показала мегалобластоз (рис. 1). Антитіла до парієтальних клітин шлунка були позитивними, тоді як антитіла до внутрішнього фактора були нормальними; ендоскопія виявила анальний атрофічний гастрит. Жодної іншої аномалії на більш детальному екрані для виявлення новоутворень або хвороби Бехчета не виявлено. Тести на антинуклеарні антитіла були негативними.
Аспірація кісткового мозку показала мегалобластоз
Його лікування включало внутрішньовенну антикоагулянтну терапію гепарином, яку згодом вводили перорально. Вітамін В12 давали у високій дозі внутрішньовенно. На 15 день його гемоглобін становив 10 г/дл. Після 6-місячного періоду спостереження при застосуванні кобаламіну та перорально антикоагулянту рівень його гемоглобіну та гомоцистеїну в плазмі був у межах норми. Він залишався вільним від тромботичних подій протягом 4 років спостереження.
Випадок 4
47-річна марокканка звернулася до нашого відділення лікарні з болем та набряком лівої ноги. Вона була в депресії і мала лабільний настрій протягом 1 року, а в анамнезі ішемічний інсульт міокарда 2 роки тому.
Фізичний огляд показав ознаки флебіту в лівій нозі. Рентгенографія грудної клітки та електрокардіограма були нічим не примітними. Її гемоглобін становив 12 г/дл; її середній корпускулярний об’єм становив 85 мкм 3. Її протромбіновий час, частковий тромбопластиновий час та рівень фібриногену були нормальними.
УЗД виявила тромбофлебіт у лівій підколінній вені. Не було клінічних чи біологічних доказів новоутворень, хвороби Бехчета, антифосфоліпідного синдрому, тромбофільних відхилень або системної вовчака. Рівень її гомоцистеїну в плазмі становив 167 мкмоль/л (норма 120). Рівень фолієвої кислоти в її плазмі був нормальним. У неї також був нормальний рівень тромбоцитів, нормальний рівень білка С і білка S та нормальна функція антитромбіну III. Генетичне тестування на фактор V мутації Лейдена та фактора II було негативним. Антитіла до внутрішнього фактора були позитивними. Ендоскопія виявила хронічний гастрит та наявність хелікобактер пілорі. Жодної іншої аномалії на більш детальному екрані для виявлення новоутворень або хвороби Бехчета не виявлено. Лікування включало пероральну антикоагуляційну терапію та добавки кобаламіну, спочатку парентеральні. Після 3-річного періоду спостереження вона залишалася вільною від психічних розладів та тромботичних подій. Рівень її гомоцистеїну в плазмі був у межах норми.
Обговорення
Перший випадок оригінальний тим, що психіатричні прояви та легенева емболія були першими проявами перніціозної анемії, пов’язаної з гіпергомоцистеїнемією. Після прийому вітаміну В12 його клінічні та біологічні відхилення зникли.
У випадку 4, ішемічний інсульт міокарда та депресія були, мабуть, першими проявами гіпергомоцистеїнемії, пов'язаної з перніціозною анемією. Крім того, у випадках 1 та 4 були психічні розлади, які повністю пройшли після прийому вітамінів. У літературі психіатричні прояви часто асоціюються із згубною анемією, включаючи депресію, манію, психоз та деменцію; ці прояви спостерігаються за відсутності інших добре розпізнаних неврологічних та гематологічних ознак (подібно до випадку 4) протягом місяців або років [17, 18].
Гомоцистеїн синтезується двома метаболічними шляхами: реметилуванням та транссульфурацією. Ці шляхи потребують вітаміну В12 та фолату для синтезу метіоніну та піридоксаль-5 фосфату для синтезу цистатіоніну [5].
Гіпергомоцистеїнемія може бути пов'язана з генетичними дефектами, такими як дефіцит CBS або термолабільний варіант MTHFR, або з дефіцитом супутніх вітамінів групи В.
Вважалося, що основною патофізіологічною ланкою між цими вітамінами та венозним тромбозом є накопичення гомоцистеїну через зниження концентрації цих вітамінів групи В. Однак усі ці вітаміни виконують незалежну від гомоцистеїну роль, пов’язану з розвитком венозного тромбозу. Крім того, гіпергомоцистеїнемія пригнічує інактивацію фактора Va активованим білком С і може посилити дію фактора V Лейдена [6, 19].
Важка гіпергомоцистеїнемія (> 100 мкмоль/л) найчастіше спричинена дефіцитом КБС. Помірна або помірна гіпергомоцистеїнемія може бути наслідком відносного дефіциту фолієвої кислоти та вітаміну В12 та гомозиготності загального поліморфізму 677CT у MTHFR ген [20].
Спадкову метаболічну патологію можна запідозрити, коли у пацієнтів спостерігаються періодичні епізоди тромбоемболії, що трапляються в ранньому віці, або тромбози в незвичних місцях.
Випадки 2, 3 та 4 мали важку гіпергомоцистеїнемію. Ми підозрювали генетичну мутацію MTHFR або CBS або інші генетичні мутації, але цих тестів у нашій лікарні не було. Однак можна припустити, що у наших пацієнтів цих дефіцитів не було з огляду на їх клінічну картину та сприятливий результат лише при застосуванні препарату В12.
Дефіцит CBS характеризується вивихом кришталика, аномаліями скелета, неврологічними порушеннями та тромбоемболією. Дефіцит MTHFR призводить до різних неврологічних симптомів, починаючи від затримки розвитку і закінчуючи енцефалопатією, включаючи порушення моторики та ходи, судоми, психічні прояви та, рідко, інсульти. Лікування КБС залежить від вітаміну В6, тоді як дефіцит MTHFR можна ефективно лікувати вітаміном В12, фолієвою кислотою та бетаїном [5, 20].
Дослідження з використанням даних Національного обстеження здоров’я та харчування (NHANES) між 1999 і 2002 рр. Показало, що учасники з дефіцитом вітаміну В12 та високим вмістом фолатів у сироватці крові мали підвищений рівень гомоцистеїну порівняно з учасниками, які мали комбінацію дефіциту вітаміну В12 та низької концентрації фолієвої кислоти в сироватці крові, вказує на роль рівня фолатів у ферментативних функціях вітаміну В12 [20].
У наших випадках ми припускаємо, що нормальний рівень фолієвої кислоти міг сприяти затримці діагностики перніціозної анемії, що призводить до важкої гіпергомоцистеїнемії та, як наслідок, розвитку судинних травм та гіперкоагуляції. Однак відсутність сімейних анамнезів для атеротромботичних захворювань разом із нормалізацією рівня їх гомоцистеїну після парентерального прийому вітаміну В12 настійно свідчать про те, що порушення всмоктування вітаміну В12, спричинене перніціозною анемією, є основною причиною важкої гіпергомоцистеїнемії.
Нестача вітаміну В12, фолієвої кислоти та вітаміну В6 пов’язана із змінним підвищенням рівня гомоцистеїну [5, 21]. Залишається незрозумілим, чи тягне гіпергомоцистеїнемія різних причин однаковий ризик тромбозу.
Для пояснення того, як гіпергомоцистеїнемія може призвести до венозного тромбозу, пропонується багато гіпотез. Однією з гіпотез є те, що гомоцистеїнемія надає токсичну дію на ендотелій судин та крапковий каскад [1]. Крім того, гомоцистеїн має кілька прокоагулянтних властивостей, включаючи зменшення зв'язування антитромбіну III з ендотеліальним сульфатом гепарану, збільшення спорідненості між ліпопротеїном (а) та фібрином, індукцію активності тканинного фактора в ендотеліальних клітинах та пригнічення інактивації фактора V активованим білком С [22, 23].
Кілька клінічних досліджень повідомляли про більш поширене збільшення рівня гомоцистеїнемії у пацієнтів з венозним тромбозом, ніж у контрольних групах [24]. Однак зв'язок між гіпергомоцистеїнемією та венозним тромбозом залишається суперечливою. Багатофакторний аналіз дослідження «випадок-контроль» показав, що низька концентрація метіоніну та низька кількість метилфолату в еритроцитах, але не гомоцистеїн, є факторами ризику венозного тромбозу, що свідчить про те, що гомоцистеїн є лише маркером дефіциту вітаміну [21]. Браттстрем та ін. [25] не виявили суттєвих відмінностей у концентрації гомоцистеїну в плазмі між здоровими учасниками контролю та пацієнтами з венозною тромбоемболією (ВТЕ). Сокіл та ін. [26] повідомили про високу поширеність гіпергомоцистеїнемії у пацієнтів віком до 40 років, які мали ВТЕ. Ducros та ін. [7] показав, що гіпергомоцистеїнемія легкого та помірного ступеня, здається, не є сильним фактором, що визначає ВТЕ. Також, Екім та ін. [6] виявили поширеність гіпергомоцистеїнемії (15%) у пацієнтів з тромбозом глибоких вен. У цьому дослідженні було 26 пацієнтів (43,3%) з низькою концентрацією фолатів, з них у п’яти осіб була гіпергомоцистеїнемія. Це дослідження свідчить про те, що гіпергомоцистеїнемія та низьке споживання фолієвої кислоти можуть бути фактором ризику тромбозу глибоких вен.
Тим не менше, невідомо, чи може терапія, що знижує гомоцистеїн, така як фолієва кислота, вітамін В6 або вітамін В12, змінити тромбогенний потенціал гіпергомоцистеїнемії у профілактиці рецидивуючого венозного тромбозу [27].
Незважаючи на низьку кореляцію між гіпергомоцистеїнемією та дефіцитом кобаламіну, а також гіпергомоцистеїнемією та тромбозом, у літературі опубліковано щонайменше 20 випадків венозного тромбозу на тлі дефіциту вітаміну В12. Перевага чоловіків надзвичайна. У багатьох випадках гіпергомоцистеїнемія, вторинна після перніціозної анемії, виявлялася тромбозом. На додаток до нашого першого пацієнта, опубліковано лише п’ять випадків [10, 13, 14, 28, 29] перніціозної анемії, виявленої легеневою емболією.
Також повідомлялося про інші асоційовані стани гіперкоагуляції, що включають антикардіоліпінові антитіла, мутацію фактора II, ВІЛ-інфекцію із підвищеним фібриногеном, мутацію фактора VIII та оральну контрацепцію. Механізм взаємодії гомоцистеїну та інших тромбофільних факторів не ясний. У всіх зареєстрованих випадках рівень гомоцистеїну та кобаламіну нормалізувався після терапії кобаламіном без рецидивів тромботичних подій.
Однак зниження незначно підвищених рівнів гомоцистеїну у пацієнтів із захворюваннями судин та без них із застосуванням вітамінних добавок не показало зменшення серцево-судинних подій у ряді проспективних та рандомізованих клінічних досліджень [30,31,32]. Сильне підвищення рівня гомоцистеїну має бути виправлене відповідною вітамінною терапією для запобігання судинних ускладнень [29].
Висновки
Ці випадки демонструють, що дефіцит вітаміну В12, спричинений перніціозною анемією, може призвести до сильно підвищеного рівня гомоцистеїну, який можна швидко скорегувати за допомогою добавок вітаміну В12 та запобігти повторним тромботичним подіям. Таким чином, ці умови повинні залишатися у свідомості клініциста, особливо коли тромбоз виникає разом з біологічними відхиленнями, такими як анемія, мегалобластоз або гемоліз.
- Що таке венозна тромбоемболія CDC
- Розуміння історії визначення випадків та критеріїв Постачальники медичних послуг Myalgic
- Глікемічний індекс Gi Diet Express для зайнятих людей, Галоп, Рік Файн М'яка обкладинка (2007) Перший
- Безглютенова дієта не забувайте про харчування! Справа Шеллі, РД
- Кишечник; вісь мозку Новий патогенний погляд на неврологічні симптоми; Опис педіатричного випадку